Clear Sky Science · he
בדיקה של נוזלי יונים מבוססי Acoramidis כיציבים פוטנציאליים לטרנסתירטין באמצעות חישובי DFT, עיגון מולקולרי ומחקרי ADMET
מדוע קשה כל כך לפתח כדור עבור מחלת לב נדירה
אמילואידוזיס של טרנסתירטין (ATTR) היא מחלה קשה שבה חלבון בדם מצטבר בלב ובעצבים ופוגע בהם בהדרגה. תרופה חדשה, Acoramidis, יכולה לסייע לעצור את ההצטברות הזו, אבל יש בעיה מעשית: התרופה מתמוססת בקושי במים, מה שמקשה על הספיגה שלה בגוף כאשר נלקחת כגלולה. מחקר זה בוחן גישה חכמה להמיר את Acoramidis לצורות מלוחות חדשות, המכונות נוזלי יונים, שעשויות להפוך את התרופה לקלה יותר לבליעה ויעילה יותר.
להפוך תרופה מבטיחה לצורה שתימס בשתייה
כדי שגלולה תעבוד, עליה קודם כל להימס בנוזלים המימיים של הקיבה והמעיים, ואז לעבור דרך דופן המעי למחזור הדם. Acoramidis יעילה בייצוב חלבון ה-TTR, מה שעוזר למנוע הצטברות מזיקה של חלבונים הקשורה ל-ATTR, אך היא דלה בפתירות ובזמינות ביולוגית דרך הפה. החוקרים ניסו לפתור זאת על ידי חיבור כימי של Acoramidis עם מולקולות שותפות טעונות שונות, ויצרו שלוש גרסאות חדשות של נוזלי יונים (IL1, IL2 ו-IL3). גרסאות אלה עוצבו להתנהג יותר כמו מלחים זורמים מאשר גבישים קשיחים, מה שעשוי לשפר את הפתרון והפיזור של התרופה בגוף. 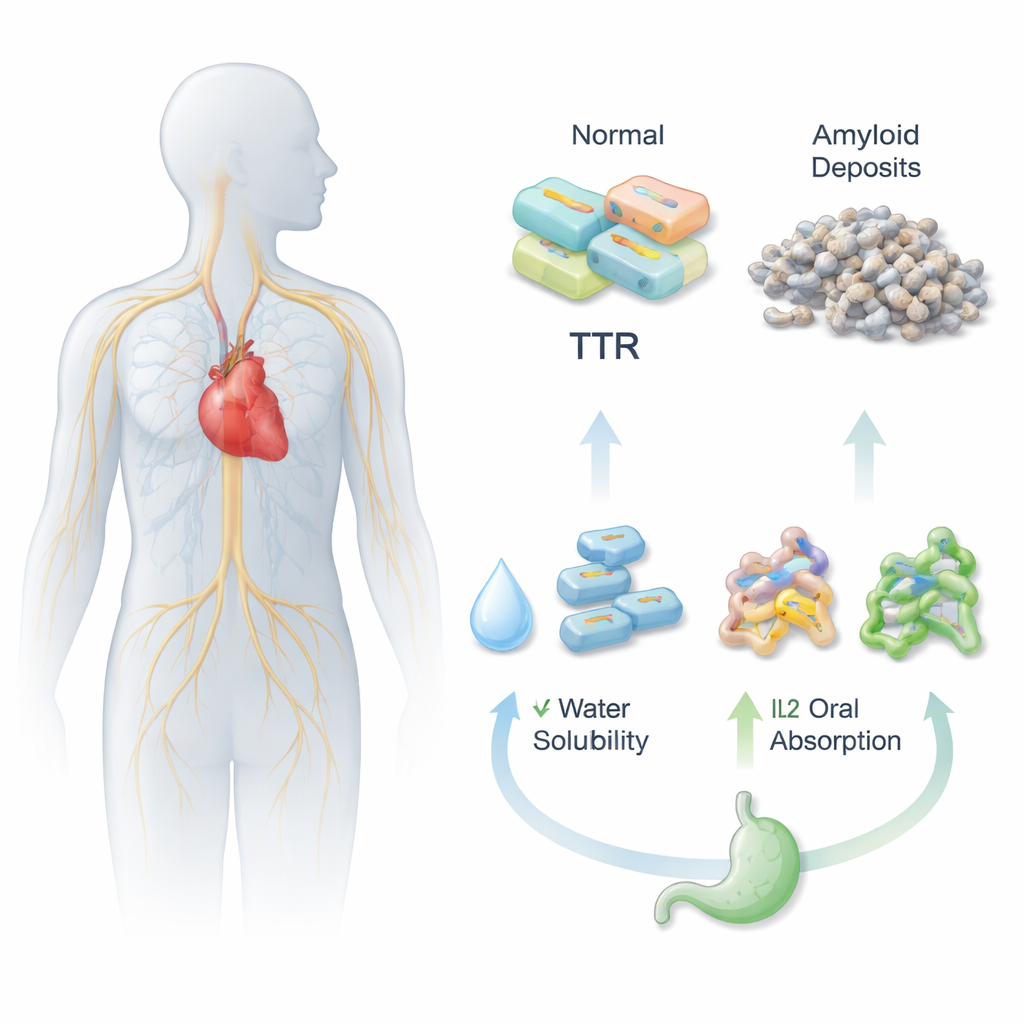
חקר המולקולות החדשות במחשב
במקום לעבור מיד לניסויים בבעלי חיים או בבני אדם, הצוות השתמש בשיטות מחשב מתקדמות כדי לחזות כיצד הצורות החדשות יתנהגו. חישובי כימיה קוונטית העריכו עד כמה כל מולקולה פולארית — מדד עיקרי לפתירות במים — וכמה בקלות האלקטרונים שלה משתנים, מה שקשור לאופן שבו היא עשויה ליצור אינטראקציות עם חלבונים. IL1 בלטה עם המומנט הדיפול הגבוה ביותר והתגובה האלקטרונית החזקה ביותר, דבר המצביע על כך שהיא אמורה להימס טוב יותר במים וליצור קשרים חזקים וגמישים יותר עם המטרות שלה. חישובי אנרגיה הציעו גם כי IL1 יציבה תרמית יותר מהתרופה המקורית ומהשני נוזלי היונים האחרים, כלומר היא צפויה להתפרק פחות לפני הגעה ליעד.
עד כמה התרופה יכולה להיאחז במטרה שלה
לאחר מכן השתמשו החוקרים בעיגון מולקולרי, מבחן וירטואלי של "מנעול ומפתח", כדי לבדוק עד כמה Acoramidis ושלוש הצורות היוניות שלה מתאימות לתעלת הקשירה של חלבון TTR. כל ארבעת התרכובות נקשרו לאזור המתאים ב-TTR, אך IL1 יצרה את האחיזה החזקה ביותר, עם אנרגיית קשירה המועדפת ביותר ומספר מגעים מייצבים — במיוחד קשרי מימן — עם חומצות אמינו מרכזיות בחלבון. קשירה חזקה יותר זו מרמזת כי IL1 עשויה להיות אף טובה יותר מהתרופה ההתחלתית בשמירה על TTR במבנה הבטוח שלו בארבע יחידות, ובכך לסייע במניעת הפירוק והקיפול השגוי שמובילים להצטברויות אמילואיד.
האם הגוף יספוג ויפרק את הצורות החדשות?
לבסוף, הצוות השתמש בכלים פרמקולוגיים מקוונים כדי לבדוק כיצד הגוף עשוי להתמודד עם תרכובות אלה — עד כמה הן נמסות, חוצות את דופן המעי, נסיעות במחזור הדם ומסולקות לבסוף. כל שלושת נוזלי היונים צפויים להיות מסיסים יותר במים מאשר Acoramidis, כאשר IL3 הראה את הפתרון הגולמי הגבוה ביותר. מדדי חדירות מעי וקליטה דרך הפה השתפרו עבור שלוש הגרסאות היוניות, כאשר IL1 ו-IL2 נתנו את האיזון הטוב ביותר בין חדירת מעי לזמינות ביולוגית צפויה. קשירת חלבונים בדם, שיעורי ניקוי וחצאי חיים השתנו גם הם בצורה שמרמזת כי צורות נוזלי היונים עשויות להציע חשיפה מהימנה יותר לאחר מתן דרך הפה, כאשר IL1 שוב מציגה פרופיל מומלץ במיוחד. 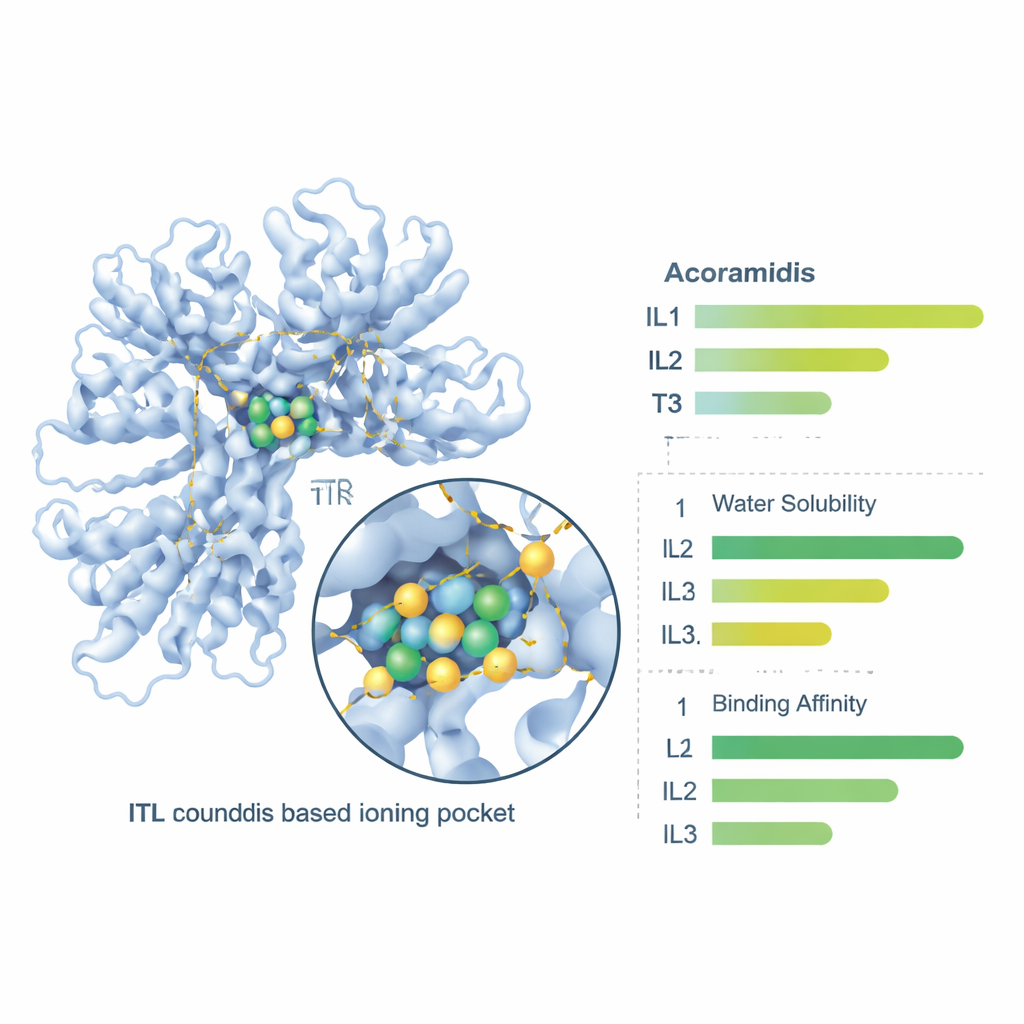
מה זה יכול להגיד על טיפולים עתידיים ל-ATTR
ללא רקע מקצועי, המסר המרכזי הוא ש-Acoramidis כבר נראית מבטיחה עבור מחלה נדירה אך קשה של הלב והעצבים, אך הפתרוליות הדלה שלה מגבילה את היעילות דרך הפה. על ידי המרת Acoramidis לנוזלי יונים מעוצבים במיוחד, מחקר זה מראה — כולו באמצעות בדיקות ממוחשבות — כי יתכן שניתן ליצור גרסאות המתמוססות טוב יותר, נקשרות בחוזקה רבה יותר למטרה החלבונית ונספגות ביעילות גבוהה יותר. מבין שלושת המועמדים, IL1 נראה כמי שמאזן הכי טוב בין יציבות, כוח קשירה, פתירות וקליטת פה צפויה, מה שהופך אותו למועמד מוביל לפיתוח מעבדתי וקליני עתידי שמטרתו לספק טיפולים יעילים יותר וקלים לנטילה ל-ATTR.
ציטוט: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
מילות מפתח: אמילואידוזיס של טרנסתירטין, Acoramidis, נוזלי יונים, קיפול מוטעה של חלבונים, מתן תרופתי דרך הפה