Clear Sky Science · he
ניתוח משולב של פרוטאומיקה ומטבולומיקה חושף הפרעת מטבוליזם חומצות אמינו בתאי לויקמיה חדה עמידים לאדריאמיצין
מדוע חלק מתרופות ללוקמיה מפסיקות להשפיע
כימותרפיה שינתה את הטיפול בלויקמיה מיולואידית חריפה (AML), סוג של סרטן דם בעל קצב גדילה מהיר. עם זאת, אצל מטופלים רבים המחלה חוזרת כי תאי הסרטן לומדים לשרוד את אותן תרופות שנועדו להשמידם. המחקר הזה שואל שאלה פשוטה אך קריטית: אילו שינויים מתרחשים בתוך תאי הלויקמיה כאשר הם הופכים לעמידים לאדריאמיצין, אחת מתרופות הכימותרפיה הסטנדרטיות, והאם שינויים אלה עשויים להצביע על דרכים חדשות לשחזור יעילות התרופה?
מציצים לתוך תאי הלויקמיה
כדי לבדוק זאת השוו החוקרים קו תאי אנושי נפוץ של AML, הנקרא HL60, עם קו אחות שהפך לעמיד לאדריאמיצין (HL60/R). במקום לבחון גן או חלבון אחד בכל פעם, הם השתמשו בשתי גישות רחבות ומשלימות. פרוטאומיקה מדדה אלפי חלבונים שונים — המולקולות המבצעות של התא. מטבולומיקה מדדה מאות מולקולות קטנות המרכיבות את המטבוליזם התאי, כולל שומנים, סוכרים וחומצות אמינו. על ידי שילוב שכבות 'אומיקס' אלה, הקבוצה בנתה תמונה מפורטת של הדרכים בהן תאים עמידים שונים מעמיתיהם הרגישים.
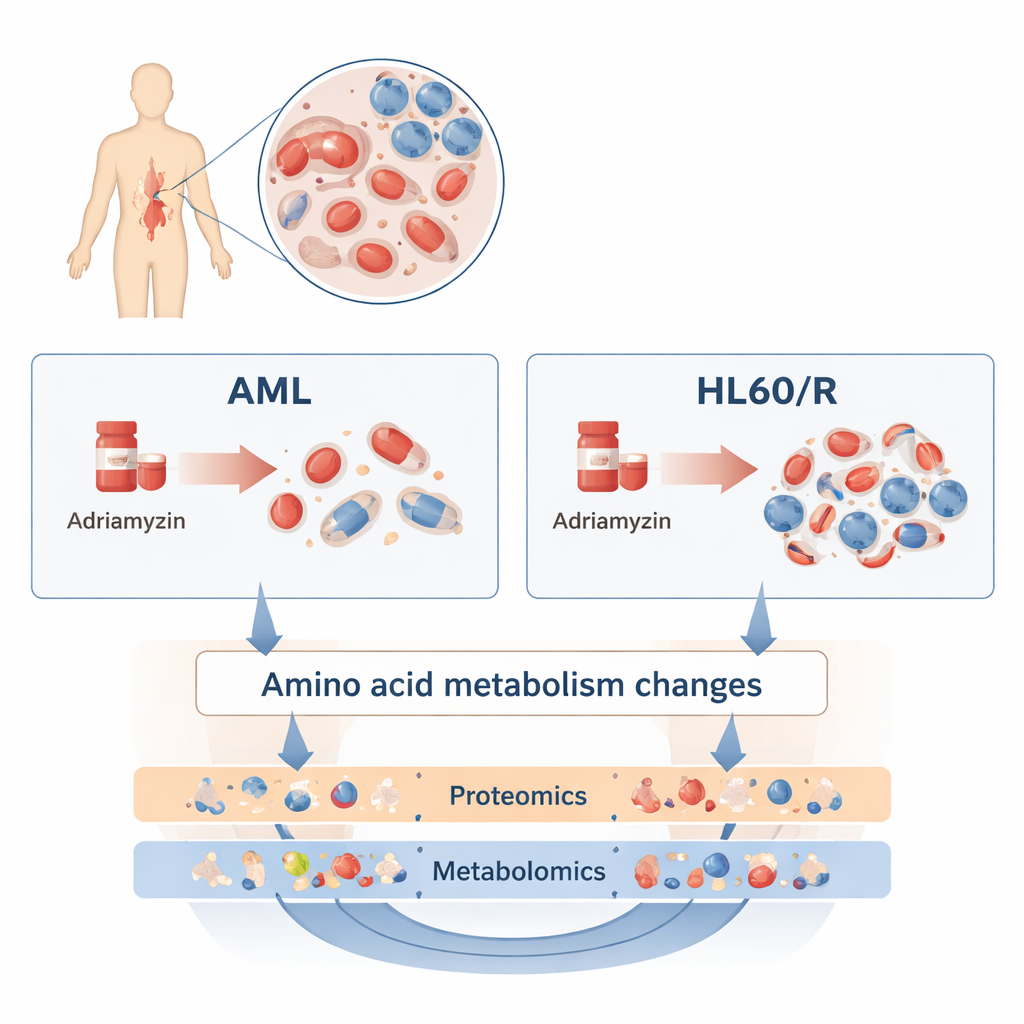
כיוונון מחדש נרחב של מכונת התא
סקר הפרוטאומיקה חשף שינויים נרחבים: יותר מ-3,200 חלבונים הופיעו ברמות גבוהות או נמוכות יותר בתאים העמידים לאדריאמיצין בהשוואה לתאי HL60 הרגילים. רבים מהחלבונים האלה התרכזו במסלולים ששולטים באופן שבו תאים משתמשים באנרגיה ומגיבים ללחץ. במיוחד, חלבונים במסלול איתות cAMP, במסלול HIF-1 (המסייע לתאים להתמודד עם חוסר חמצן) ובפורזיציה חמצונית (oxidative phosphorylation), תהליך מרכזי לייצור אנרגיה במיטוכונדריה, הראו שינויים. הזזות אלה מצביעות על כך שתאי לויקמיה עמידים מתכנתים מחדש את דרכי הנשימה, הגדילה והאיתות שלהם כדי לעמוד בכימותרפיה.
המטבוליזם משנה כיוון לעבר חומצות אמינו
ניתוח המטבולומיקה סיפר סיפור משלים. מתוך כ-1,400 מטבוליטים שזוהו, 260 השתנו באופן מובהק בתאים העמידים. מודלים סטטיסטיים הפרידו בצורה ברורה בין תאים עמידים ללא עמידים, מה שמעיד על טביעת מטבולית עקבית של עמידות. כאשר המוטבוליטים שהשתנו נזרקו למיפוי על מסלולים ביוכימיים ידועים, כמה מסלולים בלטו. רבות מהנתיבים המושפעים ביותר היו קשורים לחומצות אמינו — אבני הבניין של חלבונים — ובמיוחד אלה הכוללים אלנין, אספרטאט, גלוטמט, ציסטאין, מתיונין וגלוטתיון. רשתות נוספות, כגון מטבוליזם הפורינים והפירימידינים (חשובים ל-DNA ו-RNA) וטיפול בסוגים מסוימים של שומנים, הופרעו גם הן, מה שמחזק כי העמידות קשורה לרה-ארגון מטבולי נרחב.
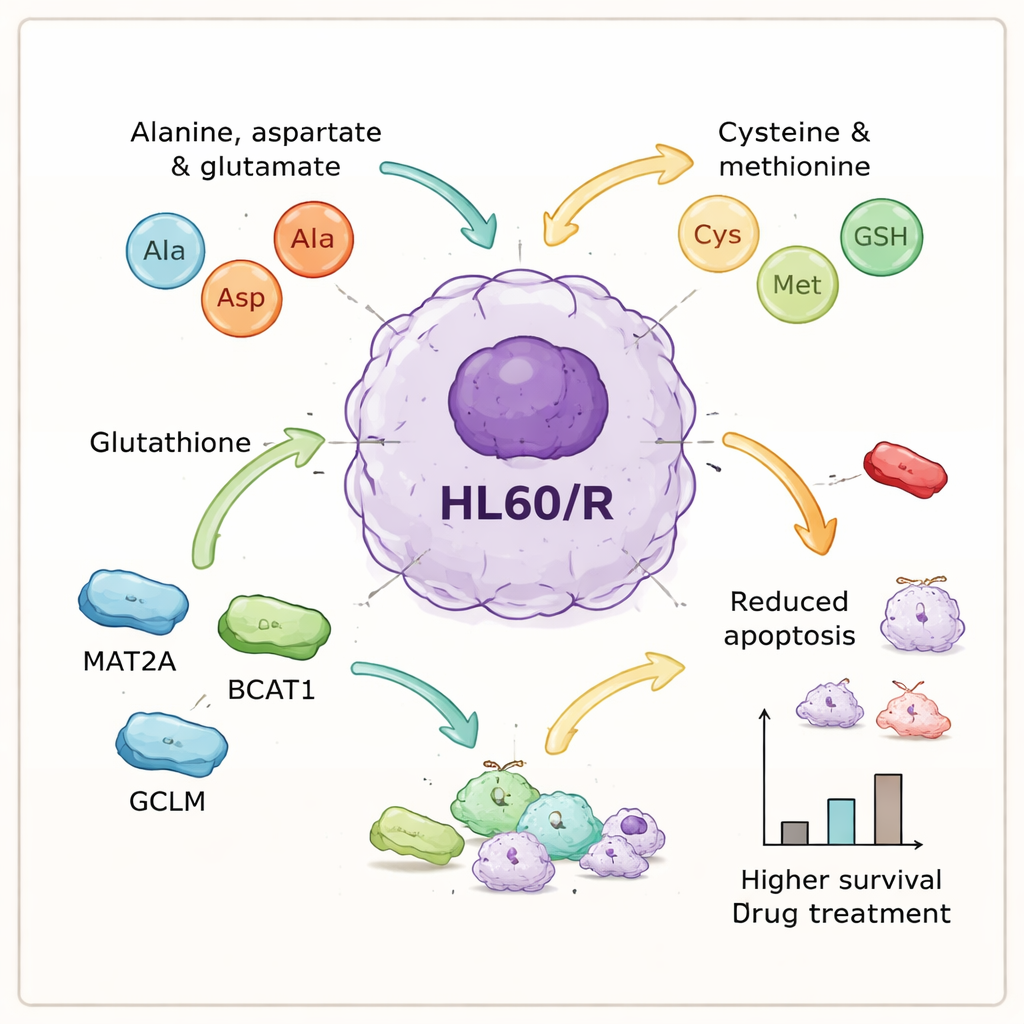
שחקנים מולקולריים מרכזיים שעוזרים לתאי הסרטן להחזיק מעמד
על ידי שילוב נתוני החלבון והמטבוליט, המחברים זיהו סט של תהליכים הקשורים לחומצות אמינו שנראו מרכזיים לעמידות. הם בחרו שש חלבונים הקשורים למסלולים אלה — GOT1, GPX1, AHCY, MAT2A, BCAT1 ו-GCLM — לבדיקה מדוקדקת יותר. ניסויים במעבדה אישרו שחמישה מהם נוכחו בשפע רב יותר בתאים העמידים, בהתאם לרעיון שהעיבוד של חומצות האמינו מואץ, בעוד אנזים אנטי-חמצוני אחד, GPX1, ירד ברמתו. כדי לבדוק סיבה ותוצאה השתמשה הקבוצה ב-RNAi להורדת הביטוי של שלושה מהחלבונים המועלים — MAT2A, BCAT1 ו-GCLM — בתאים העמידים. כאשר חלבונים אלה דוכאו, התאים עברו שיעור גבוה יותר משמעותית של מוות מתוכנת לאחר הטיפול, כלומר הם איבדו חלק ניכר מההגנה שרכשו נגד אדריאמיצין.
מה המשמעות לטיפולים עתידיים
במבט כולל, ממצאים אלה מרמזים שתאי AML עמידים לאדריאמיצין שורדים לא רק בגלל מוטציות בודדות, אלא משום שהם מעצבים מחדש את הכימיה הפנימית שלהם, כאשר מטבוליזם חומצות האמינו מהווה ציר מרכזי. על ידי סילוק משאבים נוספים לתוך מסלולים מסוימים של חומצות אמינו וגלוטתיון, התאים נראים טובים יותר בניהול מתח, תיקון נזקים והימנעות ממוות חשוף כימותרפיה. עבור הקהל הרחב, המסר המרכזי הוא שעמידות אינה אקראית: היא עוקבת אחר דפוסים שניתן למדוד ואולי לכוון. בטווח הארוך, תרופות שמפריעות לחלבונים מעובדי חומצות אמינו ספציפיים כמו MAT2A, BCAT1 או GCLM עשויות להיות משולבות עם אדריאמיצין או סוכנים דומים, ולספק לכלל הרופאים כלים חדשים למנוע או להתגבר על עמידות אצל חולי לויקמיה מיולואידית חריפה.
ציטוט: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
מילות מפתח: לויקמיה מיולואידית חריפה, עמידות לתרופות, אדריאמיצין, מטבוליזם חומצות אמינו, מולטי-אומיקס