Clear Sky Science · he
מודל תאי פונקציונלי ועמיד לסקר מהיר של מודולטורים של Piezo1
למה חיישני לחץ זעירים בתאים שלנו חשובים
בכל פעם שהדם זורם בכלי הדם שלנו, או כשאנחנו פשוט עוברים חדר, תאים חווים כוח מכאני קטן. חלבון מפתח שמתפקד כ"חיישן לחץ" הקרוי Piezo1 מסייע לתאים לתרגם כוחות אלה לאותות חשמליים וכימיים שמקיימים את בריאות הרקמות. מאחר ש‑Piezo1 משתתף בהיווצרות כלי דם, בחוזק העצם, במערכת החיסון ובמחלות גנטיות נדירות, מפתחים תרופות מעוניינים למצוא מולקולות שיכולות לכוונן את פעילותו. המאמר המתואר כאן מציג דרך חדשה ומהירה יותר לחפש מולקולות כאלה באמצעות תאים מהונדסים וקריאות מבוססות אור במקום טכניקות איטיות ומצריכות עבודה מרובה.
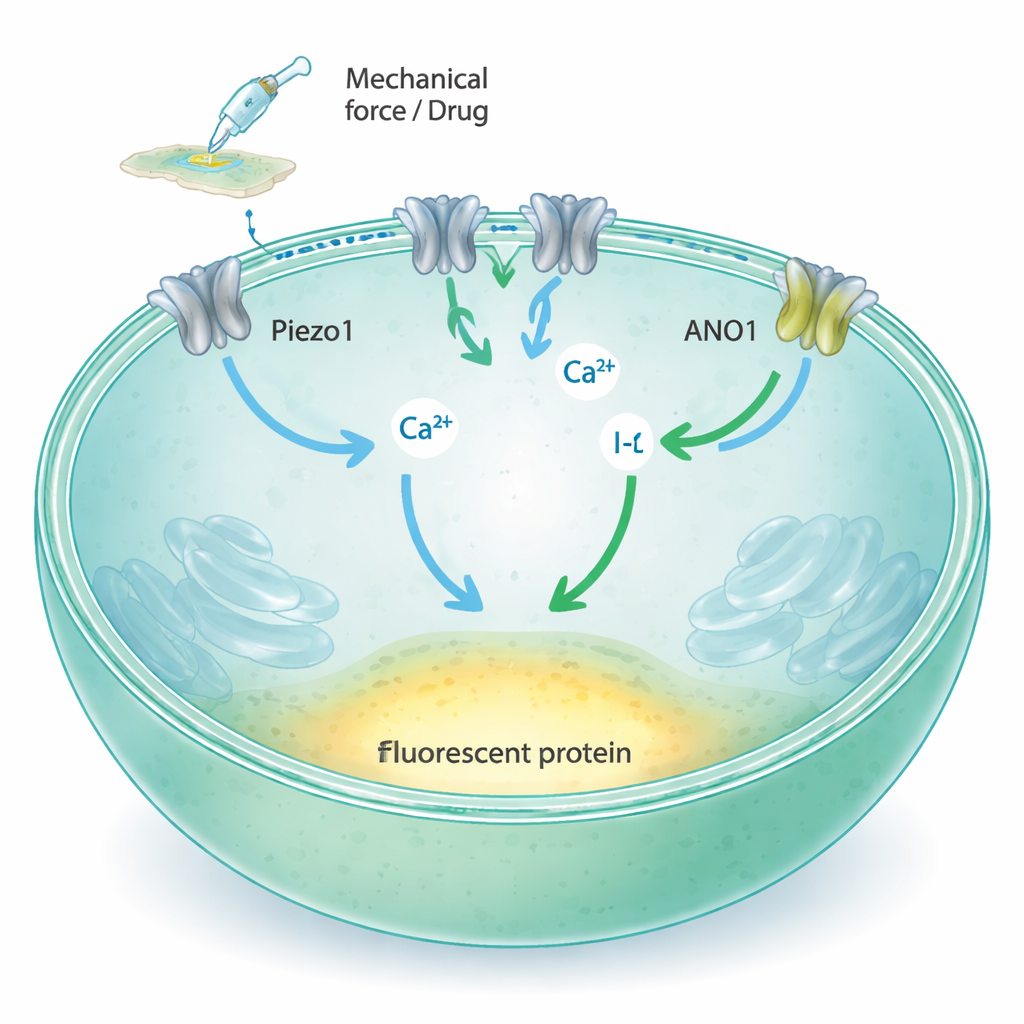
להפוך מגע לאות אור
Piezo1 הוא ערוץ בממברנת התא שנפתח כאשר הממברנה נמתחת או נדחפת, ומאפשר לסידן ויונים אחרים לזרום לתוך התא. שיטות מסורתיות לחקור ערוצים כאלה מסתמכות על אלקטרודות זכוכית דקיקות או על דיווחים פלורסצנטיים מיוחדים, שיכולות להיות עוצמתיות אך קשות להרחבה לאלפי בדיקות הנדרשות לגילוי תרופות מודרני. המחברים שאפו להמיר את פעילות Piezo1 לשינוי פשוט באור שניתן למדוד במהירות באמצעות קורא פלטות על דגימות רבות במקביל. רעיון שלהם היה לקשר את Piezo1 לשני רכיבים נוספים: ANO1, ערוץ יונים נוסף שמגיב לסידן, וחלבון פלואורסצנטי צהוב מותאם שמאבד בהירות כאשר נחשף ליאודיד.
בניית תא בדיקה רגיש
החוקרים התחילו מתאי Fischer Rat Thyroid (FRT), שמייצרים באופן טבעי Piezo1 ומידבקי היטב לצלחות פלסטיק סטנדרטיות. הם אישרו שתאים אלה מבטאים Piezo1 אך לא את קרובו Piezo2, והראו ש‑Piezo1 בתאים אלו מגיב לזרימת נוזלים ולחישה מכנית על ידי כניסת סידן. לאחר מכן הם הכניסו את ערוץ ANO1 ואת חלבון הפלואורסצנציה הרגיש ליאודיד (YFP‑H148Q/I152L) לתאים. כאשר ריכוז הסידן בתוך התא עולה, ANO1 נפתח ומאפשר ליאודיד להיכנס; חלבון הפלואורסצנציה נעשה עמום ככל שהיאודיד מצטבר מסביבו. תצפיות במיקרוסקופ, cytometry זרימה והקלטות חשמליות הראו כי גם ANO1 וגם החיישן הפלואורסצנטי נמצאים ברמות גבוהות ופועלים כמתוכנן.
מפועלת תרופה לזוהר הניתן למדידה
עם מערכת תלת‑חלקית זו במקום, הצוות יצר שרשרת סיבה‑ותוצאה פשוטה: אם מולקולה נבדקת מפעילה את Piezo1, סידן זולג פנימה, ANO1 נפתח, היאודיד נשאב פנימה,אות והפלואורסצנציה יורדת; אם מולקולה חוסמת את Piezo1, האות נשאר בהיר. הם אימתוו את הלוגיקה הזו בעזרת מפעילי Piezo1 ידועים (Yoda1, Jedi1, Jedi2) וחוסמים (Ruthenium Red, GsMTx4). מפעילים יצרו ירידות תלויי מינון בפלואורסצנציה, עם ערכי רגישות התואמים נתונים שפורסמו מראש. חוסמים גרמו לדפוס ההפוך, והפחיתו את התגובה ככל שהריכוז שלהם עלה. המבחן עבד רק כאשר גם סידן וגם ייאודיד היו נוכחים, מה שמדגיש שהאות באמת תלוי בכניסת סידן מונעת‑Piezo1 ובהזרמה הבאה של ייאודיד דרך ANO1. מדדים סטטיסטיים כגון גורם Z ומאזן אות‑לרעש הראו שהשיטה יציבה ואמינה דיה לסקר בתעשייה.
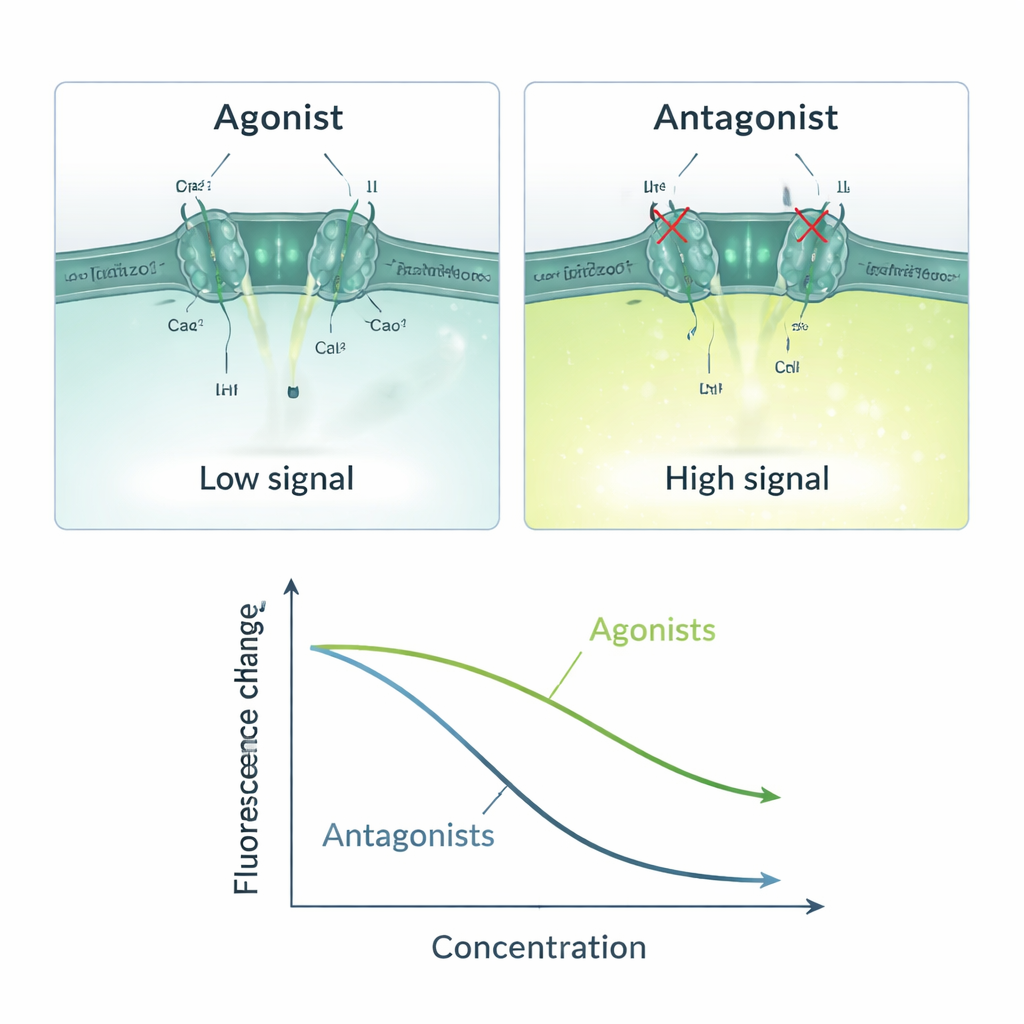
בדיקה מהירה וניתנת להרחבה עם כמה הסתייגויות
המודל התאי החדש יכול להשלים מדידת בארור יחידה בכ־14 שניות ולסרוק צלחת 96 בארוכים בכ‑22 דקות בקירוב, וניתן להתאימו למכשירים שקוראים מאות בארות במקביל. התאים המהונדסים נשארים יציבים במשך דורות רבים תחת בחירת אנטיביוטיקה, מה שמאפשר ניסויים חוזרים לאורך זמן. מאחר שהקריאה אופטית ומשתמשת בציוד מיקרופלייט סטנדרטי, הגישה יחסית זולה ונגישה. עם זאת, המחברים מציינים שהמבחן הוא עקיף: כל תרכובת הפועלת על שלבים לפני או אחרי Piezo1 בשרשרת האיתות — כגון ANO1 עצמו או חלבונים אחרים המטפלים בסידן — עלולה לייצר חיוב כוזב. לכן, ממצאים מתוך סקר זה עדיין צריכים אישור בשיטות ישירות יותר כמו אלקטרופיזיולוגיה.
מה המשמעות לעתיד הטיפולים
במונחים פשוטים, החוקרים בנו "גלאי עשן" מעבדתי שמבהק פחות בכל פעם שמולקולה דוחפת את Piezo1 להיפתח, ונשאר בהיר כש‑Piezo1 חסום. הגלאי הזה רגיש, מהיר, וקל להפעלה בכמויות גדולות, מה שהופך אותו מתאים לשלב הראשוני בחיפוש תרופות שמכוונות חיישני המגע של הגוף. בעוד שהוא לא יחליף בדיקות מעקב מפורטות יותר, המודל התאי הזה מספק נקודת פתיחה חזקה לזיהוי מולקולות שעשויות בעתיד לסייע בטיפול בהפרעות כלי דם, במחלות עצם, בבעיות חיסוניות ובהמצבים נוספים הקשורים לדרך שבה תאים חשים ומגיבים לכוח פיזי.
ציטוט: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
מילות מפתח: ערוץ Piezo1, ערוצי יונים מכאניים-רגישים, סקר בריבוי גבוה, בדיקה מבוססת תאים, גילוי תרופות