Clear Sky Science · he
סינתזה, מאפיינים, ניתוח DFT, דוקינג מולקולרי וחקירות אנטי‑סרטניות בסרטן המעי הגס של קומפלקס חדש של פיזאזול‑הידזון של אבץ(II)
למה תרופה מבוססת מתכת עשויה להילחם בסרטן המעי בעדינות יותר
תרופות סרטן רבות וחזקות מתבססות על מתכות כבדות כמו פלטינה. הן יכולות להיות אפקטיביות אך לעתים קרובות מלוות בתופעות לוואי חמורות ובהתפתחות עמידות לאורך זמן. המחקר הזה בוחן גישה שונה: מועמדת לתרופה חדשה המבוססת על אבץ, מינרל חיוני שכבר קיים בגופנו, המשולב עם שלד אורגני בשם פיזאזול‑הידזון. החוקרים בדקו האם קשירת האבץ למסגרת זו יכולה ליצור תרכובת שפוגעת בתאי סרטן המעי הגס בצורה משמעותית תוך שמירה על תאים בריאים.
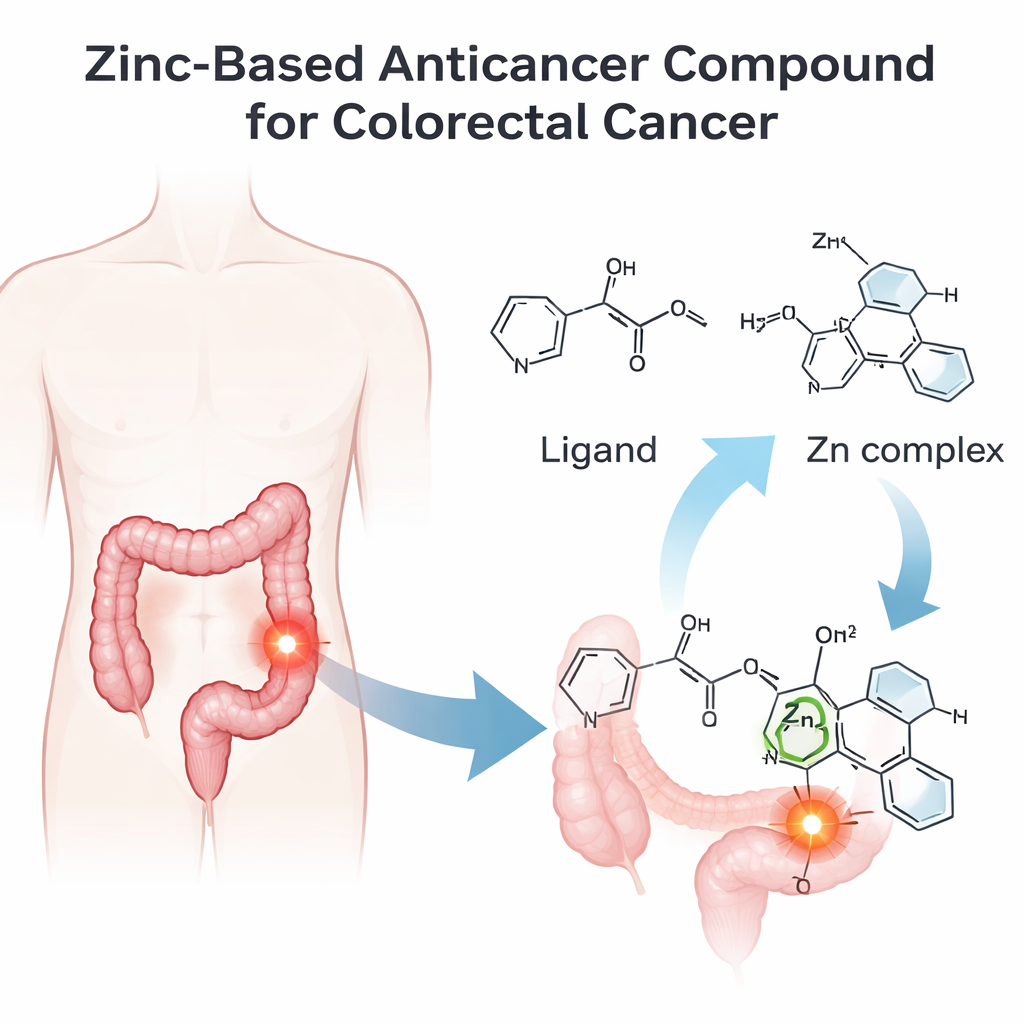
בניית מולקולה חכמה יותר מבוססת אבץ
צוות המחקר עיצב וסינתז בתחילה מולקולה אורגנית חדשה, שכונה IMP, ולאחר מכן קשרה אותה ליוני אבץ ליצירת קומפלקס האבץ שנקרא IMP‑Zn. הם אישרו את המבנה המדויק של שניהם באמצעות מערך טכניקות שהן מעין "טביעת אצבע" מולקולרית: ספקטרוסקופיית אינפרא‑אדום לזיהוי הקשרים הכימיים, תהודה מגנטית גרעינית למיפוי מיקום האטומים, ספקטרומטריית מסה לווידוא מסת המולקולה, וספקטרוסקופיית אולטרה‑סגול‑נראה לחקר אינטראקציות עם אור. ניסויים אלה, ביחד עם בדיקות מוליכות חשמלית, הראו שהאבץ מתואם באופן הדוק לשלושה אטומים מרכזיים ב‑IMP ושתי יוני כלוריד, ויוצר קומפלקס חד‑משמעי וממוקד סביב מרכז האבץ.
הביט לתוך המולקולה בעזרת כימיה וירטואלית
כדי להשלים את המדידות במעבדה, החוקרים הריצו סימולציות מחשב מפורטות באמצעות תורת הפונקציונל הצפיפות (DFT). חישובים אלה אפשרו לחזות כיצד האלקטרונים מפוזרים בתוך ה‑IMP וה‑IMP‑Zn, עד כמה כל צורה יציבה, וכמה בנקל המולקולות עשויות להשתתף בתגובות כימיות. התוצאות הראו כי ברגע שהאבץ קשור, המרווח האנרגטי בין אורביטלי החזית של המולקולה מצטמצם, כלומר האלקטרונים יכולים לנוע בקלות רבה יותר בתוך המבנה. בדרך כלל זה מתרגם לעלייה בריאקטיביות הכימית. קומפלקס האבץ גם הציג אינדקס אלקטרופיליות גבוה יותר, מה שמעיד שהוא מצויד טוב יותר לאינטראקציה עם מטרות ביולוגיות מאשר הליגנד החופשי IMP לבדו.
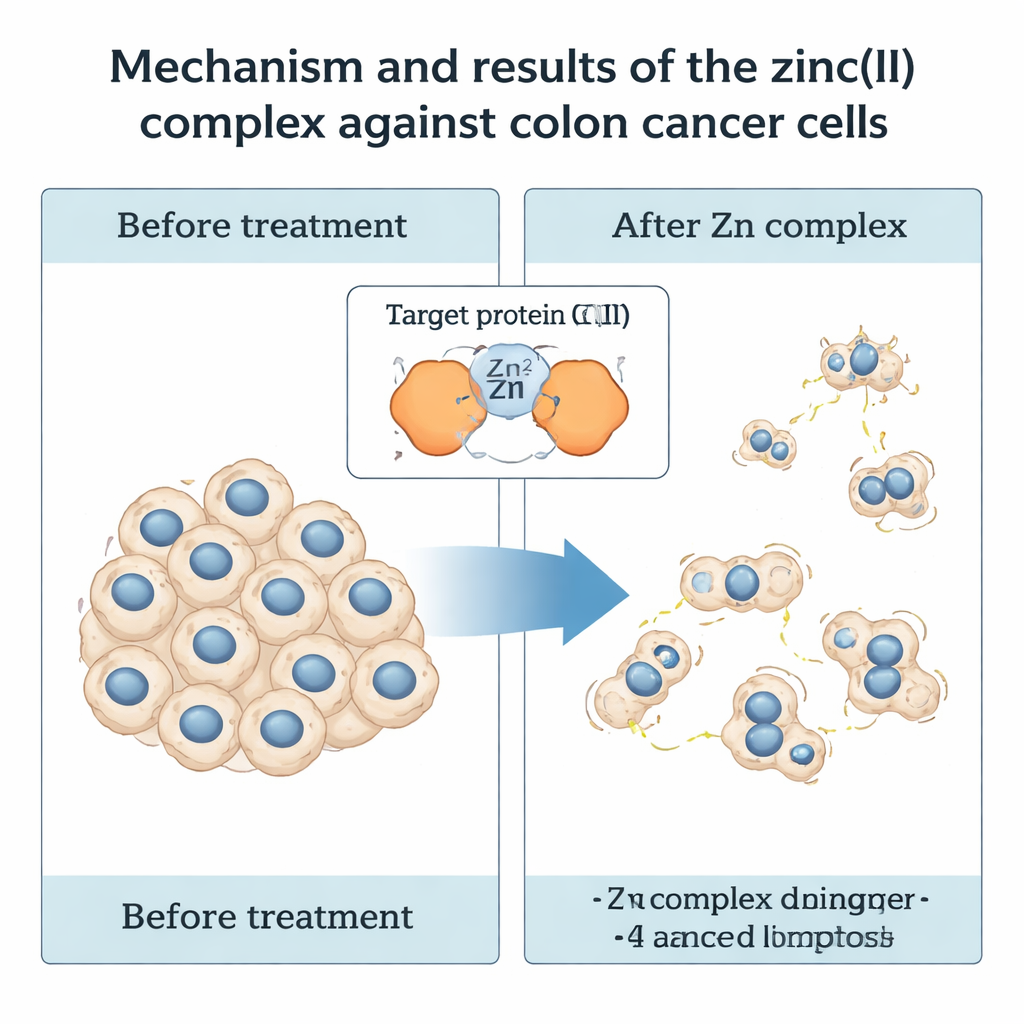
איך קומפלקס האבץ מתמודד עם תאי סרטן המעי
המבחן האמיתי היה ביולוגי. החוקרים טיפלו בתאי סרטן מעי גס אנושיים (HCT116) ב‑IMP ו‑IMP‑Zn בריכוזים וזמני חשיפה שונים, ואז מדדו כמה תאים שרדו. שתי התרכובות האטו את גדילת תאי הסרטן, אך קומפלקס האבץ היה בולט בעוצמתו: לאחר 48 שעות, IMP‑Zn קיצץ את חיוניות התאים בחצי בריכוז של כ‑25 מיקרומולר, בעוד שהליגנד לבד דרש מנה גבוהה בהרבה. חשוב לא פחות, אותו טווח ריכוזים של IMP‑Zn לא הפגין השפעה רעילה ניתנת לזיהוי על שורת תאים כלייתית אנושית נורמלית (HEK293), מה שמצביע על מידת סלקטיביות לטובת תאי הסרטן. כאשר הצוות עקב אחרי תאים מטופלים במשך שבועיים, הם מצאו כי IMP‑Zn הקטין בצורה חדה הן את מספר והן את גודל הקולוניות שהתאים היו מסוגלים ליצור, מה שמרמז כי הוא מפריע ליכולת ההתרבות לטווח הארוך שלהם.
רמזים לכך שהתאים נדחקים לעבר מוות מתוכנת
כדי להבין כיצד קומפלקס האבץ מזיק לתאי הסרטן, המדענים בחנו את מחזור התא — סדרת השלבים שהתא עובר בזמן גדילתו וחלוקתו. לאחר חשיפה ל‑IMP‑Zn, חלק גדול יותר משמעותית מתאי HCT116 הזיזו את עצמם לשלב "SubG0", חתימת חיים של תאים עם DNA מקוטע. תבנית זו מקושרת לעתים קרובות לאפופטוזה, צורה מבוקרת של מוות תאי שאליה כיוונות רבות מהתרופות האנטי‑סרטניות. סימולציות דוקינג מולקולרי סיפקו חתיכה נוספת לפאזל: מודלים וירטואליים הציעו כי IMP‑Zn נקשר בחוזקה רבה יותר מאשר IMP למספר חלבונים הקשורים לסרטן, כולל קינאזת מקבל גורמי גדילה, קינאז השולט במחזור התא, וגם אנזים המעורב במטבוליזם של תרופות. אינטראקציות הדוקות יותר אלה תומכות ברעיון כי תאום האבץ מסייע לתרכובת לשים עין על מכניקה תאי קריטית ולהפריע להישרדות תאי הסרטן.
מה זה עשוי לומר על טיפולים עתידיים
בסך הכל, המחקר מראה כי "קישוט" של שלד פיזאזול‑הידזון באבץ עושה יותר מאשר לשנות מינורית את הכימיה שלו: הוא הופך את IMP ליותר ריאקטיבי, חזק יותר, ובמבט ראשון גם סלקטיבי יותר נגד תאי סרטן המעי הגס. למרות ש‑IMP‑Zn רחוק עדיין מלהיות תרופה מוכנה — הוא טרם נבחן בבעלי חיים או בבני אדם — יכולתו להאט בצורה משמעותית את גדילת תאי סרטן המעי, להדחיק תאים לכיוון אפופטוזה ולשמר תאים נורמליים מסמנת אותו כחבר מבטיח בשורה גדלה של מטלותרפיה מבוססת אבץ. עבודה זו מציעה כי קומפלקסים של אבץ שמעוצבים בקפידה עשויים לספק חלופות או השלמות ממוקדות ועדינות יותר לכימותרפיה המסורתית מבוססת מתכות בעתיד.
ציטוט: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
מילות מפתח: גורמים אנטי‑סרטן מבוססי אבץ, סרטן המעי הגס, קומפלקס פיזאזול‑הידזון, דוקינג מולקולרי, אפופטוזה