Clear Sky Science · he
תפקוד מיטוכונדריאלי לקוי והפרת איזון Ca2+ בנוירונים אנושיים שהופקו מ-iPSC ונושאים מוטציית פרסנילין-1 מופיעים תחת לחץ באמצעות מנגנון בלתי תלוי ב-MCU-1
מדוע זה חשוב למחלת אלצהיימר
מחלת אלצהיימר מתוארת לעתים קרובות במונחים של משקעים חלבוניים דביקים במוח, אך הרבה לפני שהזיכרון מתפוגג, "תחנות הכוח" הזעירות בתוך תאי העצב — המיטוכונדריות — וטיפול ביוני הסידן עלולים כבר להתחיל להתקלקל. מחקר זה משתמש בנוירונים אנושיים שגודלו מתאים עור של אדם נושא מוטציה משפחתית ידועה של אלצהיימר כדי לשאול שאלה פשוטה אך מכריעה: כמה מוקדם, ובאיזה אופן, ייצור האנרגיה ואיזון הסידן מתחילים לכשל?
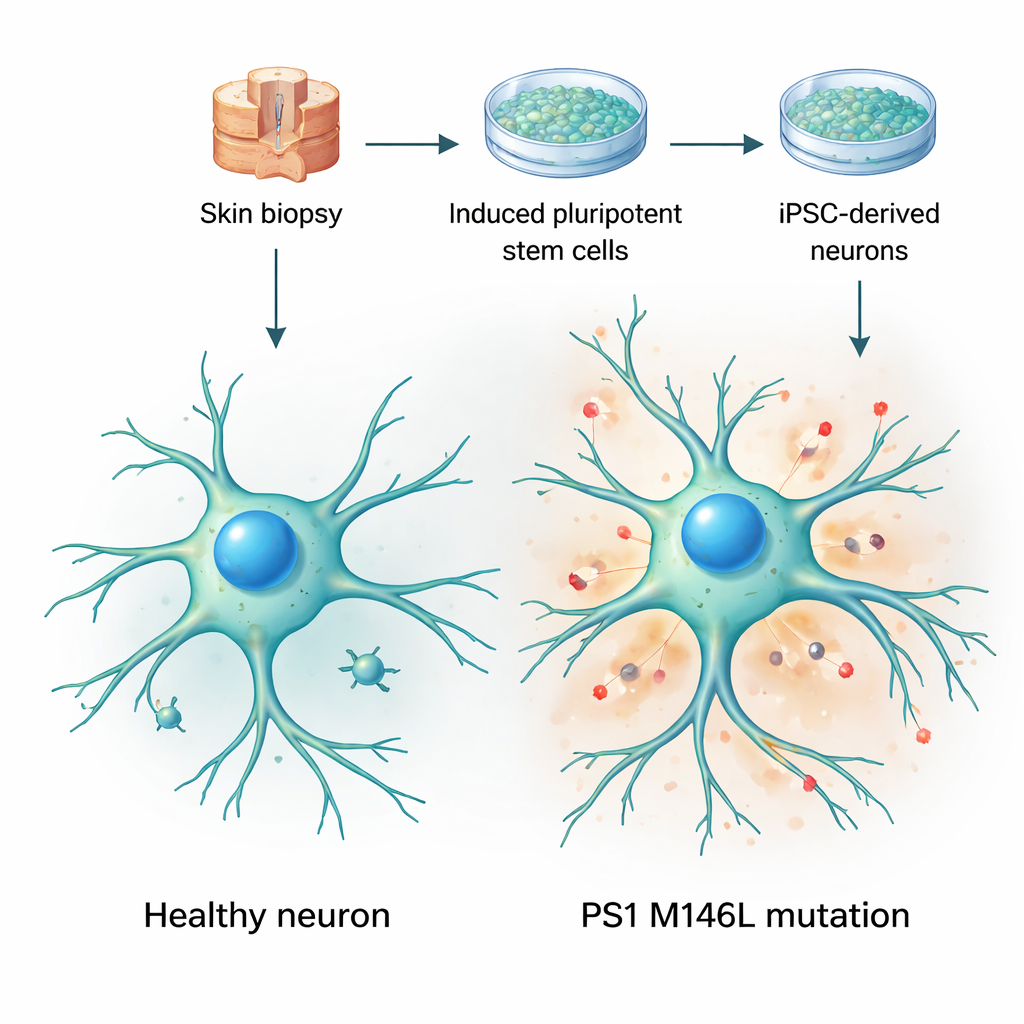
להפוך תאי עור לדגמי מוח חיים
החוקרים התחילו מביופסיות עור משתי נשים: מתנדבת בריאה ואחת נושאת ללא תסמינים של מוטציית פרסנילין-1 בשם M146L, שמופיעה במשפחה ארגנטינאית עם הופעה מוקדמת של אלצהיימר. הם תכנתו מחדש את תאי העור לתאי iPSC — תאים פלוריפוטנטיים היכולים להפוך כמעט לכל רקמה — ולאחר מכן כיוו אותם להפוך לתאי עצב. במשך שבועות מבחנה התאים הרכיבו צורות נוירונליות טיפוסיות, שלחו תהליכים ארוכים ומסועפים והביעו סמנים נוירונליים סטנדרטיים. חשוב לציין, גם תאי הבקרה וגם התאים המוטנטיים הגיעו לבגרות בקצבים דומים ונראו באופן כללי בריאים, מה שאפשר לצוות להתמקד בשינויים פונקציונליים עדינים במקום באובדן או נזק תאי גלוי.
אותות חשמליים וסידן תחת לחץ
תאי עצב מסתמכים על שליטה הדוקה בסידן, אטום טעון המשמש כמפסק מהיר לתהליכים תאיים רבים. בעזרת צבענים פלואורסצנטיים עקבו החוקרים כיצד משתנים רמות הסידן בתוך התאים כאשר הם הועלו לגירוי חשמלי עם אשלגן או הופעלו עם מולקולות איתות. בתגובה לגירוי פשוט המוליך לדה-פולריזציה, נוירונים הנושאים את מוטציית M146L הראו עליות סידן חלשות יותר בהשוואה לנוירוני הבקרה, מה שמרמז על בעיות בשמירה על מפל הריכוזים והמטענים החשמליים שמניעים כניסת סידן. עם זאת, כאשר החוקרים גרמו למצוקה חזקה יותר — אילצו דליפה של סידן מאגרי ה-ER (הרשתית האנדופלסמית) — ההבדל נעשה ברור יותר. בתגובה ללחץ זה, מיטוכונדריות בנוירונים המוטנטיים ספגו פחות סידן באופן ניכר מאשר אלה בתאי הבקרה, מה שמעיד על יכולת מצטמצמת לטשטש שגיאות סידן מסוכנות.
לנתק בין שימוש באנרגיה לאיזון סידן
כדי להבין כיצד טיפול הסידן המשתנה משפיע על המטבוליזם התאי, החוקרים מדדו כמה חמצן הנוירונים צורכים — פרוקסי ישיר לפעילות מיטוכונדריאלית. באופן מפתיע, הנוירונים עם מוטציית M146L נושמים יותר: קצבי צריכת החמצן הבסיסיים והמקסימליים שלהם, וכמות החמצן המקושרת לייצור ATP, היו גבוהים יותר מאשר בתאי הבקרה. עם זאת, היעילות של קישור שימוש בחמצן לייצור ATP נראתה דומה, ולא נצפה גידול במספר המיטוכונדריות או באנזימים מרכזיים לייצור ATP. במקום זאת, המיטוכונדריות בנוירונים המוטנטיים היו ארוכות וצינוריות יותר, עם רמות גבוהות יותר של חלבון מיזוג שנקרא מיטופוזין‑1, דפוס הנצפה לעתים בתאים תחת מתח כרוני ברמה נמוכה. מיטוכונדריות פעילות יתר אלה, המעוגלות ומוארכות, גם ייצרו יותר סוגי חמצון תגובתיים (ROS), מולקולות בלתי יציבות היכולות לגרום נזק לחלבונים ול-DNA אם לא מוגברות בשליטה מתאימה.
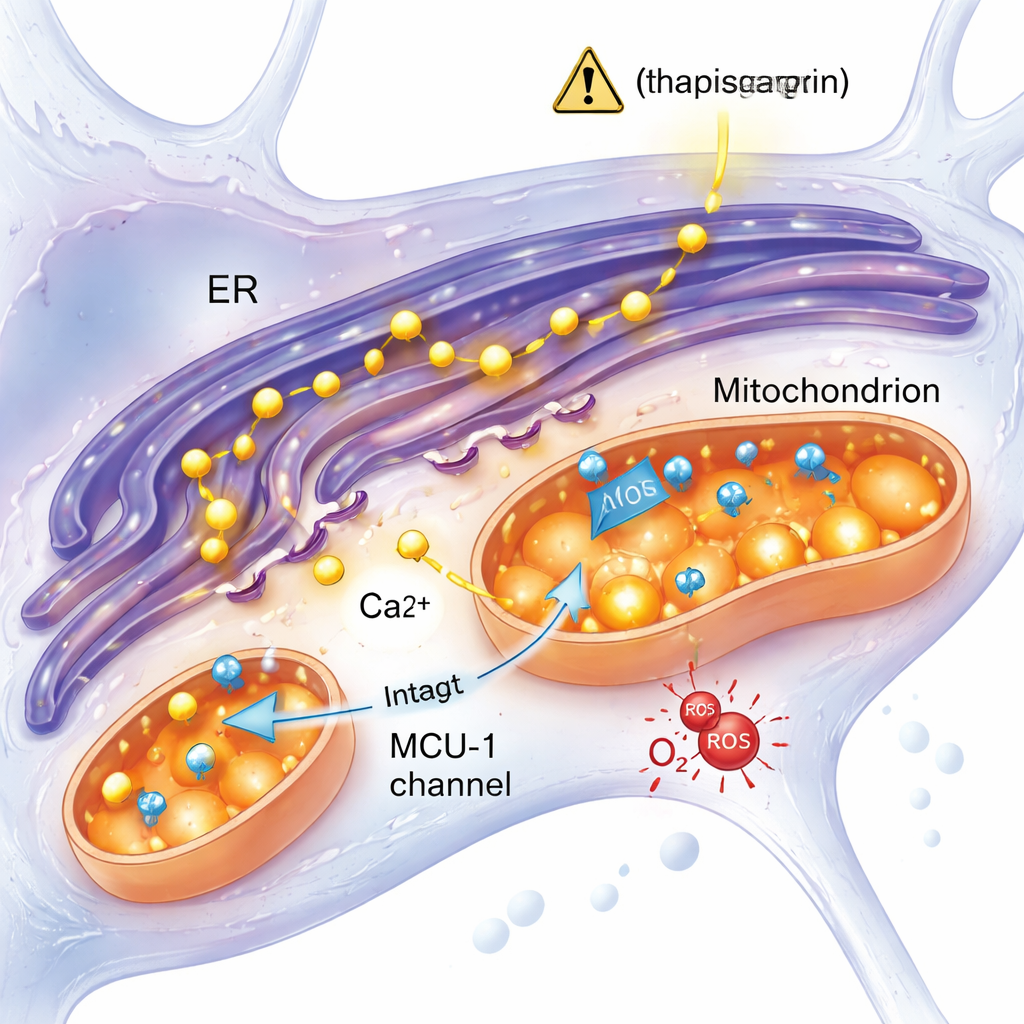
תגובה ללחץ שאינה תלויה בתעלת סידן מרכזית
רעיון מרכזי במחקר האלצהיימר הוא שסידן מיותר מהרשתית האנדופלסמית חודר למיטוכונדריה דרך תעלה הנקראת ה- mitochondrial calcium uniporter (MCU‑1), מעמיס עליהן ומניע ליקוי תפקודי. המחקר בחן רעיון זה ישירות. כאשר החוקרם חסמו את MCU‑1 בעזרת מעכב ספציפי, גם תאי הבקרה וגם התאים המוטנטיים הראו ירידה חדה בספיגת סידן מיטוכונדריאלית, מה שאישר שהתעלה עצמה פעילה בשתי הקבוצות. יתר על כן, כאשר שחרור הסידן הושרה דרך מסלול פיזיולוגי יותר שכלל את קולטן ה-IP3 — שער סידן מרכזי נוסף — התגובות של התאים המוטנטיים והבקרים היו דומות. תוצאות אלה מרמזות כי הבעיה אינה בתעלת MCU‑1 שבורה אלא יותר בקשרים הפיזיים והפונקציונליים בין הרשתית האנדופלסמית למיטוכונדריה, או בהיבטים אחרים של האינטראקציה ביניהן, ששונו בנוירונים המוטנטיים.
מה משמעות הממצאים להבנה ולטיפול
במכלול, הממצאים מציירים תמונה של נוירונים אנושיים נושאי המוטציה PS1 M146L של אלצהיימר כתאים הנראים נורמליים במנוחה אך מגיבים באופן חריג תחת לחץ. המיטוכונדריות שלהם אינן מצליחות לקלוט מספיק סידן כאשר מאגרים פנימיים משתחררים בבת אחת, ובכל זאת הן פועלות חזק יותר — צורכות יותר חמצן ומייצרות יותר מולקולות חמצון תגובתיות — כאילו תקועות במצב פיצוי יקר. מאחר שזה קורה בניורונים שמקורם באדם חי לפני הופעת תסמינים קליניים, העבודה תומכת ברעיון שהפרת איתות סידן ועומס מיטוכונדריאלי מוקדם הם אירועים המתרחשים לפני מחלת האלצהיימר ולא רק תוצר לוואי מאוחר. עבור קוראים שאינם מומחים, המסר המרכזי הוא ששמירה על האיזון בין אותות סידן לייצור אנרגיה מיטוכונדריאלית יכולה להיות חשובה ככל הידוע בטיפוח ושימור מוח תקין, לא פחות ממיקוד במשקעים האמילואידיים הידועים יותר.
ציטוט: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
מילות מפתח: מחלת אלצהיימר, מיטוכונדריה, אותות סידן, מוטציית פרסנילין-1, נוירונים שמקורם ב-iPSC