Clear Sky Science · he
SHP2 מקדם אוסטאוסרקומה דרך ויסות איתות STAT3/TET3/HOXB2
מדוע המחקר הזה על סרטן העצם חשוב
אוסטאוסרקומה היא סרטן העצם הראשוני השכיח ביותר בילדים ובמתבגרים, ובמרות כימותרפיה וניתוח מודרניים, הישרדות של חולים עם מחלה מפושטת או חוזרת כמעט שלא השתפרה בעשורים האחרונים. המחקר חוקר את החיבורים הפנימיים של תאי האוסטאוסרקומה כדי לזהות אילו מולקולות פועלות כ'מפסקי על' המסייעים לגידולים לצמוח, להתפשט ולעמוד בפני טיפולים. על ידי חשיפת מסלול בקרה מרכזי שמרכזו חלבון הנקרא SHP2, העבודה מצביעה על מטרות תרופתיות חדשות שיכולות יום אחד להפוך את הטיפולים ב אוסטאוסרקומה ליעילים ומדויקים יותר.
במעקב אחרי הרמזים בפעילות הגנים של הגידול
החוקרים התחילו בטיפול באוסטאוסרקומה כבעיית נתונים. הם כרו מאגרי ביטוי גנים ציבוריים השווים דגימות גידול לרקמת עצם נורמלית, ואז השתמשו בכלים סטטיסטיים כדי לזהות גנים שהודלקו או השתקו בעקביות בסרטן. מאות גנים היו שונים, ורבים מהם התקבצו במסלולי סרטן ידועים שמניעים גדילה, הישרדות ותנועה של תאים. בין אלה, חלבון אחד, SHP2, בלט כצומת שמקושר בחוזקה לכמה אחרים: גורם האיתות STAT3, האנזים המשנה-DNA TET3, והבקר ההתפתחותי HOXB2. הדבר הצביע על כך שמולקולות אלה עשויות להוות שרשרת מחוברת המסייעת לתאי אוסטאוסרקומה להתנהג באגרסיביות. 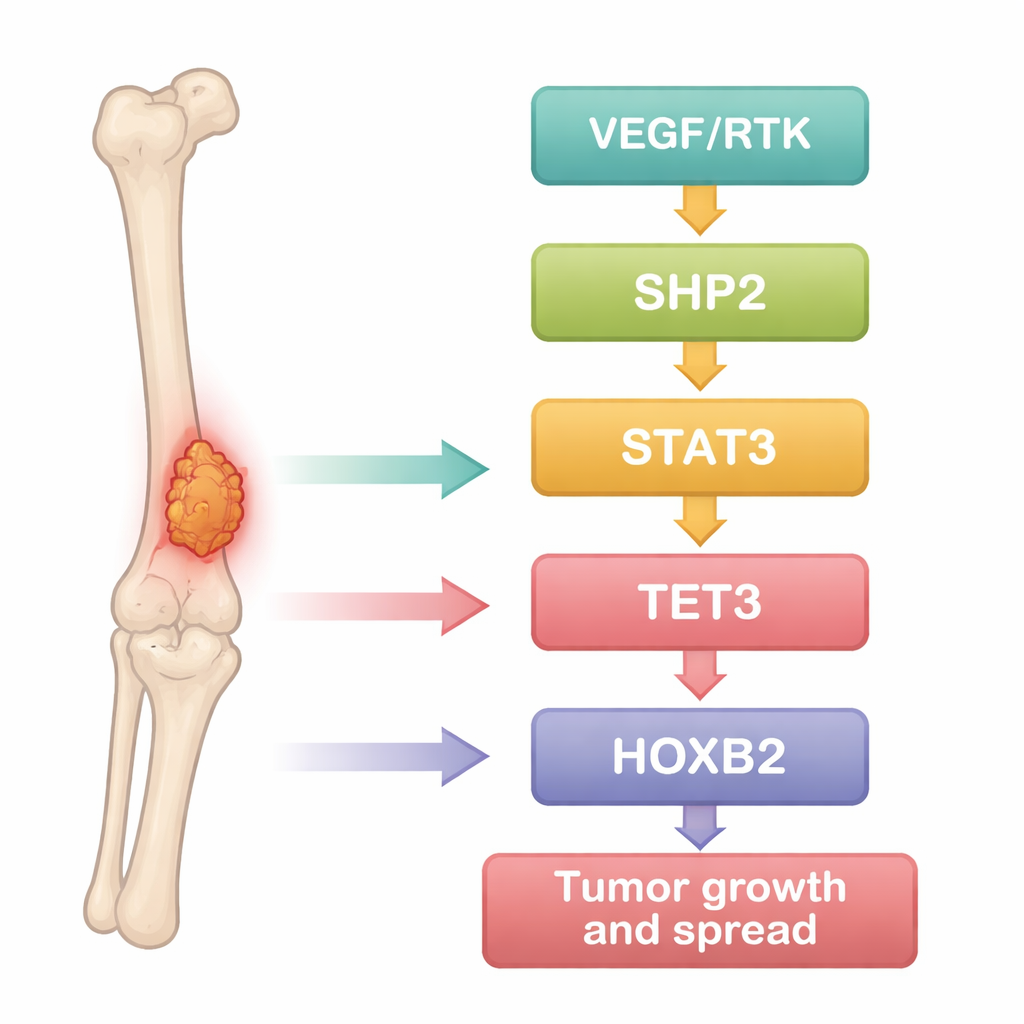
בדיקת תפקידו של SHP2 בתאי הסרטן
כדי לצאת מעבר לקורלציות, הצוות מהנדס קווי תאי אוסטאוסרקומה אנושיים (143B ו-MG63) לשם הקטנה או הגברה של SHP2. כשהורידו את SHP2, יכולת התאים להתחלק, להיגרר על משטח ולחדור דרך ממברנה ירדה באופן ניכר. גם רמות החלבונים STAT3, TET3 ו-HOXB2, וכן סמנים המקושרים לסרטן כמו c-Myc, NANOG ו-NUSAP1, ירדו. כאשר הפעילו מחדש את STAT3 או הביטו מעבר ל-HOXB2, רבים מהאפקטים האלה הופרו, מה שמעיד ש-SHP2 נמצא במעלה שרשרת שסופו משפיע על גנים השולטים בחלוקת תאים, בתכונות דמויות-תא גזע ובמכונות החלוקה התאית.
בניית מסלול סרטן של שלב אחר שלב
בהרכבת הניסויים, המחברים מתארים מודל של צעדים. בסביבת הגידול, רמות גבוהות של גורם גדילה אנדותלי וסקולרי (VEGF) מעוררות טירוזין קינאזות-מקבל (RTKs) על פני התא. אלה, בתורם, מפעילים את SHP2 בתוך התא. SHP2 פעיל מדליק את STAT3, פקטור שכפול שנעה אל הגרעין ועוזר להגדיל את ייצור TET3. לאחר מכן TET3 עורך את התגים הכימיים על ה-DNA, בהסרת קבוצות מתיל מאזור גן HOXB2. דה-מתילציה זו פועלת כמו הסרת מעצור, ומאפשרת ביטוי מוגבר של HOXB2. HOXB2, גן שמדריך בדרך כלל התפתחות, מעודד כעת את הפעילות של c-Myc, NANOG ו-NUSAP1, שלצדם מזינים צמיחה בלתי פוסקת של תאי גידול, משפרים יכולת פולשנות ותומכים בתכונות המקושרות למטסטאזות.
מצלחת פטרי אל בעלי חיים חיים
כדי לבדוק האם המסלול הזה משפיע גם בגידולים שלמים, המדענים השתילו תאי אוסטאוסרקומה מותאמים מתחת לעור של עכברים. גידולים שנוצרו מתאים המייצרים מדי SHP2 גדלו והיו כבדים יותר בהשוואה לגידולים ביקורתיים. כשהשתקו את TET3 בתאים עשירי SHP2 אלה, קצב הגידול האט ורמות HOXB2 פחתו, אף על פי ש-SHP2 ו-STAT3 נותרו פעילים. החזרת HOXB2 החזירה את החיות של הגידול. לאורך כל הדרך, מדידות רמות החלבון ברקמת הגידול השתקפו בממצאי תרבית התאים המוקדמים, וחיזקו את הרעיון ש-SHP2, STAT3, TET3 ו-HOXB2 פועלים כאקסיס מחובר שמניע את האוסטאוסרקומה להתנהגות ממאירה יותר. 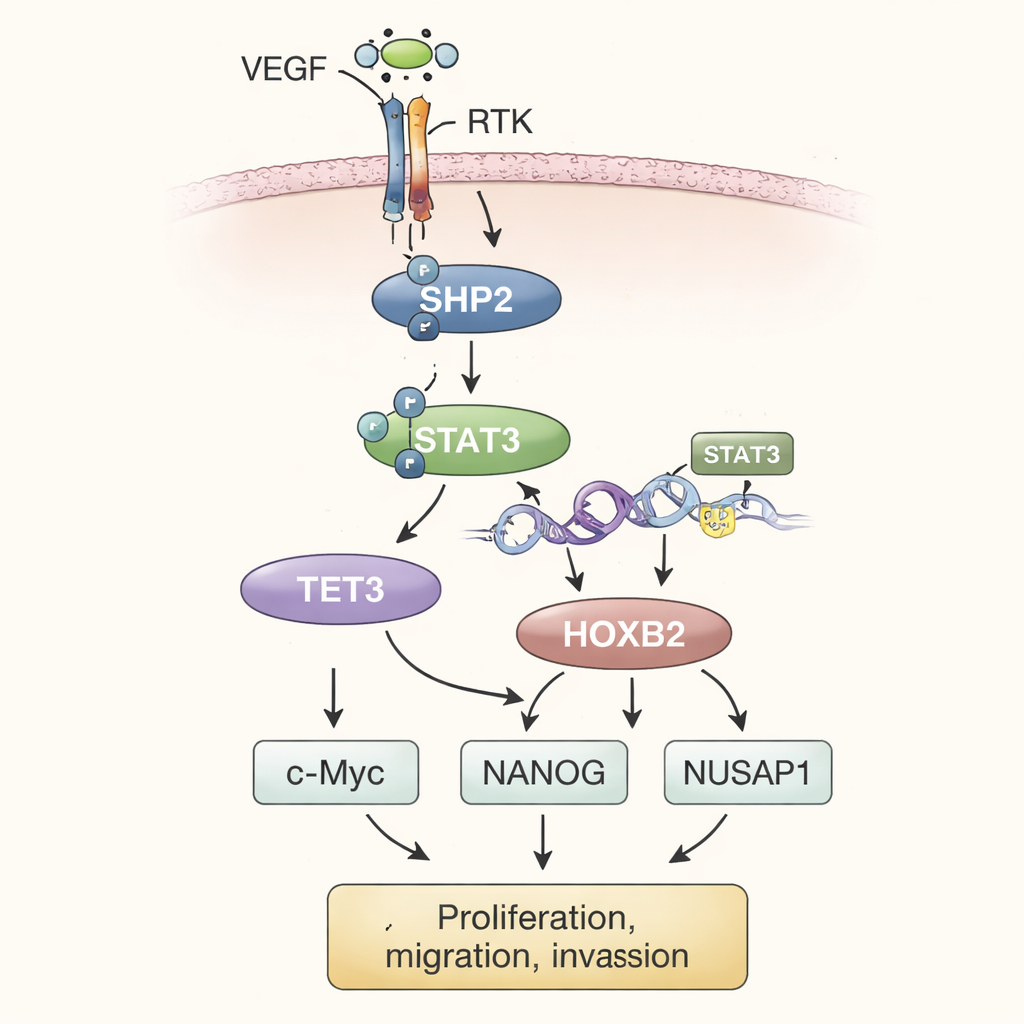
ממה זה משמעותי לטיפולים עתידיים
לקורא שאינו מומחה, המסר הוא שהחוקרים ציירו שרשרת איתות ברורה — מ-VEGF וקולטניו על המשטח, דרך SHP2 ו-STAT3, ועד TET3, HOXB2 וכמה גני צמיחה משמעותיים — שמסבירה מדוע אוסטאוסרקומה יכולה לגדול במהירות ולהתפשט מוקדם. מאחר ש-SHP2 ו-STAT3 הם אנזימים שניתן, בעקרון, לעכב באמצעות תרופות מולקולריות קטנות, ו-TET3 ו-HOXB2 מציינים שלבים מאוחרים במסלול זה, המסלול מציע מספר נקודות שבהן טיפולים עתידיים יוכלו להתערב. למרות שהמחקר בוצע בקווי תאים ובעכברים, הוא מספק מפה מפורטת שמפתחי תרופות יכולים להשתמש בה כדי לעצב טיפולים משולבים שמטרתם לכבות את מפסקי השליטה המרכזיים של הגידול במקום להסתפק בתקיפת התוצאות הסופיות שלו.
ציטוט: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
מילות מפתח: אוסטאוסרקומה, SHP2, מסלול STAT3, איתות גידולי, טיפול ממוקד