Clear Sky Science · he
המאגרים המיוסדים על חלקיק ההכרה לאיתות בבני אדם
איך התאים מחליטים אילו חלבונים עוזבים את התא
התאים שלנו שולחים באופן קבוע חלבונים שמרכיבים הורמונים, נוגדנים ומערכי תשתית בין רקמות. אך לא כל חלבון מיועד לנוע החוצה. המחקר הזה בוחן שאלה בסיסית שבינתיים לא נענתה: איך תאים אנושיים מחליטים אילו חלבונים זקוקים לעזר מרכזי הנקרא חלקיק ההכרה לאיתות (SRP) כדי להגיע למרכז השילוח התאי, ואילו יכולים להגיע לשם בלעדיו? על‑ידי מיפוי ההחלטה הזו על פני אלפי חלבונים בבת אחת, המחברים חושפים מי תלוי ב‑SRP, מי לא, ומה קורה כשהמערכת הזו משתבשת — נושא שרלוונטי למחלות רבות שקשורות לטעויות במסלול ההפרשה או לחלבונים מופרשים חסרים.
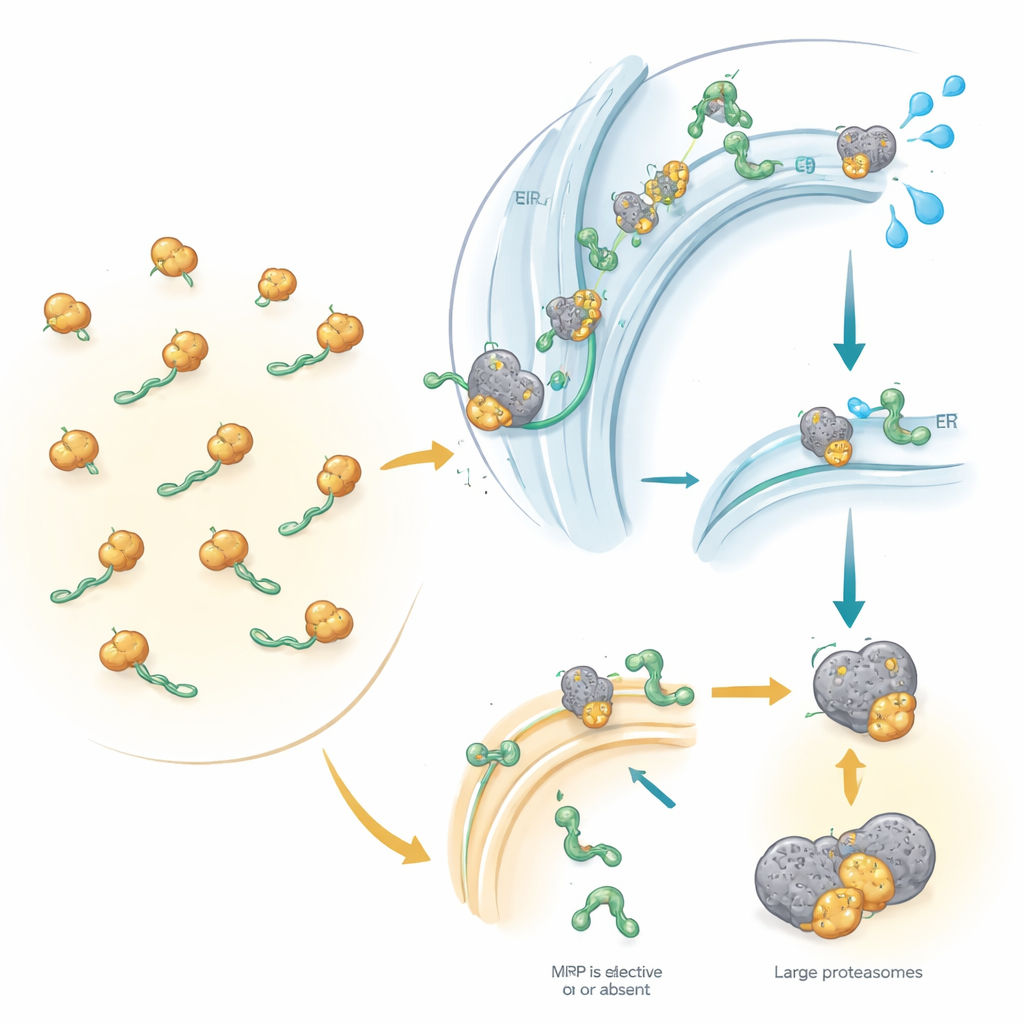
מזח השילוח של התא והמדריך העיקרי שלו
בערך אחד מכל שלושה חלבונים אנושיים מיועד לממש את פני התא, לממברנות התאית או לשחרור מחוץ לתא. כדי להגיע ליעד הנכון, רוב החלבונים הללו חייבים תחילה להיכנס לרשת ממברנות פנימית שנקראת רשתית אנדופלזמטית, מזח השילוח של התא. ה‑SRP משמש כמדריך: הוא מזהה "תג כתובת" קטן בהתחלה של חלבונים חדשים ועוצרת זמנית את יצירתם. עצירה זו נותנת להריבוזום — מכונת ייצור החלבון — זמן לעגון ברשתית האנדופלזמטית, שם הייצור ממשיך והחלבון המתרכז מוכנס לתוך הממברנה או דרך הממברנה. עם זאת, ידועים חלבונים שמשתמשים במסלולים חלופיים שאינם דורשים SRP, במיוחד חלבונים קטנים מאוד או כאלה המעוגנים בקצה הזנב שלהם. עד כה לא היה ברור, בקנה מידה גלובלי, אילו חלבונים אנושיים באמת זקוקים ל‑SRP ואילו יכולים לעקוף אותו.
כיבוי חלקי של SRP כדי לראות מה נשבר
כדי להשיב על השאלה הזו, החוקרים הפחיתו באופן סלקטיבי את רמות אחד מרכיבי ה‑SRP החיוניים, SRP54, בתאי הילה אנושיים. לאחר מכן השתמשו בטכניקה רגישה הנקראת ספקטרומטריית מסה כדי למדוד מעל 6,000 חלבונים בתוך התאים וכמעט 2,000 חלבונים בנוזל הסובב, הידוע כמדיה מותנית. השוואת תאים עם רמות תקינות של SRP54 לאלה שבהן SRP54 נדחס אפשרה לראות אילו חלבונים הפכו לפחות שכיחים, אילו עלו ואילו לא השתנו. ירידה חדה ברמת חלבון — בייחוד הן בתוך התא והן במדיה — נחשבה סימן לכך שחלבון זה תלוי ב‑SRP כדי להיות מיוצר וממופה כהלכה.
מי תלוי ב‑SRP ומי מסתדר בלעדיו
הניתוח הראה שרוב החלבונים שבדרך כלל מופרשים למדיה תלויים בבירור ב‑SRP. כאשר SRP54 הופחת, רוב החלבונים המופרשים הללו, במיוחד אלה הנושאים תג כתובת קלאסי, צנחו באופן חד. גם חלבוני ממברנה רבים בתוך התא ירדו, מה שהצביע על כך שהם לקוחות של SRP. קבוצה קטנה יותר של חלבונים עם תגי כתובת דומים לא הושפעה במידה רבה, וסומנה כבלתי תלויה ב‑SRP; סביר שהם משתמשים במסלולים חלופיים כדי להגיע לרשתית האנדופלזמטית. החוקרים גם גילו שתכונות מסוימות של תג הכתובת — כגון אזור בעל מטען חיובי בתחילתו — היו שכיחות יותר בקרב חלבונים תלויי SRP, מה שמרמז על כללים עדינים שעוזרים ל‑SRP לבחור את המטען שלו. במקביל, כמה חלבונים המעורבים בסימון חלבונים פגומים להשמדה ובתפקוד המיטוכונדריה עלו ברמותיהם, מה שמרמז שהתאים מפעילים מערכות גיבוי וייצור אנרגיה כשהמדריך הראשי שלהם לשילוח נפגע.
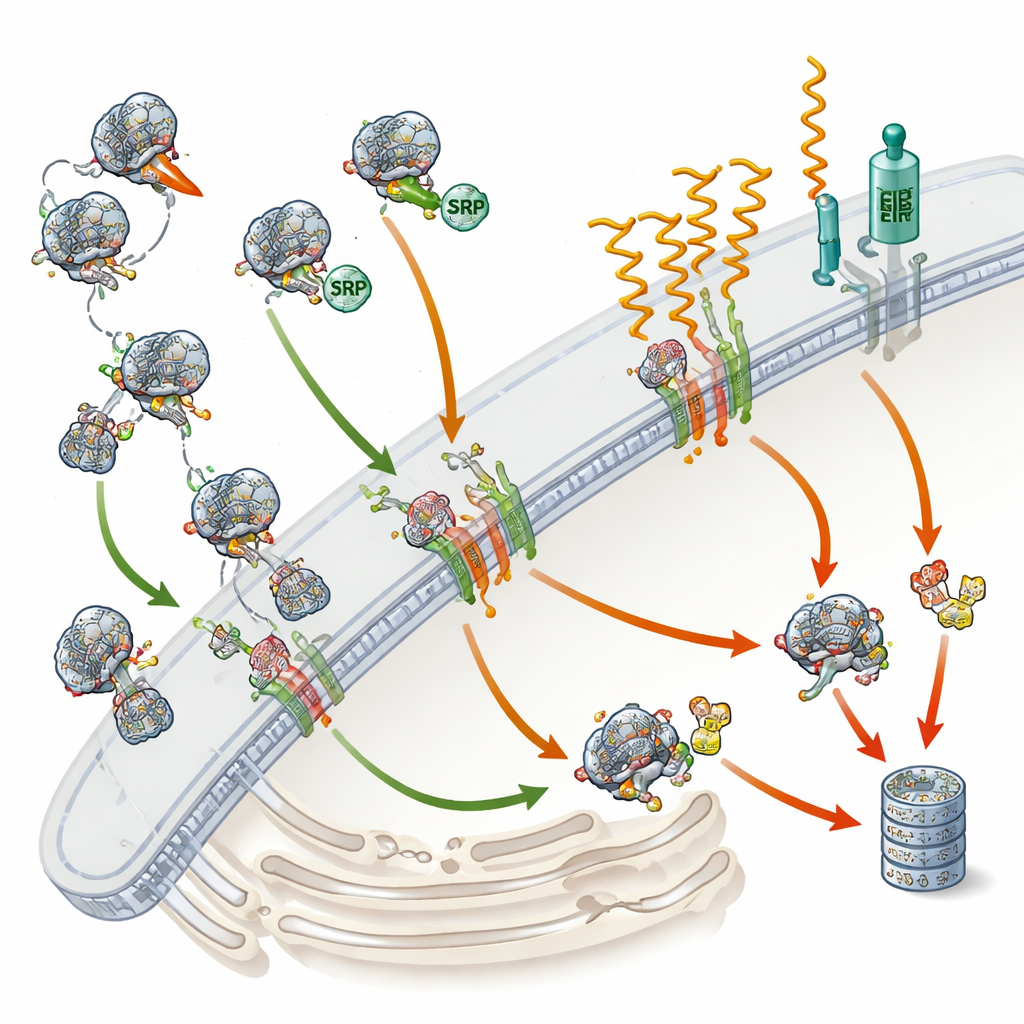
בקרת איכות כשמכוונים לא נכון
המחקר חרג מעבר לספירת חלבונים: הוא השווה את השינויים האלה להזזות בכמויות ה‑mRNA, התוכניות המשמשות לייצור חלבונים. רבים מהחלבונים התלויים ב‑SRP איבדו לא רק את החלבון אלא גם את התבניות ה‑RNA שלהם, מה שמצביע על מסלול בקרת איכות הידוע בשם RAPP. כאשר SRP אינו מצליח להיקשר כראוי לחלבון סקרטורי או ממברנתי בתהליך ההיווצרות, נראה כי מסלול זה מפעיל פירוק של ה‑RNA המתאים, ומונע המשך ייצור של חלבון שייפנה בדרך שגויה. במקביל, חלבונים שלא הושלמו ונכשלו להגיע לרשתית האנדופלזמטית מסומנים כהסתברות בדגלים מולקולריים קטנים ומועברים ל"מגרסות" התא שנקראות פרוטאוזומים. באופן מעניין, מסלולי מתח קלאסיים ברשתית האנדופלזמטית לא הופעלו בעוצמה רבה, מה שמרמז כי כשל ב‑SRP מעורר סוג שונה של תגובת לחץ תאית.
מה משמעות הדבר עבור בריאות ומחלה
על ידי מיפוי, לראשונה בתאים אנושיים, אילו חלבונים מופרשים וממברנליים תלויים ב‑SRP ואילו בלתי תלויים, עבודה זו מספקת מפת ייחוס של כללי השילוח התאים. הממצאים מראים שרוב החלבונים המיוצאים באמת תלויים ב‑SRP וכי כאשר SRP מתקשה, התאים מגיבים על‑ידי פירוק הן את החלבונים והן את התבניות שלהם תוך הפעלת מנגנוני התמודדות חלופיים. מכיוון שרבים מהמוטציות הגורמות למחלות משפיעות על תגי ה"כתובת" של חלבונים מופרשים, הבנת האופן שבו SRP מזהה את לקוחותיו וכיצד RAPP מסלק טעונים פגומים עשויה לעזור להסביר מדוע מוטציות מסוימות גורמות לחוסרים הורמונליים, לבעיות חיסוניות או לנוירודגנרציה — ואולי בסופו של דבר להצביע על דרכים לכוון את מסלולי השילוח התאיים במסגרת הבריאות האנושית.
ציטוט: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
מילות מפתח: הפרשת חלבונים, חלקיק ההכרה לאיתות, סקרטום, בקרת איכות חלבונים, רשתית אנדופלזמטית