Clear Sky Science · he
עיכוב רצפי של פלטינה ו‑PARP משפר את היעילות של אימונו‑תרפיית PD1 בסרטן הלבלב BRCA2‑מוטנטי בעכברים
מדוע המחקר הזה חשוב למטופלים
סרטן הלבלב הוא אחד הסרטנים הקטלניים ביותר, ואף כאשר הרופאים מזהים פגיעות גנטית שיכולה לעזור — כמו מוטציה ב‑BRCA2 — הטיפולים הקיימים נדירים שמצליחים לשלוט במחלה לאורך זמן. המחקר הזה משתמש במודל עכבר ריאלי כדי לבדוק שאלה מעשית שרבים מהמטופלים והאונקולוגים נתקלים בה כיום: אחרי כימותרפיה חזקה ומעכב PARP, האם הוספת אימונו‑תרפיה מודרנית יכולה להאריך משמעותית את ההישרדות, ומדוע הגידולים לעתים קרובות חוזרים?
סרטן עקשן עם נקודת תורפה גנטית
אדנוקרצינומה של צינוריות הלבלב קשה מאוד לטיפול, עם הישרדות לחמש שנים שנשארת באחוזים בודדים. מקצת מהמטופלים נושאים ליקויים תורשתיים או ספציפיים לגידול ב‑BRCA2, גן הממלא תפקיד בתיקון שברי DNA. גידולים אלה רגישים באופן חריג לתרופות המזיקות ל‑DNA, כמו כימותרפיה מבוססת פלטינה, ולמעכבי PARP, שמחלישים עוד יותר את יכולת תאי הגידול לתקן DNA. הטיפול הסטנדרטי לחולי סרטן לבלב מתקדם עם מוטציות BRCA הוא חודשים של כימותרפיה מבוססת פלטינה ולאחר מכן טיפול תחזוקתי עם מעכב PARP. עם זאת, בניסוי הקליני המרכזי POLO, אסטרטגיה זו לא האריכה את ההישרדות הכוללת, מה שמדגיש את הצורך להבין את מנגנוני ההתנגדות ולעצב גישות תחזוקה טובות יותר.
בניית מודל עכבר ריאליסטי יותר
רבים מהמודלים במעבדה מפשירים או מסירים את מרכיבי המערכת החיסונית והתמיכה הרקמתית שמקיפים גידולים אמיתיים בחולים. כדי להתגבר על כך, החוקרים הנדסו עכברים שמפתחים גידולי לבלב חסרי BRCA2 בהקשר של מערכת חיסון מתפקדת לחלוטין. מהגידולים הספונטניים הללו הפיקו קווי תאים קלונליים שניתן היה להשתיל בעכברים גנטית תואמים. גידולי Brca2‑מוטנטי אלה נראו והתנהגו בדומה לסרטני לבלב אנושיים: הם היו צפופים ופיברוטיים, רוב הזמן מנעו חדירת תאי T, והראו רמות גבוהות של נזק DNA ספונטני. חשוב לציין שהגידולים היו רגישים מאוד לתרכובת פלטינה נפוצה (גמיציטאבין בתוספת ציספלטין), בעוד שטיפול במעכב PARP לבדו הניב אפקטים מתונים וקצרים בחיות, אף על פי שבאותם תאים בתרבית פעילותו הייתה חזקה. 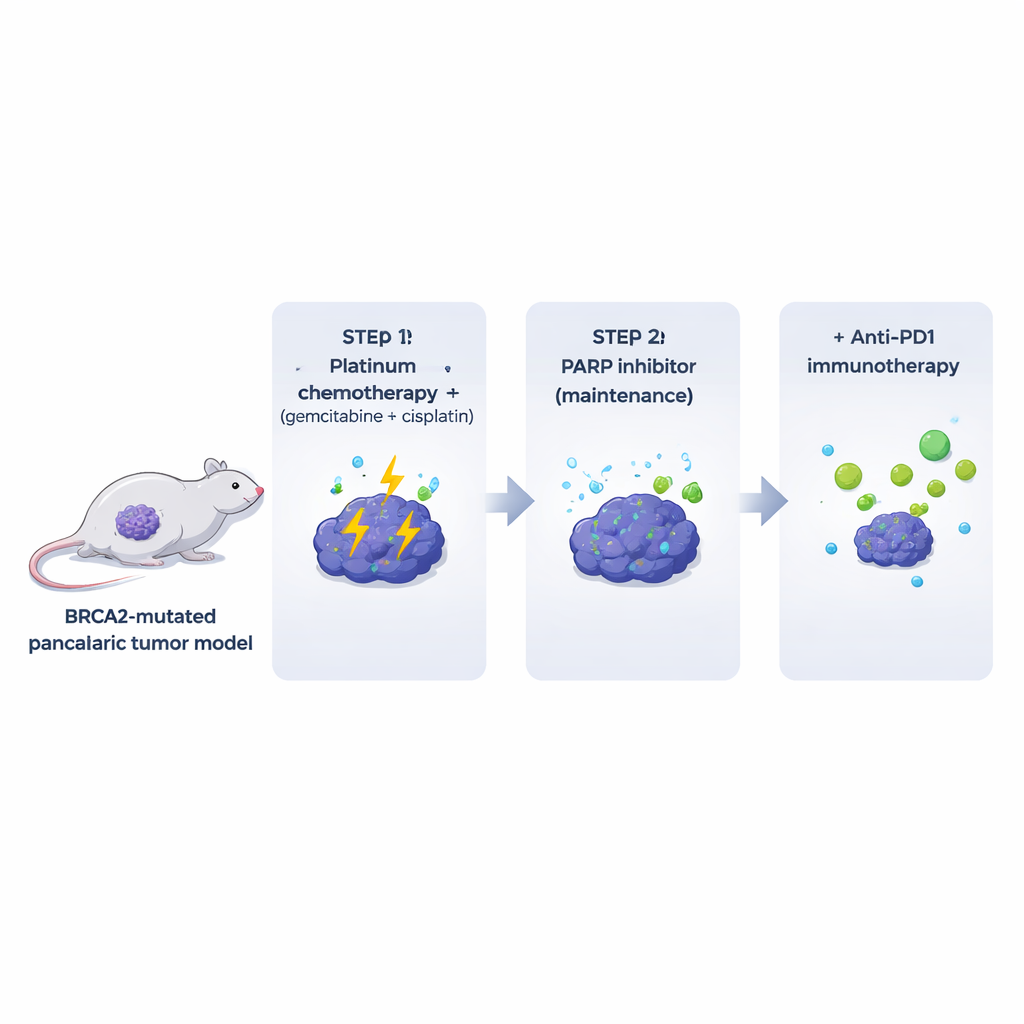
הכימותרפיה משנה את סביבת הגידול
הצוות חקר מה קורה בתוך הגידול לאחר כימותרפיה מבוססת פלטינה. עשרה ימים לאחר הטיפול, הגידולים הצטמצמו אך לא הושמדו. ניתוחי ביטוי גנים חשפו שינוי בולט לכיוון פעילות חיסונית: מסלולים הקשורים להפעלת תאי T ולחיסון אדפטיבי הופעלו. נמצאו יותר תאי T בתוך הגידולים המטופלים, ורבים מתאי ה‑T הללו נשאו סמנים של תשישות — סימן לכך שהופעלו אך נעשו פחות יעילים. דפוסים דומים של עלייה בנוכחות תאי T נצפו בסרטני לבלב אנושיים עם מוטציות ב‑BRCA או ב‑PALB2 לאחר שחולים קיבלו כימותרפיה מבוססת פלטינה לפני ניתוח. במקביל, תאי הגידול העלו רמות של PD‑L1, חלבון שטח שיכול לכבות תאי T באמצעות קשירה לקולטן PD‑1, רמז לכך שהגידולים מגינים על עצמם מפני הלחץ החיסוני החדש.
מדוע PARP לבדו אינו מספיק — ואיפה מתעוררת עמידות
בהדמיית טיפול שדומה לטיפול בחולים, החוקרים נתנו לעכברים קורס התחלתי של גמיציטאבין וציספלטין, ואחריו טיפול תחזוקתי במעכב PARP, אולפאריב. רצף זה שיפר את שליטת הגידול וההישרדות בהשוואה לכימותרפיה בלבד, ואישר כי כימותרפיה קודמת יכולה להפוך גידולים לרגישים יותר לעיכוב PARP. עם זאת, אף עכבר לא הוכרז מרפא: הגידולים בסופו של דבר צמחו מחדש תחת טיפול תחזוקתי ב‑PARP. גידולים עמידים הראו מראה יותר ממויין והעלאה חכמה ברמות של המווסת ההתפתחותי CDX2. זה מרמז שבמוקד המודל הזה, העמידות לא נובעת פשוט מתיקון הפגם המקורי בתיקון DNA, אלא עשויה לערב שינוי בזהות התאית של הגידול. CDX2 עלולה לשמש ביומרקר מוקדם להופעת עמידות בחולים.
שחרור הפוטנציאל של אימונו‑תרפיה באמצעות רצף נכון
תרופות חוסמות נקודות עצירה חיסוניות כמו נוגדנים נגד PD1 שינו את הטיפול במספר סוגי סרטן, אך סרטן הלבלב נותר ברובו בלתי רגיש. בהתאם לכך, נוגד‑PD1 (עם או בלי תרופה נוספת לחסימת נקודת עצירה, נוגד‑CTLA4) לא עזר כשניתן לגידולים BRCA2‑מוטנטיים שלא טופלו קודם, ולא תרם הרבה כשהתווסף פשוט לטיפול במעכב PARP. התמונה השתנתה כאשר השתמשו ברצף המלא: קודם כימותרפיה מבוססת פלטינה, ואז מעכב PARP בתוספת נוגד‑PD1 כטיפול תחזוקתי. בסידור זה, הגידולים הצטמצמו באופן עמוק יותר והעכברים חיו יותר מאשר בכימותרפיה עם PARP בלבד או נוגד‑PD1 לבדו. הוספת נוגד‑CTLA4 לתחזוקת PARP לא הניבה יתרונות דומים, מה שמרמז שסביבת הגידול שהוכנה על ידי הכימותרפיה נמצאת במצב שמתאים במיוחד להגיב לחסימת PD‑1. 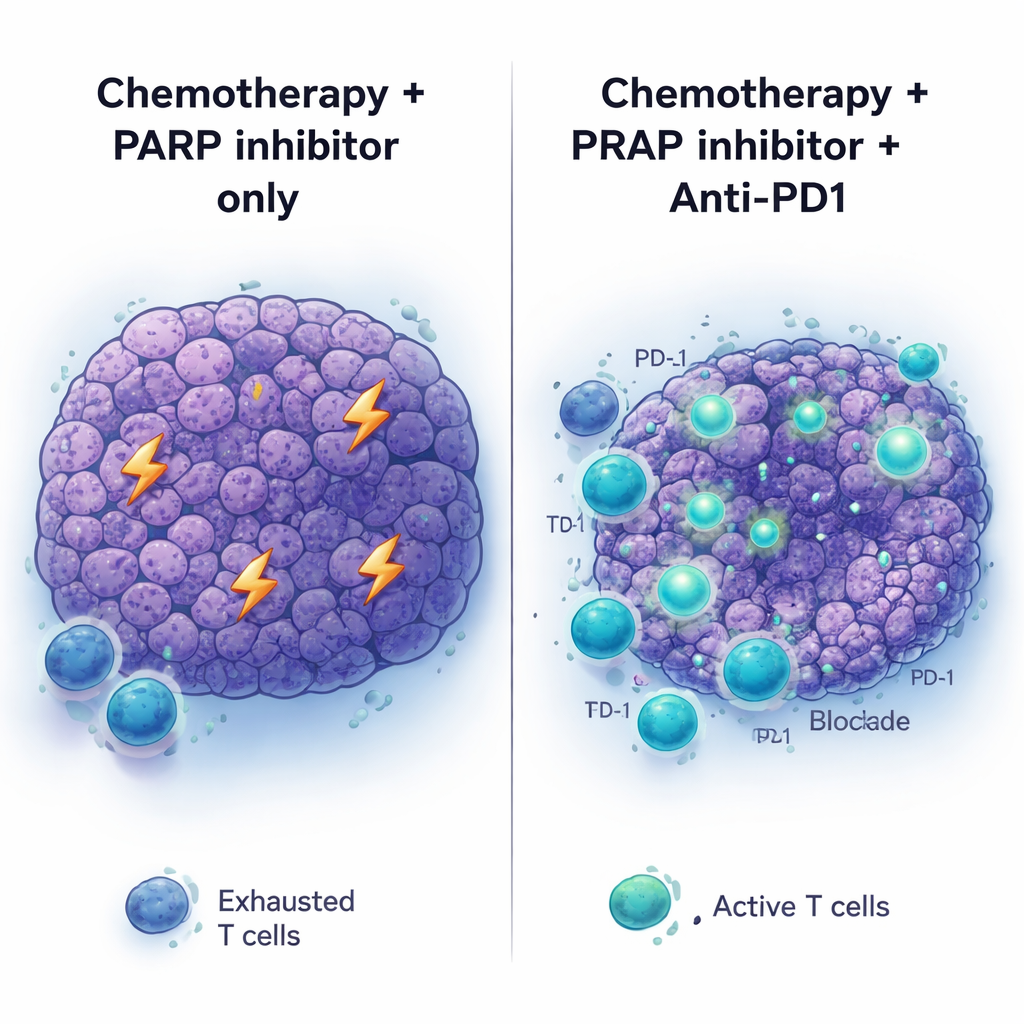
מה זה עשוי לשנות בטיפול עתידי
לסיכום, המחקר טוען כי בסרטן הלבלב עם מוטציית BRCA, הסדר והשילוב של הטיפולים משמעותיים מאוד. כימותרפיה חזקה הפוגעת ב‑DNA אינה רק תוקפת את תאי הגידול ישירות, אלא גם מעוררת תגובה חיסונית, אף אם תגובה זו מוחלשת בתחילה על‑ידי תשישות וסלידת PD‑L1. מעכבי PARP עשויים להאריך את התועלת אך צפויים לא לרפא לבדם ועלולים לדחוף גידולים למצב עמיד עם ביטוי גבוה של CDX2. על ידי הוספת אימונו‑תרפיית נגד PD‑1 לתחזוקת PARP לאחר כימותרפיה מבוססת פלטינה, עשוי להיות ניתן להפוך את הנוף החיסוני המדולל והמתיש הזה להתקפה אנטי‑גידולית חזקה ועמידה יותר. ניסויים קליניים מתמשכים שמשלבים מעכבי PARP עם אימונו‑תרפיה בסרטן לבלב הקשור ל‑BRCA יהיו מכריעים כדי לבדוק האם אסטרטגיה מתוזמנת זו יכולה לתרגם להארכות חיים טובות יותר ואיכות חיים מטופלים.
ציטוט: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
מילות מפתח: סרטן הלבלב, מוטציה ב‑BRCA2, כימותרפיה מבוססת פלטינה, מעכב PARP, אימונו‑תרפיית PD‑1