Clear Sky Science · he
שיבוש הומאוסטזת הברזל התאית דרך תפקוד מיטוכונדריאלי לקוי המקושר לדיכוי ביטוי ATP13A2
מדוע ברזל בתוך תאי המוח חשוב
מחלת פרקינסון ידועה בעיקר ברעד ותנועות נוקשות, אך עמוק בתוך התאים הנוירונים הנפגעים מתרחש דרמה אחרת: ברזל, מתכת חיונית, מתחיל להצטבר במקום שבו אין לו להיות. המחקר הזה שואל שאלה פשוטה אך מהותית: כיצד מתרחשת הצטברות הברזל הזו, וכיצד היא עלולה לפגוע בכוריות הכוח והמרכזים למיחזור בתא? בעזרת מענה לשאלה זו, העבודה מספקת רמזים מדוע אזורים מסוימים במוח מתנוונים בפרקינסון והפרעות דומות, ומצביעה על כיווני טיפול חדשים שמעבר להחלפת דופמין.
מבט מקרוב על רמז גנטי נדיר
החוקרים מתמקדים בצורה תורשתית נדירה של פרקינסון, הנקראת PARK9, הנגרמת על ידי פגמים בגן בשם ATP13A2. גן זה מקודד חלבון הממוקם בליזוזומים, מחלקות העיבוד והמיחזור של התא. אנשים עם מוטציות ב‑ATP13A2 עלולים גם לפתח מצב המתאפיין בהשקעות ברזל במוח. הקישור הזה הפך את ATP13A2 לנקודת כניסה אידיאלית לחקור כיצד מאזן הברזל נפרץ. באמצעות שורת תאים דמוית נוירון אנושית המייצרת בשפע את החלבון אלפא‑סינוקלאין הקשור לפרקינסון, הקבוצה השתמשה בקטעי RNA קטנים כדי להפחית את ביטוי ATP13A2 ואז עקבה אחר השינויים בברזל, בייצור האנרגיה ובבריאות התא.
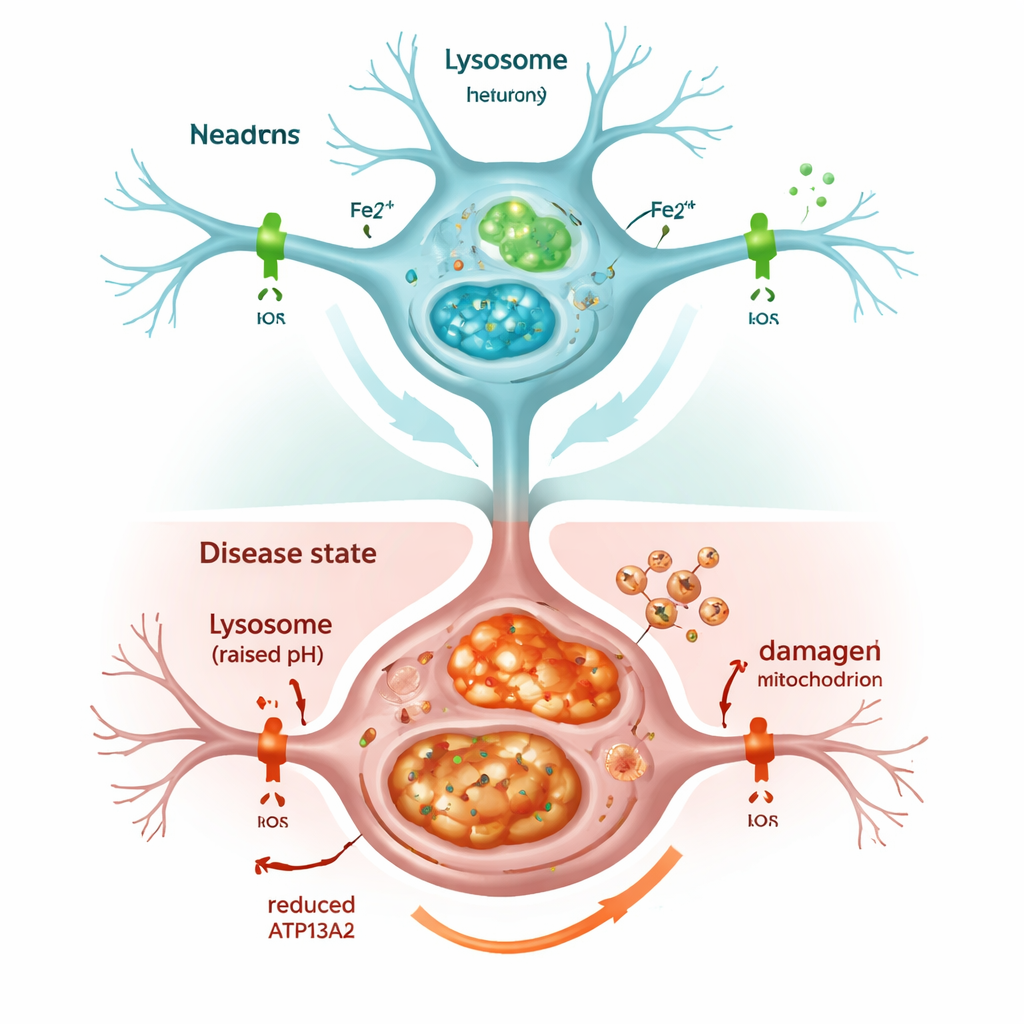
כאשר מערכת המיחזור התאית נתקעת
כיבוי ATP13A2 החליש במהרה את הליזוזומים. החומציות הפנימית שלהם, החיונית לפירוק חומר בלתי רצוי, ירדה, וסמנים של תהליך הניקוי התאי, האוטופאגיה, הצטברו במקום להימחק. כתוצאה מכך, אלפא‑סינוקלאין הצטבר, בחוזר למה שנצפה במוחות חולי פרקינסון. התאים גם הפגינו עלייה בכמות הברזל הכוללת, ובמיוחד בגירסה הפעילה מבחינה כימית, הנקראת Fe2+, בתוך הליזוזומים והמיטוכונדריות. התא הגיב על ידי ייצור מוגבר של פריטין, חלבון האוגר ברזל, אך זה לא הספיק למנוע נזק: המיטוכונדריות העמוסות ייצרו מולקולות חמצון ריאקטיביות מופרזות, והישרדות התאים ירדה. טיפול בתאים בתרופה הקושרת ברזל, בדומה לחלק מהתרופות הקליניות, הקטין את הלחץ החמצוני והציל חלקית את בריאות התאים, מה שמדגיש כי עודפי הברזל עצמם היו גורם מרכזי לנזק.
חיישני הברזל מפסיקים 'להקשיב' למתכת
באופן רגיל, לתאים יש מערכת משוב שמזהה עלייה ברמות הברזל ומגיבה על‑ידי הפחתת היבוא של ברזל. חלבון בשם IRP2 חושש (חוש) ברזל בין השאר דרך אות התלויHEME שמקורו במיטוכונדריות, ואז מותאם את ייצור החלבונים הנושאים ברזל על פני שטח התא. בתאים חסרי ATP13A2, המנגנון הזה נכשל. הטרנספורטרים שמכניסים ברזל לתא נשארו ברמות גבוהות למרות שהברזל כבר היה מוגבר. רמות חלבון IRP2 כמעט שלא השתנו, והוספת ברזל חיצוני לא עוררה את הפירוק הרגיל שלו. הצוות עקב אחרי הכשל הזה עד למיטוכונדריות: מיטוכונדריות פגומות נשמו פחות ביעילות, הראו סימנים של בקרה איכותית לקויה (מיטופאגיה לקויה), ומהחשוב מכל—איבדו את היכולת לייצרHEME, המולקולה המכילה ברזל שעוזרת ל‑IRP2 לחוש את הברזל. בלי מספיקHEME, IRP2 לא קיבל את האות "יותר מדי ברזל" ואיפשר המשך זרימת ברזל לתוך התא.
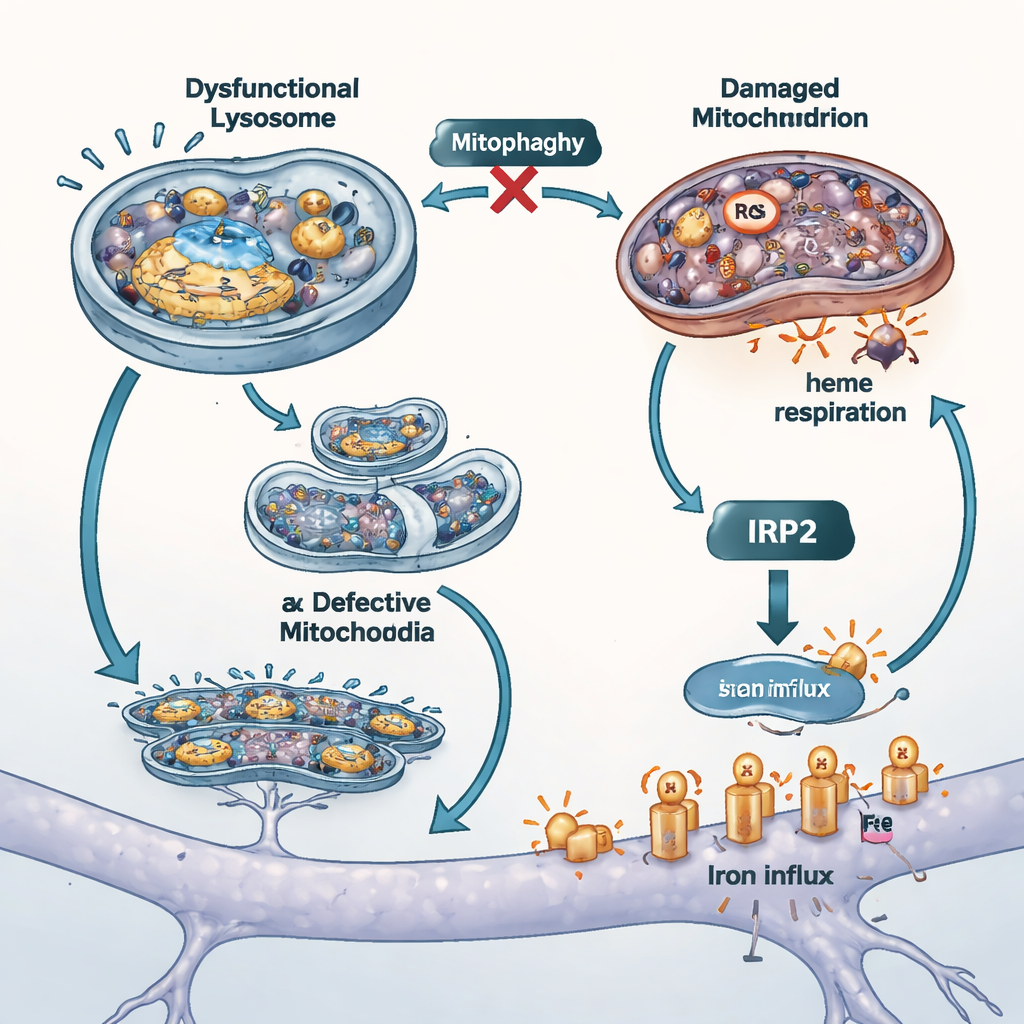
חסימת ברז הברזל ובחינת מודלים אחרים
כדי לבדוק עד כמה כניסת הברזל הבלתי מבוקרת תורמת לפגיעת התאים, המדענים חסמו שני מסלולי ייבוא הברזל העיקריים. הם השתמשו בגרסה נטולת ברזל של חלבון הדם טרנספרין כדי להתחרות על מפעיל כניסה אחד, ובתרופה קטנה כדי להנמיך את פעילותו של טרנספורטור נוסף בשם DMT1. שני המהלכים הורידו את הברזל הכולל והחופשי בתוך התאים, צמצמו את הלחץ החמצוני במיטוכונדריות ושיפרו את הישרדות התאים, מה שמרמז כי תעלות הברזל על הממברנה החיצונית מהוות מוגברים חשובים של הנזק כאשר ATP13A2 חסר. החוקרים חזרו גם על ניסויים מרכזיים בתאים החסרים גן אחר המקושר לפרקינסון, PINK1, הידוע כמפגע במיטופאגיה. תאים אלה הראו את אותה שילוב של הצטברות ברזל והיחלשות ייצורHEME, ותמכו ברעיון שבקרת איכות מיטוכונדריאלית ומאזן ברזל משולבים זה בזה בצורות שונות של המחלה.
מסקנות לפרקינסון ולטיפולים עתידיים
פשוטו כמשמעו, המחקר מתאר מעגל מלחיץ. כאשר ATP13A2 מדוכא, הליזוזומים נכשלו בניקוי רכיבים פגומים, כולל מיטוכונדריות לקויות. מיטוכונדריות מוחלשות אלה ייצרו פחות אנרגיה ופחותHEME, מה שהחליש את מערכת חישת הברזל של התא. ברזל המשיך לזרום דרך הטרנספורטרים החיצוניים, הצטבר במחלקות פגיעות והזין תגובות רעילות שפגעו עוד יותר במיטוכונדריות. עם הזמן, הלולאה הזו עשויה להסביר מדוע נוירונים מסוימים מתים בפרקינסון ובהפרעות מוחיות מלוות בהעמסת ברזל. הממצאים מצביעים כי טיפולים עתידיים עשויים לא רק לנסות להסיר עודף ברזל, אלא גם לשקם את תפקוד הליזוזומים, את בקרת האיכות המיטוכונדריאלית ואת ייצורHEME—לתקוף את הבעיה במקורה במקום רק לנקות את המתכת לאחר מעשה.
ציטוט: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
מילות מפתח: מחלת פרקינסון, ברזל במוח, מיטוכונדריות, ליזוזומים, סינתזת המוֹלֶקולהHEME