Clear Sky Science · he
דפוסים מודעים לחלל עבור נתוני אימונופלואורסצנציה מרובת אותות
למה השכונה של תאי הגידול חשובה
סרטן הלבלב הוא אחד מסוגי הסרטן הקטלניים ביותר, בין היתר כי הגידולים שלו חיים בתוך "שכונה" מורכבת של תאי חיסון ותמיכה שיכולים להילחם בסרטן או לסייע לו להסתתר. המחקר הזה מציג שיטה חדשה לקריאה של הפריסה המרחבית של תאים אלה בתמונות מיקרוסקופיות, וחושף כיצד התנהגות מערכת החיסון שונה במטסטזות דרמטיות של אדנוקרצינומה צינורית של הלבלב (PDAC) לעומת השכנה הקדם-סרטנית שלה, נגע פפילרי תוך-צינורי מייצר מוקוס (IPMN). הבנת דפוסים חבויים אלה עשויה להצביע על אבחנות טובות יותר וטיפולים ממוקדים וחכמים יותר.
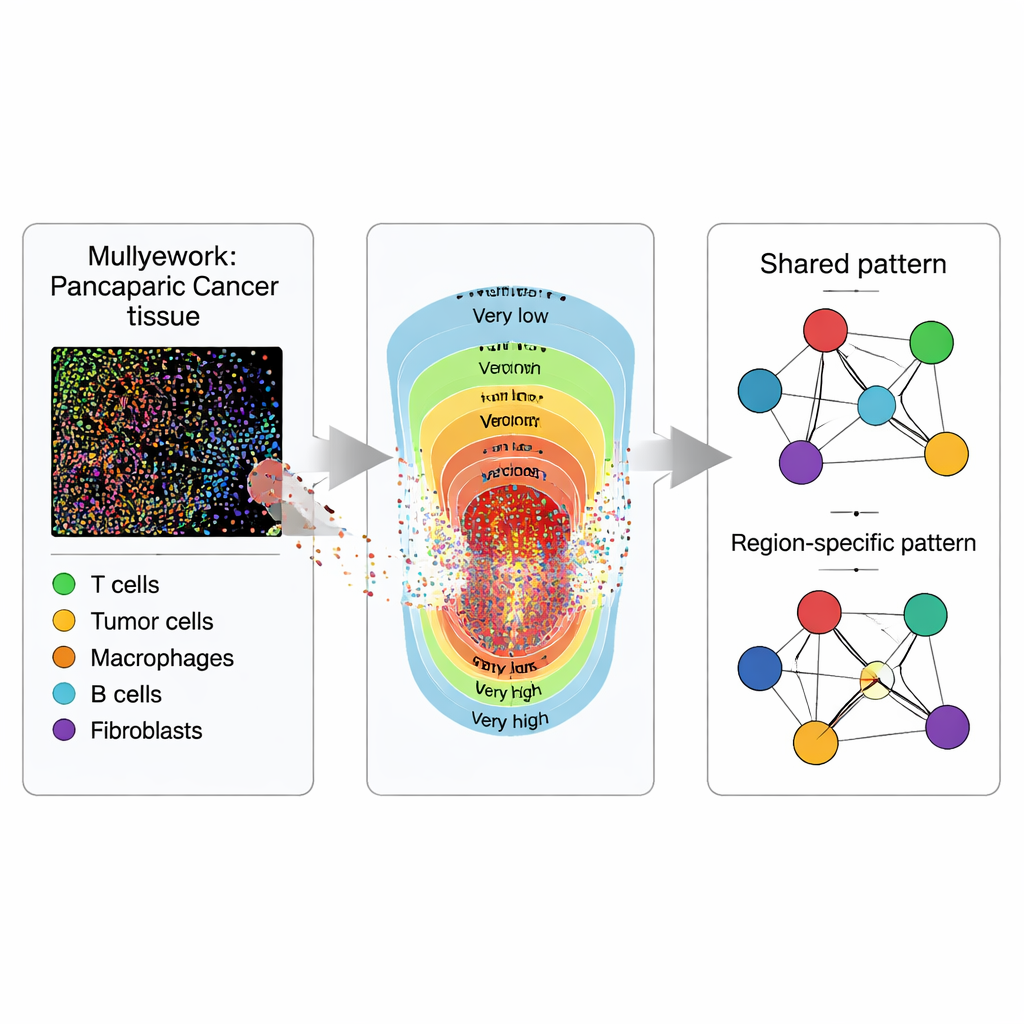
להביט ברקמות כמפות, לא רק כתמונות
במקום להתייחס לפרוסת הגידול כתמונה שטוחה, החוקרים מתייחסים אליה כמפה מלאה נקודות. באמצעות הדמיית אימונופלואורסצנציה מרובת אותות הם צובעים דגימות רקמה מ-119 חולי PDAC ו-53 חולי IPMN כך שסוגי תאים שונים זוהרים בצבעים מובחנים. תוכנה מיוחדת ממירה כל תא נראה לנקודה עם קורדינטות ותווית: תאי גידול (אפיתליאליים), מספר סוגי תאי T שיכולים לתקוף או לווסת תגובות חיסוניות, ותאי מציגי אנטיגן המציגים שברי גידול לתאי T. השאלה המרכזית אינה רק כמה מכל סוג של תא קיימים, אלא היכן הם נמצאים יחסית זה לזה ברחבי הרקמה.
חלוקת הגידול לאזורים
כדי ללכוד כיצד הגידולים משתנים מהמרכז כלפי חוץ, כל דגימת רקמה מחולקת לחמישה אזורים על בסיס צפיפות תאי הגידול, מ"נמוכה מאוד" ועד "גבוהה מאוד" בעוצמת הגידול. אזורים אלה מייצגים גרדיאנט של עומס גידולי וצפיפות תאית שמפתחים לעתים קרובות רואים במיקרוסקופ אבל כמעט שלא כמותיים. בתוך כל אזור, הצוות מעריך "מפות עוצמה" מעוקלות לכל סוג תא, בעצם הופך נקודות מפוזרות למפות חום רציפות של מקומות שבהם כל סוג תא נוטה להצטבר. החלוקה הזו מאפשרת להם להשוות לא רק כיצד תאים מתקשרים באופן כללי, אלא כיצד אינטראקציות אלה משתנות מאזורי גידול דלילים לאזורי גידול צפופים.
הפיכת שכונות תאים לרשתות
בהמשך, החוקרים מתרגמים את הדפוסים המרחביים לרשתות, שבהן כל סוג תא הוא צומת וקישורים מייצגים עד כמה שני סוגי תאים נוטים להופיע יחד לאחר התחשבות בכל השאר. באמצעות מסגרת סטטיסטית בייסיאנית שהם מכנים ISPat (Informed Spatially aware Patterns), הם מפרידים תכונות שמשותפות לכל האזורים מאלו הייחודיות לכל אזור. ISPat יכולה גם לשלב ידע ביולוגי מקדים כשזמין, מה שעוזר לייצב הערכות בנתונים מורכבים. ניסויי סימולציה מראים ש-ISPat מסוגלת לשחזר דפוסים ידועים במהימנות ולעשות זאת הרבה יותר מהר משיטות מסורתיות, מה שהופך אותה לפרקטית במחקרים תמונתיים רחבי היקף.
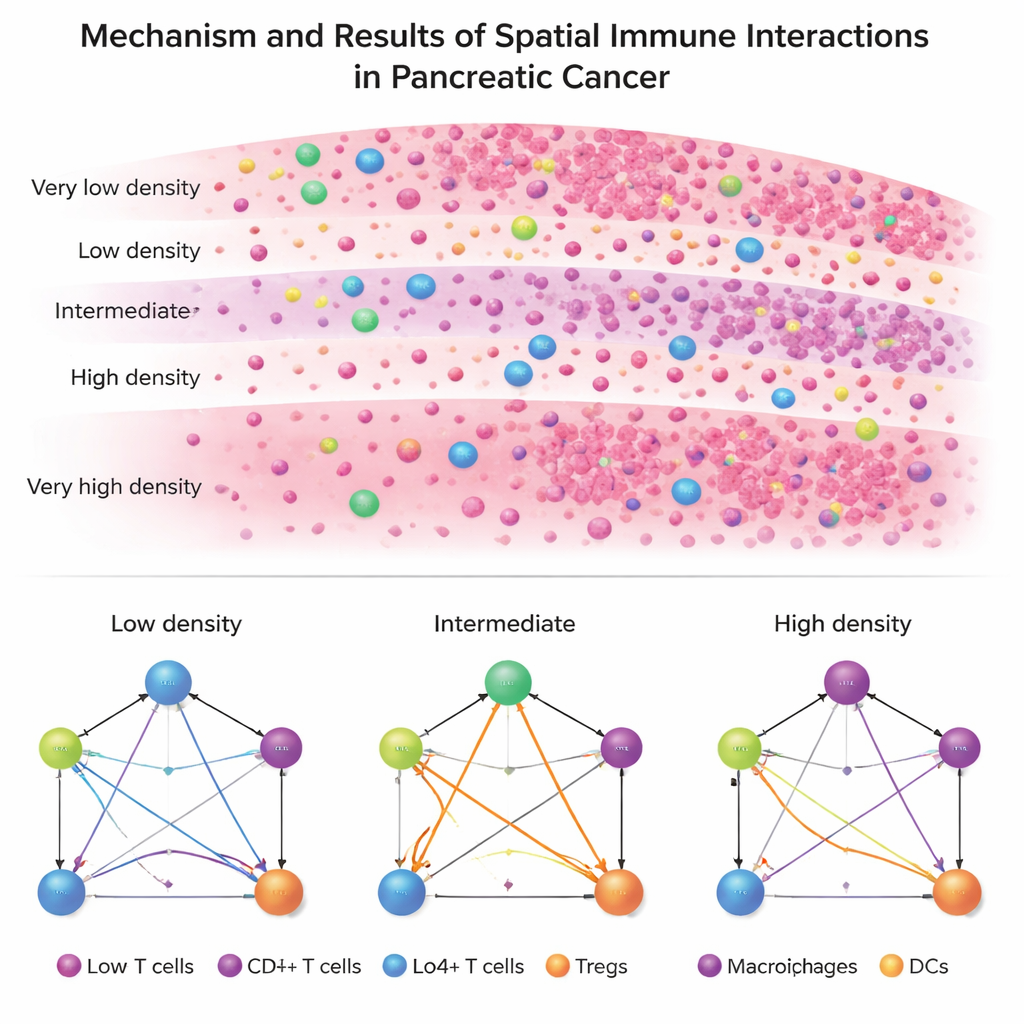
שתי מחלות, שתי ארכיטקטורות חיסוניות
כאשר הם מחילים את ISPat על נתוני מטופלים אמיתיים, עולה ניגוד בולט בין PDAC ל-IPMN. PDAC מציג ארכיטקטורה חיסונית נוקשה ואחידה: כמעט בכל האזורים, תאי הגידול, תאי T מסייעים, תאי T ציטוטוקסיים (קילר), תאי T רגולטוריים ותאי מציגי אנטיגן שומרים על דפוסי קשרים דומים. הדבר מרמז על סביבה מדכאת חיסונית יציבה ומושרשת שקשה לפרקה. לעומת זאת, ב-IPMN נצפית וריאציה רבה יותר מאזור לאזור, במיוחד באופן שבו תאי T רגולטוריים מתקשרים עם תאים חיסוניים אחרים. ב-IPMN, אזורי צפיפות בינונית—שלא צפופים לחלוטין בתאי גידול אך גם לא כמעט נקיים מהם—מראים את השינוי הדרמטי ביותר בעיצוב האינטראקציות החיסוניות.
נקודות חמות להימנעות מחיסון וטיפול
בהעמקה נוספת, המחקר מזהה זוגות ספציפיים של סוגי תאים שאינטראקציותיהם שונות בעקביות בין PDAC ל-IPMN, במיוחד באותם אזורי צפיפות בינונית. רבים מהם כוללים תאי T רגולטוריים, שיכולים לדכא את התקפות החיסון, ותאי מציגי אנטיגן ותאי קילר, שמניעים ומבצעים תגובות אנטי-גידוליות. באופן בולט, אינטראקציות שמניעות הצגת אנטיגן והרג ישיר של תאים, וכן אלו שמחזקות דיכוי חיסוני, נבדלות בצורה החדה ביותר באזורים אלה באמצע הגרדיאנט, לא באזורי הגידול הקיצוניים ביותר. תבנית זו מרמזת כי שדה הקרב המרכזי לשליטה חיסונית נמצא באזורים מעבריים שבהם הגידול ומערכת החיסון עדיין מנהלים משא ומתן פעיל.
מה זה אומר עבור מטופלים
לא-מומחה יכול להסיק שהמיקום שבו תאים יושבים בתוך הגידול חשוב לא פחות מסוגי התאים הנמצאים שם. PDAC נראה כגורם לפריסת חיסון מדכאת, יציבה וקבועה, בעוד שנוף החיסון ב-IPMN נשאר גמיש ותלוי אזור. טביעות מרחביות אלה יכולות להפוך לביומרקרים המבדילים בין גידולים מסוכנים לנגעים קדם-סרטניים ולחזות אילו מטופלים עשויים להפיק תועלת מטיפולי חיסון מסוימים. מסגרת ISPat מציעה כלי כללי לקריאה של קודי מרחב מסוג זה במחלות רבות, ותומכת בעתיד שבו טיפול בסרטן מונחה לא רק על ידי גנטיקה וסוגי תאים, אלא גם על ידי הגאוגרפיה המדויקת של התאים בתוך הגידול של כל מטופל.
ציטוט: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
מילות מפתח: סרטן הלבלב, מיקרו-סביבה של הגידול, הדמיה מרחבית, אינטראקציות חיסוניות, אונקולוגיה מדויקת