Clear Sky Science · he
מערכת תג REC ללא ליזין לשימוש בביוטינילציה בקרבה
מדוע תגיות זעירות על חלבונים חשובות
בתוך כל תא, חלבונים בדרך כלל לא פועלים לבדם — הם מתקבצים בקשרים משתנים שמניעים בריאות ומחלה. כדי לחקור את השותפויות האלה, מדענים לעתים קרובות צימדו לחלבונים "תגיות שם" קטנות כך שניתן לעקוב אחריהם, למשוך אותם מתערובת, או לראותם במיקרוסקופ. שיטה פופולרית בשם ביוטינילציה בקרבה מאפשרת לחוקרים למפות מי עומד ליד מי בתוך התא, אך יש לה בעיה נסתרת: תגיות רבות אלה עוברות שינויים כימיים ונעלמות בפועל בדיוק כשהן נדרשות ביותר. מחקר זה מציג סוג חדש של תג, שנקרא תג REC, שמעוצב להישאר נראה בתנאים תובעניים אלה.
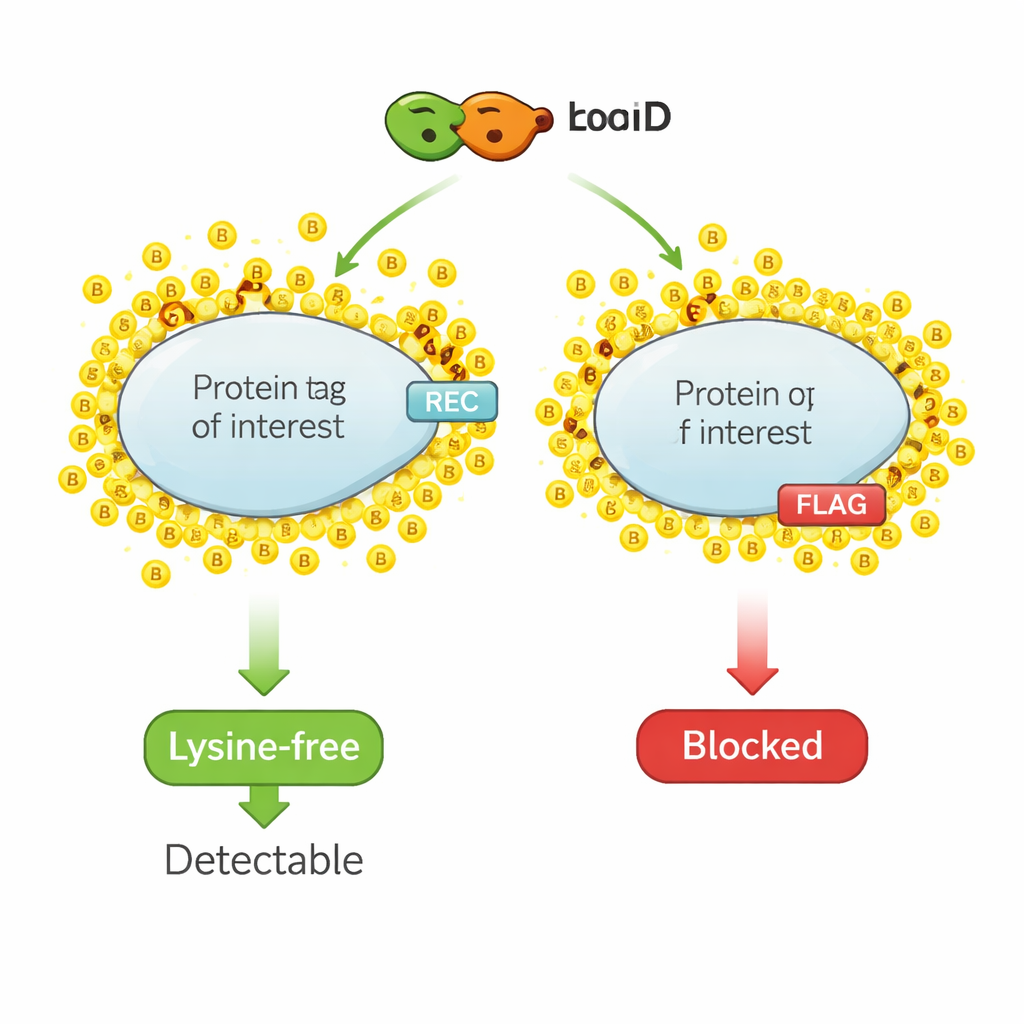
הדג כימי להדגשת שכני החלבון
ביוטינילציה בקרבה פועלת כמו טוש מולקולרי. אנזים מהונדס, כגון TurboID, מחובר לחלבון מעניין. כאשר מוסיפים ביוטין — ויטמין קטן — TurboID מצמיד במהירות מולקולות ביוטין לחלבונים בסביבה. החוקרים אז מושכים החוצה את כל החלבונים שסומנו בביו־טין ומזהים אותם, וזוכים לצילומסך של השכונה המקומית של החלבון. עם זאת, אותה כימיה המסמנת חלבונים קרובים פוגעת גם בתגיות האפיטופ הקטנות המשמשות לזיהוי, משום שהתבניות האלה בדרך כלל מכילות ליזין, חומצת אמינו שהיא אתר הנחיתה העיקרי לביוטין. כאשר הליזינים בתג מכוסים בביו־טין, נוגדנים כבר אינם מזהים את התג, והאות בשיטות זיהוי סטנדרטיות יורד או נעלם.
עיצוב תג שסירב לשינוי כימי
כדי לפתור זאת, המחברים יצאו ליצור תג חדש החסיר לחלוטין ליזין. הם התחילו מקטע של חלבון של טפיל המלריה בשם PfRipr5, שיש בו דמיון מועט לחלבונים אנושיים, מה שמפחית את הסיכון לתגובות חוצות לא רצויות. באמצעות שיטת סקר מבוססת מיקרוצ'יפ על ארנבים, הם גידלו 22 נוגדנים מונוקלונליים נגד PfRipr5 וזיהו אחד, שכונה שיבוט מס' 6, עם קשירה חזקה וספציפית במיוחד. על ידי חיתוך ושינוי סיסטמטי של מקטע ה‑PfRipr5, הם צמצמו את אתר הקשירה של הנוגדן למקטע של 11 חומצות אמינו. רצף מינימלי זה הכיל ליזין אחד בלבד, אותו הם החליפו בחומצת אמינו דומה, ארגינין. באופן מדהים, הנוגדן עדיין נקשר באותה מידה. רצף מאופטם זה, חסר הליזין, נקרא תג REC, והנוגדן המתאים נקרא נוגדן REC.
בדיקת תג REC בתנאי מעבדה
הצוות בדק אז האם תג REC יכול להחליף תגיות נפוצות כמו FLAG בטכניקות מעבדה שגרתיות. כאשר צימדו אותו לחלבונים זוהרים או חלבונים סיגנליים והפיקו במערכות ללא תאים ובתאים של יונקים, חלבונים עטופי REC זוהו בקלות על ידי אימונובלוטינג, באמצעות מבחן רגיש לאור בשם AlphaScreen, ובאימונוסטיינינג בתאים. עוצמת הזיהוי הייתה דומה לזו של תג FLAG ולמערכת תג ללא ליזין אחרת (AGIA), ונוגדן REC הראה רעש רקע מועט מאוד במגוון קווי תאים אנושיים וקופי. חשוב לציין שהתג עבד הן כשהוצב בקצה ההתחלתי והן בקצה הסופי של חלבון, ועל חלבונים הממוקמים באזורים תאיים מגוונים, כולל גרעין, מיטוכונדריה, רשתית-endoplasmic והממברנה התאית.
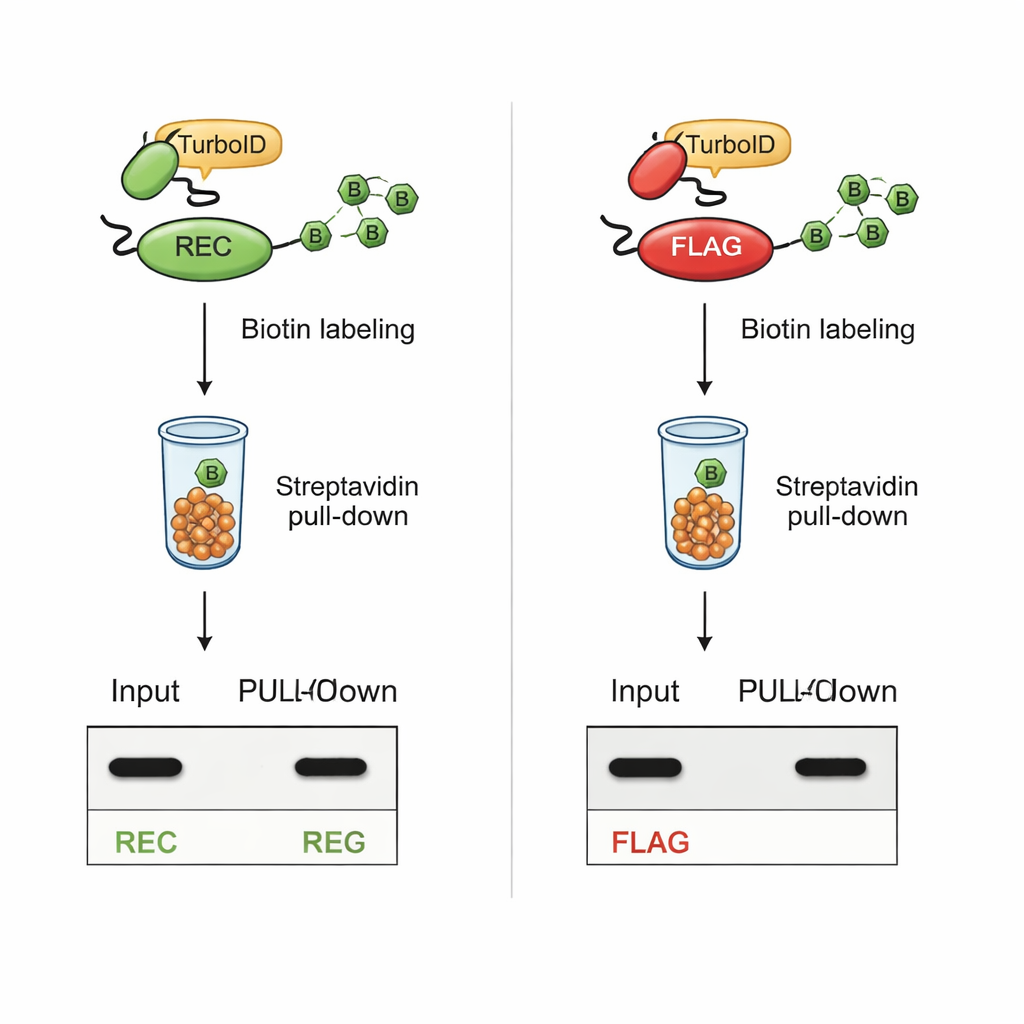
נשאר נראה במהלך סימון אינטנסיבי
המבחן הקריטי היה האם REC יישאר ניתן לזיהוי לאחר ביוטינילציה מבוססת TurboID. בתאים שבהם TurboID היה צמוד לשותפי אינטראקציה ידועים, חלבונים הנושאים את תג REC נותרו גלויים בבירור גם בתמציות תכולת התא המלאות וגם בחלק המסונן שסומן בביו־טין. בניגוד לכך, חלבונים הנושאים את תג FLAG הקלאסי איבדו את האות FLAG ברגע ש‑TurboID היה פעיל, אף על פי שהחלבונים עצמם עדיין היו נוכחים. ניסויים נוספים עם פפטידים סינתטיים הראו כי TurboID ביו־טינילט ישירות את הליזינים ברצף FLAG, מה שחוסם פיזית את הגישה של הנוגדן. תג REC, החסר ליזין לחלוטין, נותר בלתי מושפע מ‑TurboID והמשיך להיות קל לזיהוי.
מה משמעות הדבר לניסויים עתידיים
לחוקרים החוקרים רשתות חלבונים בתוך תאים חיים, תג REC מציע כלי מעשי חדש: הוא מתנהג כמו תגיות מוכרות בניסויים יומיומיים אך ממשיך לתפקד גם כשהאנזימים העוצמתיים לסימון בקרבה פעילים. משמעות הדבר היא שמדענים יכולים לאשר בצורה אמינה יותר שהחלבונים המתויגים שלהם נוכחים ונלכדו כראוי, ולחקור שינויים מבוססי ליזין אחרים — כמו יוביקויטינציה ואצטילציה — מבלי שהתג עצמו יתערב. בקיצור, REC הוא שינוי עיצובי קטן עם השפעה גדולה, שעוזר להפוך ניסויי מיפוי חלבונים מורכבים לברורים ואמינים יותר.
ציטוט: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
מילות מפתח: תיוג חלבונים, ביוטינילציה בקרבה, TurboID, אינטראקציות חלבונים, תגי אפיטופ