Clear Sky Science · he
רפרוגרמינג מטבולי משפר את העמידות ללחץ חמצוני בתאי לב בדרגת התמיינות
מדוע המאבק של תאי הלב בחמצן חשוב
כל פעימת לב שלך נשענת על תאי שריר מיוחדים הנקראים קרדיומיוציטים. ככל שאנו גדלים, תאים אלה עוברים שינוי מהותי: הם עוברים מסביבה דלת חמצן התלויה בסוכרים ברחם אל עולם עשיר בחמצן אחרי הלידה. החמצן חיוני, אך גם מייצר תוצרים מזיקים שיכולים לפגוע ב־DNA ולגרום למוות תאי. מחקר זה חוקר כיצד תאי לב בבגרות מתכוננים מחדש מבחינה מטבולית כדי להתמודד עם יותר חמצן, לייצר יותר אנרגיה ועדיין להגן על עצמם מפני נזק חמצוני — תובנות שעשויות להנחות טיפולים עתידיים למחלות לב ולרגנרציה.
מבונים פשוטים לאתלטים של כוח
תאי לב לא בשלים, הידועים כקרדיומיובלסטים, הם תאים קטנים המחלקים את עצמם ותלויים בעיקר בפירוק גלוקוז כמקור אנרגיה. כשהם מתמיינים לקרדיומיוציטים בוגרים, הם מפסיקים להתחלק, גדלים לעתים מתאחים לתאים רב־גרעיניים ומוארכים המתאימים יותר לכיווץ חזק. בעזרת מיקרוסקופיה ברזולוציה גבוהה צפו החוקרים בשינוי זה במשך עשרת הימים במודל תאי מעבדה. סמני חלוקה ירדו, והתקבלו תאים שנמתחו והתארגנו למבנים סיביים בדומה ללב, מה שאישר שהם נכנסו למצב בוגר ודחיסתי יותר. 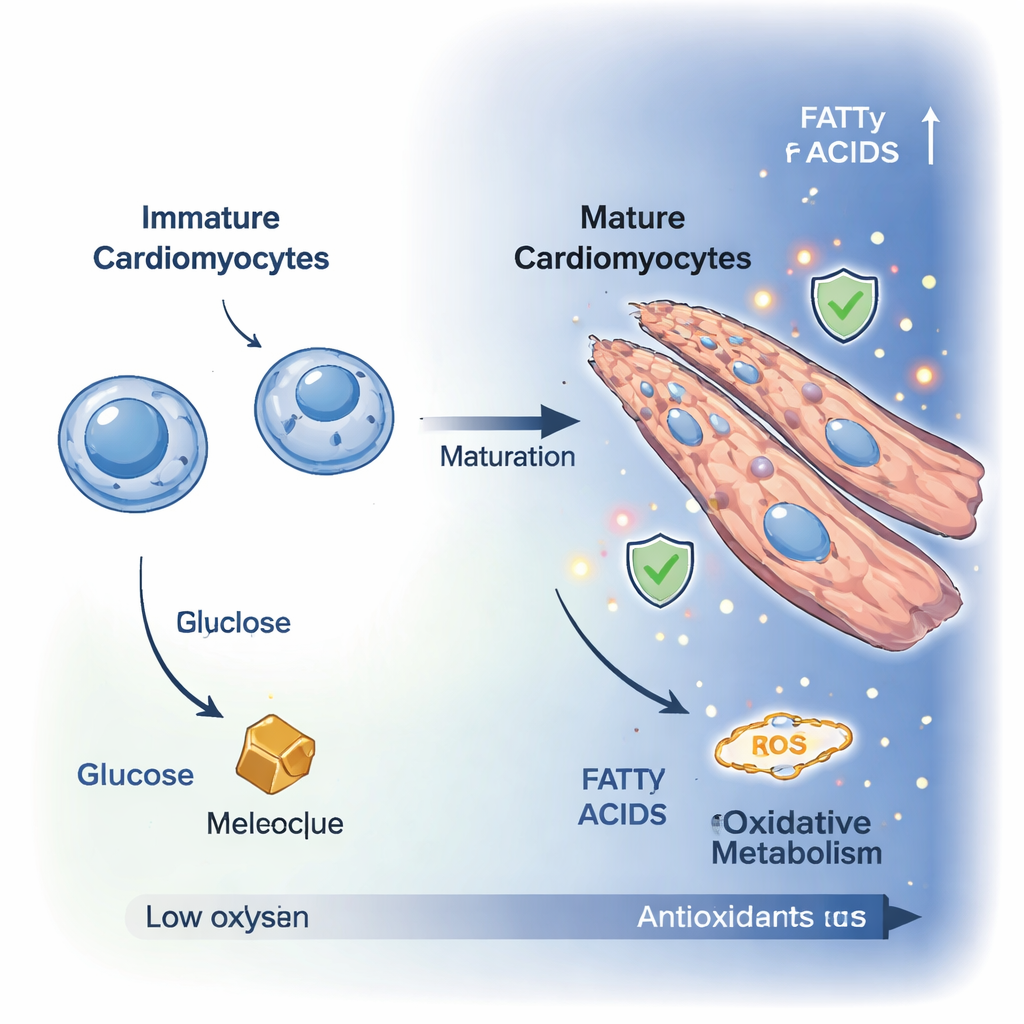
מעבר לדלקים חדשים וחיבור נתיבי אנרגיה
כדי להבין מה קורה מתחת למכסה המנוע, הצוות מדד מאות מולקולות קטנות בתוך התאים והשתמש בהדמיה מתקדמת של פלואורסנציה טבעית של התאים כדי לעקוב בזמן אמת אחרי ניצול האנרגיה. יחד הראיות הראו מעבר ברור ממצב גליקוליטי, שבו התאים בעיקר בוערים גלוקוז, למצב חמצוני שדומיננטי על ידי הנשימה המיטוכונדריאלית. רמות הגלוקוז והפרוקטוז ירדו, בעוד מתווכים של מחזור חומצת הטריקרבוקסיל (TCA) — כגון חומצה ציטרית, מלאט ואוקסו־גלוטארט — עלו. ניתוח מסלולים חשף פעילות מוגברת בדרכים שמזינות דלק אל המיטוכונדריות, כולל מעביר המלאט–אספרטט ושבירת חומצות אמינו, מה שמצביע על כך שקרדיומיוציטים בוגרים מרחיבים את אפשרויות הדלק שלהם ומערבלים את האנרגיה ביתר יעילות אל תחנות ההטענה שלהם.
לחיות עם יותר חמצן — ויותר לחץ
שריפת דלק יעילה יותר במיטוכונדריות נושאת מחיר: ייצור גבוה יותר של סוגי חמצן ריאקטיביים (ROS), מולקולות כימיות אגרסיביות שיכולות להזיק לשומנים, לחלבונים ול־DNA. החוקרים מצאו שכאשר הקרדיומיוציטים בגרו, המיטוכונדריות שלהם הפכו לגדולות ומוארכות יותר, וסמני לחץ חמצוני עלו. הדמיית פלואורסנציה גילתה יותר גרגירים דמויי ליפופוסצין, סימן לאוקסידציה של שומנים, וחזקן גרעיני הצביע על רמות ROS גבוהות יותר בתאים המתמיינים. מטבולומיקה הראתה שינויים במטבוליזם של גלוטתיון, מערכת אנטי־חמצונית מרכזית שמשתמשת בגלוטתיון — שנבנה מחומצות אמינו כמו גלוטמט וג'ליצין — לנטרול ROS. ממצאים אלה מרמזים שכאשר תאי הלב מגדילים את המטבוליזם החמצוני, הם גם מכווננים את מסלולי האנטי־אוקסידציה שלהם כדי לשמור על הנזק תחת שליטה. 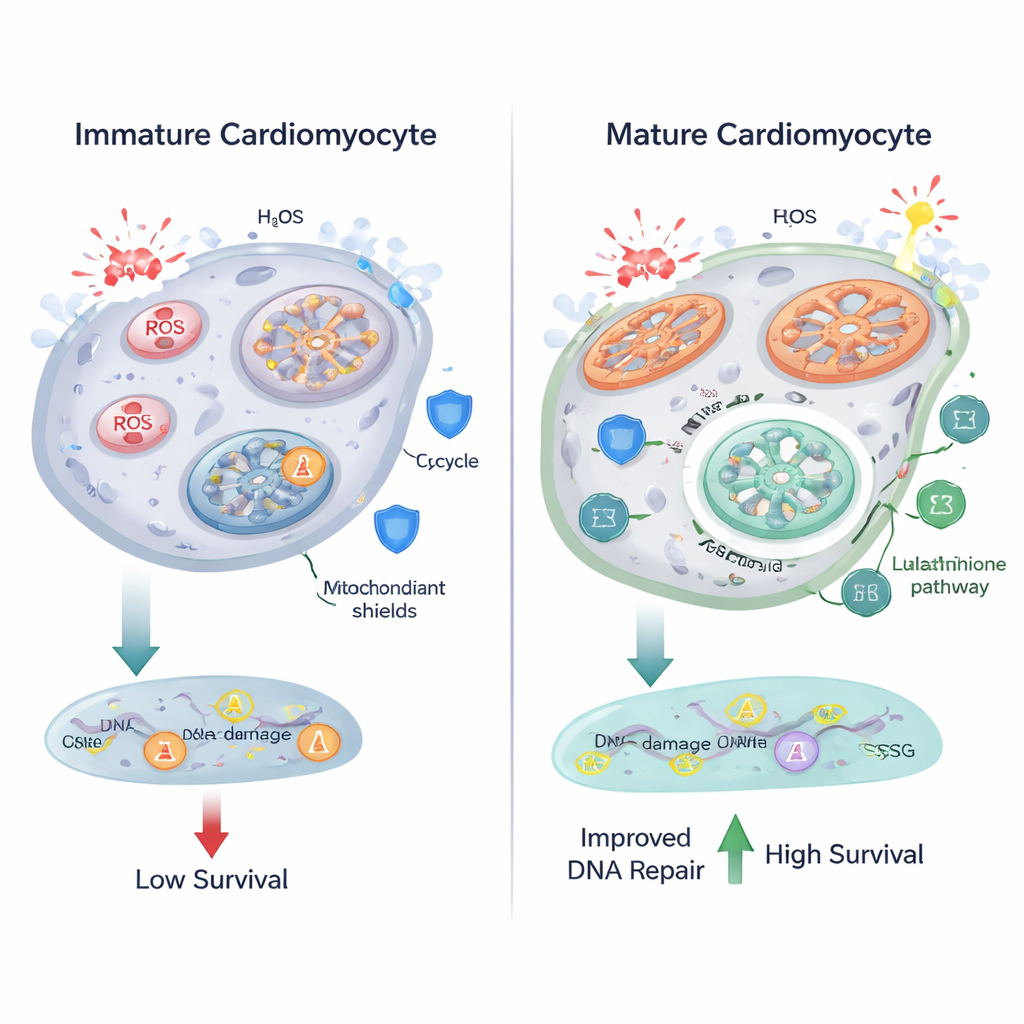
נזק מוגבל, הגנות מחוזקות
המפתיע הוא שלמרות עליית ה־ROS, קרדיומיוציטים מתמיינים לא הראו יותר שברים ב־DNA מאשר מקביליהם הבלתי בוגרים כשהנבדק היה באמצעות מוקדי γ‑H2AX, סמן רגיש לנזק DNA. כאשר הצוות אתגר את התאים עם מי חמצן, ממס מחמצן חזק, גם התאים הבלתי בוגרים וגם הבוגרים צברו ROS ושברי DNA — אך התאים הבוגרים שרדו טוב יותר. הם הראו יחסית פחות פגיעות DNA ביחס לרמות ה־ROS הגבוהות שלהם, היו פחות נוטים להפעיל סיגנלים מקושרי מוות תאי כגון PUMA והציגו שיעורי הישרדות גבוהים משמעותית. תוצאות אלה מעידות שקרדיומיוציטים מתמיינים לא רק מתאימים את המטבוליזם שלהם אלא גם משדרגים את מערכות תיקון ה־DNA והמכונות להישרדות, מה שמאפשר להם לעמוד בתנאי חמצון קשים יותר.
מה המשמעות להגנה על הלב
במילים פשוטות, מחקר זה מראה שכאשר תאי הלב בוגרים, הם לומדים לפעול חזק יותר בלי להישרף. הם עוברים מאורח חיים עשיר בסוכרים ודל־חמצן לאורח חיים אינטנסיבי בחמצן המונע על ידי מיטוכונדריות, ובמקביל בונים מגינים טובים יותר וצוותי תיקון כדי להתמודד עם לחץ חמצוני. הבנת האיזון המוקפד הזה בין ייצור אנרגיה להגנה עצמית עשויה לסייע למדענים לעצב אסטרטגיות להפוך רקמת לב בוגרת פגועה לעמידה יותר, או לייחד תאי גזע לקרדיומיוציטים בטוחים ועמידים יותר לטיפולים רגנומטיביים.
ציטוט: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
מילות מפתח: התמיינות קרדיומיוציטים, לחץ חמצוני, מיטוכונדריות, מטבוליזם תאי, מחלות לב