Clear Sky Science · he
מיון באמצעות בינה מלאכותית של ניאופלזיה רקטלית על ידי ניתוח פרפוזיה פלואורסצנטית אנדוסקופית
מדוע זה חשוב עבור מטופלים ורופאים
לאנשים עם פוליפים רקטליים גדולים, אחת השאלות המרכזיות היא האם הגידול חסר מזיק או כבר הופך לסרטן. כיום, רופאים לעתים קרובות לא יכולים לדעת בוודאות עד לאחר הסרת כל השגשוג, מה שעלול לגרור ניתוחים גדולים מהמובטח או עיכובים בטיפול. המחקר בוחן האם טכניקת דימות חכמה, בשילוב בינה מלאכותית, יכולה לזהות סרטן נסתר במהלך ההליך עצמו על ידי מעקב אחר אופן זרימת הדם ברקמה.
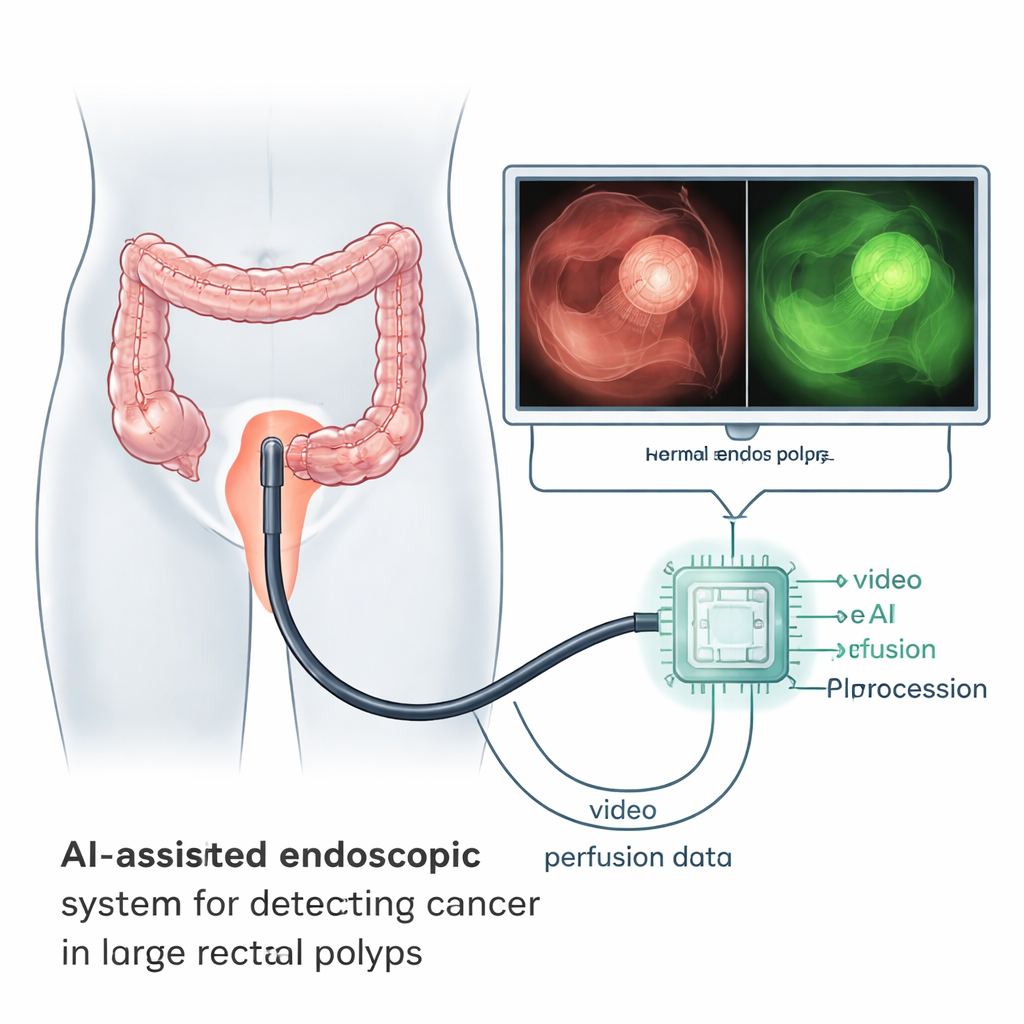
להקשיב לאופן בו הגידול מקבל אספקה
סרטן אינו גדל כמו רקמה רגילה. הוא מעורר היווצרות כלי דם חדשים וחריגים שמדלפים ומתפצלים באופן לא מסודר. שינויים אלה יוצרים דפוסים מובחנים באיך שהדם וחומרי צבע מוזרקים נשפכים לתוך הגידול ויוצאים ממנו. החוקרים השתמשו בצבע בשם אינדוציאנין גרין, הנצפה תחת אור תת‑אדום קרוב, ורשמו סרטונים קצרים במהלך ניתוחים אנדוסקופיים במטופלים עם פוליפים רקטליים גדולים וסרטן רקטלי מוקדם. על ידי מעקב אחרי עוצמת הזוהר לאורך מספר דקות ניתן היה ללכוד מעין "טביעת אצבע פרפוזיונית" לאזורים החשודים ולעור הבריא באותו מטופל.
להפוך דפוסי זוהר לנתונים
כל וידאו נותח על ידי תוכנה ייעודית שחילקה את האזור הנראה של דופן המעי לרשת של ריבועים זעירים ועקבה אחריהם לאורך זמן, גם כאשר המצלמה והרקמה נעים. עבור כל ריבוע המדד בתוכנית כמה בהירה הפכה הפלואורסצנציה, כמה מהר הגיע השיא וכמה מהר דעכה. לאחר מכן היא ניקתה ונירמלה את העקומות הללו כדי שניתן יהיה להשוותן ישירות. מתוך העקבות הזמןיות האלה הוציא הצוות תכונות מספריות פשוטות כגון עוצמת השיא והירידה באות בזמנים ספציפיים לאחר השיא. הם גם בדקו עד כמה ערכים אלה היו לא אחידים בתוך האזור הבלתי תקין, באמצעות סטטיסטיקה הלוכדת שונות בתוך הגידול בהשוואה לרקמה הבריאה הסמוכה.
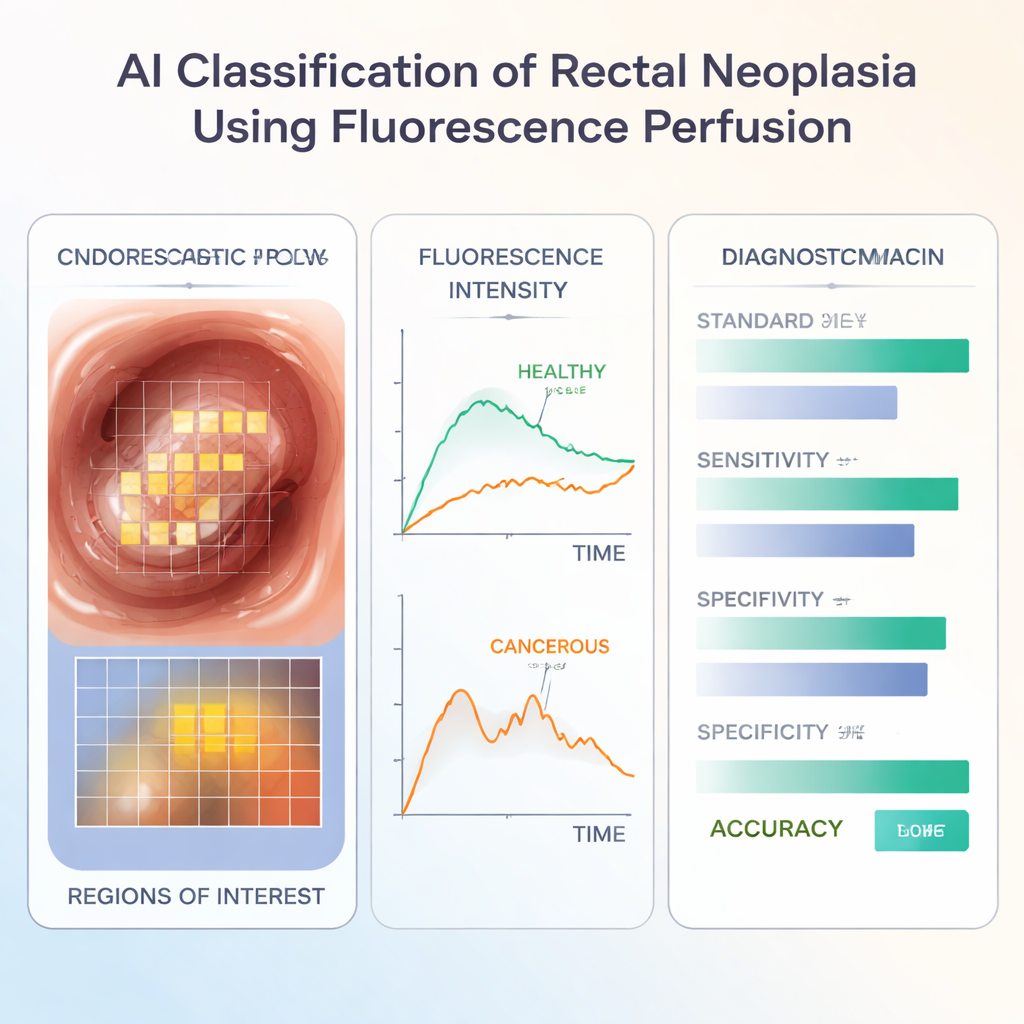
לאמן את הבינה המלאכותית
הקבוצה חקרה 190 סרטונים מ‑182 מטופלים שטופלו בשישה בתי חולים בארבע מדינות; בכמעט שלושה מתוך חמישה מטופלים אושרה בסופו של דבר נוכחות סרטן תחת המיקרוסקופ. הם אימנו מודל למידת מכונה (ממיין XGBoost) להבחין בין נגעים שפירים לגידוליים אך ורק על סמך תכונות זרימת הצבע, ללא התייחסות לתמונות הצבע הרגילות. בשימוש על מקרים חדשים זיהה המודל נכון סרטן ברוב ניכר מהמטופלים, והתפקוד שלו היה מקביל או מעט גבוה משל כלי אבחון מקובלים רבים בשימוש קליני, כגון ביופסיות אנדוסקופיות, סריקות MRI טרום‑ניתוח ורושם הוויזואלי של המנתח המומחה.
להוסיף רמזים קליניים מהעולם האמיתי
בחיי היומיום רופאים כמעט ולא סומכים על מבחן יחיד. לכן החוקרים שילבו את תפוקת ה‑AI עם מידע שכבר זמין: דוחות MRI ושיקול דעת המנתח המפעיל. כאשר מידע זה הוזן לאותה שרשרת עיבוד ממוחשבת, היכולת לזהות סרטן השתפרה, במיוחד ביכולתה לשלול מחלה בנגעים שפירים. בתרחיש הטוב ביותר, המערכת המשולבת זיהתה כ‑86% מהסרטן תוך שהיא נמנעת מאותות שווא בכ‑71% מהמקרים שאינם סרטן. הגישה עבדה גם באופן סביר בקבוצות משנה של מטופלים האופייניות יותר למחלה מוקדמת שניתנת להסרה מקומית.
מה זה עשוי להשפיע על הטיפול בעתיד
המחקר מראה כי בגידולים בפוליפים רקטליים גדולים יש חתימה ניתנת לזיהוי באופן פרפוזיוני של אופן זרימת הדם והצבע דרכם, וניתן לזהות חתימה זו באופן אוטומטי על ידי בינה מלאכותית. על אף שהעבודה עד כה בוצעה על סרטונים מוקלטים והיא עדיין צריכה הוכחה בניסויים קליניים בזמן אמת, היא מצביעה על עתיד שבו קולונוסקופ יכול לקבל התרעה, במהלך ההליך, כי פוליפ שנראה חסר סכנה מסתיר ככל הנראה סרטן פולשני. מידע זה יכול להנחות היכן לבצע ביופסיה, האם להסיר את הנגע באופן מקומי או להפנות את המטופל לניתוח מקיף יותר, ובכך להפחית גם סרטן שפספסו וגם ניתוחים גדולים מיותרים.
ציטוט: Boland, P.A., MacAonghusa, P., Singaravelu, A. et al. Artificial intelligence classification of rectal neoplasia by endoscopic fluorescence perfusion analysis. Sci Rep 16, 4761 (2026). https://doi.org/10.1038/s41598-026-35233-x
מילות מפתח: סרטן רקטום, דימות אנדוסקופי, פרפוזיה פלואורסצנטית, בינה מלאכותית, למידת מכונה