Clear Sky Science · he
ננוקאפסולות כיטוזן–דקסטרן סולפט לשיפור היעילות של טיגיציקלין נגד Salmonella enterica שאינן טיפואידיות
מדוע זה חשוב לבטיחות המזון
רוב האנשים מכירים את סלמונלה כסיבה מרשעת להרעלת מזון, לעתים קרובות מקשר לעוף לא מבושל היטב. מעטים מודעים לכך שכמה זנים הפכו לעמידים כל כך לאנטיביוטיקה שאפילו תרופות חזקות "של המגרה האחרון" עלולות להיכשל. המחקר הזה חוקר גישה מבוססת ננוטכנולוגיה להציל תרופה כזו, טיגיציקלין, על ידי אריזתה בתוך קפסולות מזוקקות מסוכרים זעירים שעוזרות לה להחליק לתוך תאים נגועים ולכבות מנגנוני עמידות מרכזיים בסלמונלה.
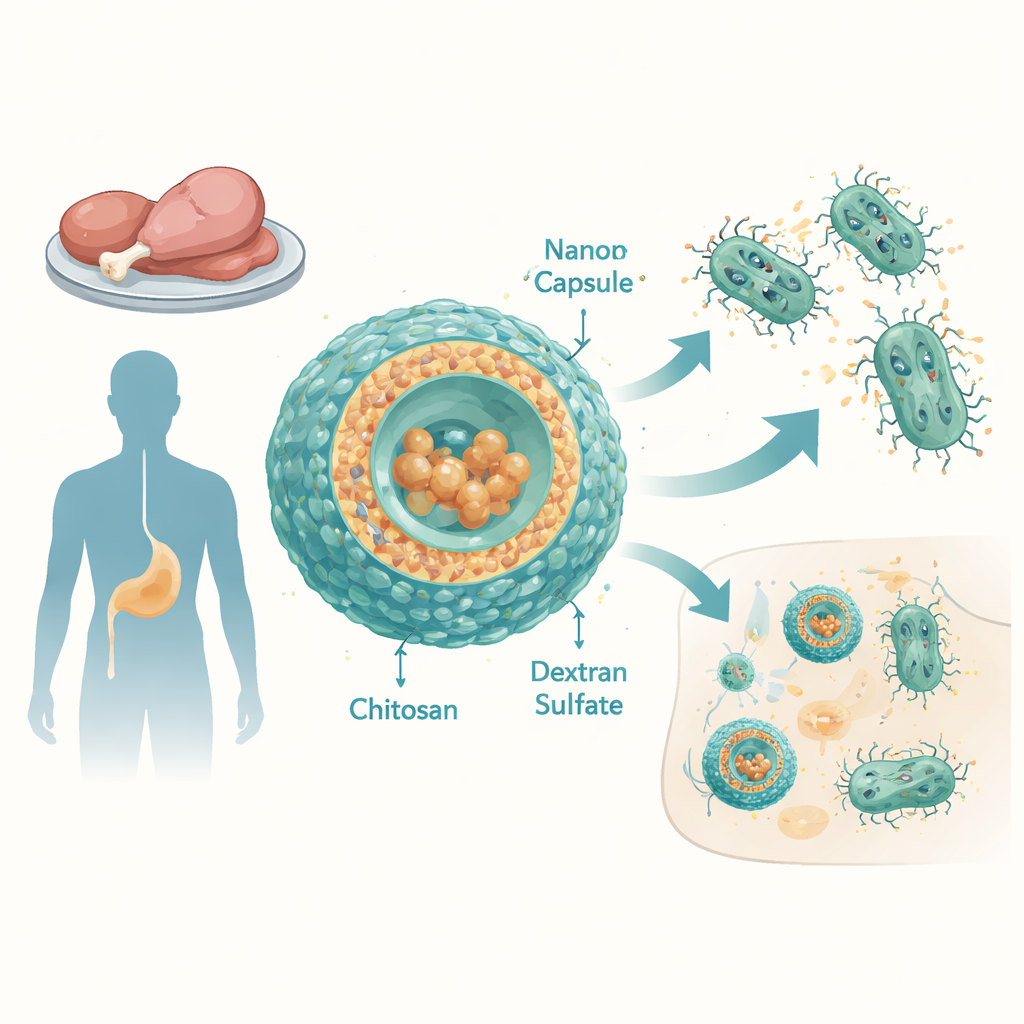
האיום הגובר מזני סלמונלה עקשניים
סרווארים של Salmonella שאינם טיפואידיות (NTS) הם גורם מוביל לשלשול וזיהומים במערכת הדם ברחבי העולם, במיוחד במדינות בעלות הכנסה נמוכה ובינונית. החוקרים בדקו 12 זני Salmonella enterica שנלקחו מבשר עוף וברווז במצרים. זנים אלה היו עמידים להרבה אנטיביוטיקות נפוצות, כולל פניצילינים, צפלוספורינים, טטרציקלינים ואחרות, והציגו ציוני עמידות מרובים גבוהים. אפילו טיגיציקלין, תרופה רחבת-ספקטרום המיועדת למקרים קשים, פעלה היטב במידה מועטה: החיידקים יכלו לסבול ריכוזים גבוהים מאוד שלה. סיבה מרכזית לכך הייתה משאבות פליטה פעילות יתר—מכונות מולקולריות הממוקמות בממברנת החיידק ושואבות כל הזמן את האנטיביוטיקה החוצה מהתא.
בנייה של קפסולת־תרופה חכמה
כדי להתגבר על כך, הצוות תכנן קפסולות בקנה־מידה ננו העשויות משני פולימרים שמקורם בטבע: כיטוזן, שמקורו בכיטין (החומר בקליפות רכיכות), ודהקסטרן סולפט, מולקולת סוכר מסועפת. באמצעות כוונון מדויק של יחס החומרים הללו הם הפיקו חלקיקים יציבים בקוטר של כ־100–150 ננומטר, עם מטען פני חיובי שעוזר להם להתקשר לממברנות החיידק והמאחסן. טיגיציקלין הוטען לתוך חלקיקים אלה ביעילות מרשימה—בפועל כל התרופה נכנסה לקפסולות. בניסויים במעבדה המדמים תנאים במחזור הדם, הקפסולות שחררו את רוב הטיגיציקלין בתוך כמה שעות, מה שמרמז שהן יכולות לספק גל חזק של אנטיביוטיקה באתרי הזיהום.
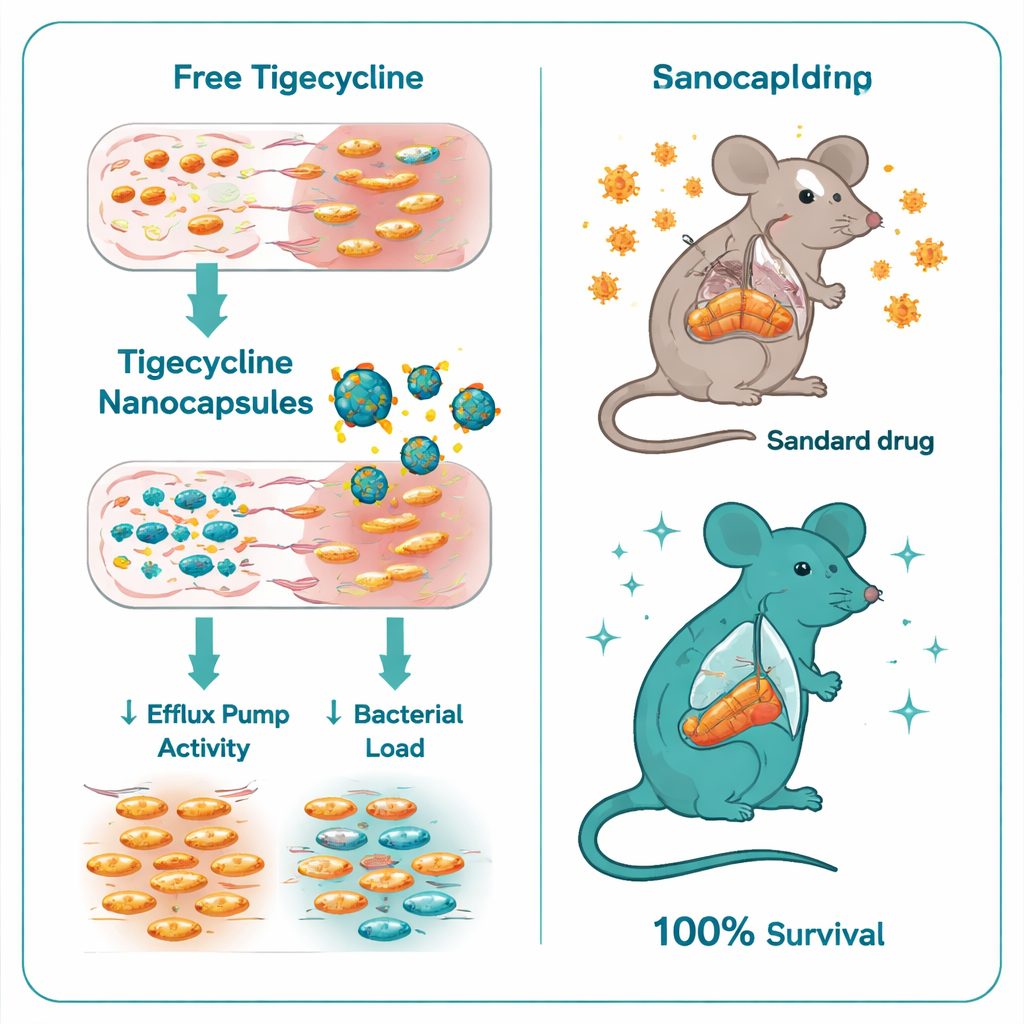
החלשת מנגנוני ההגנה של החיידק
כאשר החוקרים השוו טיגיציקלין פשוט מול טיגיציקלין עטוף בננוקאפסולות כיטוזן–דקסטרן סולפט, ההבדל היה דרמטי. הריכוז המינימלי של התרופה הדרוש לעיכוב גדילת החיידק ירד מ־32–128 מיקרוגרם למיליליטר בטיגיציקלין הפשוט ל־רק 0.5–1 מיקרוגרם למיליליטר עם הננוקאפסולות—שיפור של פי שש עד שבע. ניסויי זמן-הריגה הציגו כי הצורה המוטמעת הרגה את הסלמונלה מהר ובאופן יסודי יותר. ברמה הגנטית, הננוקאפסולות גם השתקו רגולטורים מרכזיים של עמידות: הביטוי של הגנים ramA ו‑acrB, המסייעים בשליטה ובהרכבת משאבות הפליטה העיקריות, ירד במספר פי טיפול בחיידקים. במילים אחרות, הקפסולות לא רק סיפקו יותר תרופה; הן עזרו לכבות אחד מנתיבי המילוט העיקריים של החיידק.
הגנה על עכברים נגועים ממחלה קטלנית
הצוות בדק לאחר מכן את הנוסחה החדשה במודל עכבר לזיהום חמור ב‑Salmonella Typhimurium. כל העכברים הנגועים שלא טופלו מתו בתוך שמונה ימים. עכברים שקיבלו טיגיציקלין סטנדרטי התרבו במצב טוב יותר אך עדיין סבלו מתמותה גבוהה, כאשר רק 40% שרדו. בניגוד חמור לכך, כל העכברים שטופלו בננוקאפסולות המכילות טיגיציקלין שרדו. בעלי החיים הללו הכילו הרבה פחות חיידקים בכבד ובמעיים, תוצאות בדיקות דם שהראו תפקוד כבד וכליות קרוב לנורמה, ונזק רקמתי הרבה יותר מתון בבדיקה מיקרוסקופית. אפילו הקפסולות הריקות של כיטוזן–דקסטרן סולפט, ללא אנטיביוטיקה, העניקו מידה מסוימת של הגנה, סביר שהודות להשפעות אנטימיקרוביאליות ואנטי-דלקתיות מתונות של הכיטוזן עצמו, אך השילוב עם טיגיציקלין היה בעל עדיפות ברורה.
מה משמעות הדבר לטיפולים עתידיים
עבור לא-מומחים, המסר המרכזי הוא שאריזת אנטיביוטיקה קיימת בתוך ננוקאפסולה חכמה וביוקאומפטבילית יכולה להשיב את יעילותה נגד סלמונלה עמידה מאוד. על ידי עזרה לתרופה להגיע לחיידקים המתחבאים בתוך תאים ועל ידי דיכוי המשאבות שמרוקנות בדרך כלל את התרופה החוצה, מערכת כיטוזן–דקסטרן סולפט הפכה אנטיביוטיקה של רזרבה שנאבקה לטיפול יעיל מאוד בעכברים, עם 100% הישרדות. בעוד שעדיין נדרשים מחקרים נוספים לפני שניתן יהיה ליישם גישה זו בבני אדם או בחיות משק, היא מציעה דרך מבטיחה להאריך את חיי השימוש של אנטיביוטיקות חשובות ולשפר את בטיחות אספקת המזון שלנו מבלי להמציא תרופות חדשות מהיסוד.
ציטוט: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
מילות מפתח: סלמונלה, עמידות לאנטיביוטיקה, ננוכּרסוליות, העברת תרופות, טיגיציקלין