Clear Sky Science · he
פרוטאומיקה ומטבולומיקה משולבות חושפות שחלבוני לטונים ססקו‑טרפניים צמחיים מעכבים פעילות של סרטן שד משולש‑שלילי על‑ידי דלדול סינתזת ATP ותכנות מחדש של מטבוליזם ראשוני
תרכובות צמחיות שמרעיבות סרטן שד אלים
סרטן השד המשולש‑שלילי הוא אחת הצורות הקשות ביותר לטיפול כיוון שהוא חסר את ה״ידיות״ ההורמונליות הרגילות שהתרופות רבות נוהגות לתפוס. מחקר זה בוחן שתי מולקולות שמופקות מצמח מרפא ונראות כאילו הן סוגרות את תחנות הכוח הפנימיות של תאי סרטן אלה, חותכות את אספקת האנרגיה שלהם בעוד שהתאים השדיים התקינים נשמרים יחסית. הבנת המנגנון עשויה לפתוח דלת לטיפולים ממוקדים ועדינים יותר עבור מטופלים שמעטים עבורם האפשרויות כיום.
מדוע חשוב לתקוף את מקור הכוח של הסרטן
כל תא תלוי במבנים זעירים שנקראים מיטוכונדריות כדי לייצר ATP, הדלק הבסיסי של התא. תאי סרטן, ובפרט תאים אגרסיביים, לעתים קרובות תלויים יתר על המידה במיטוכונדריות שלהם כדי לתמוך בצמיחה מהירה, בהפצה ובהישרדות במצבי לחץ. החוקרים התמקדו בתאי סרטן שד משולש‑שלילי, שמייצגים כ‑15–20% מהמקרי סרטן השד ונוטים לחזור ולהתפתח גרורות לעתים תכופות יותר מסוגים אחרים. הם חקרו מולקולה טבעית, דיאוקסילפנטופין (DET), ואת הדמויה המעובדת שלה DETD‑35, שתיהן לטונים ססקו‑טרפניים מצמח המרפא Elephantopus. עבודות קודמות הראו שהתרכובות הללו מעוררות מתח חמצוני וצורות בלתי שגרתיות של מוות תאי בתאי סרטן, אבל לא הובהר במלואו כיצד הן מפריעות לתחנות האנרגיה של התאים.
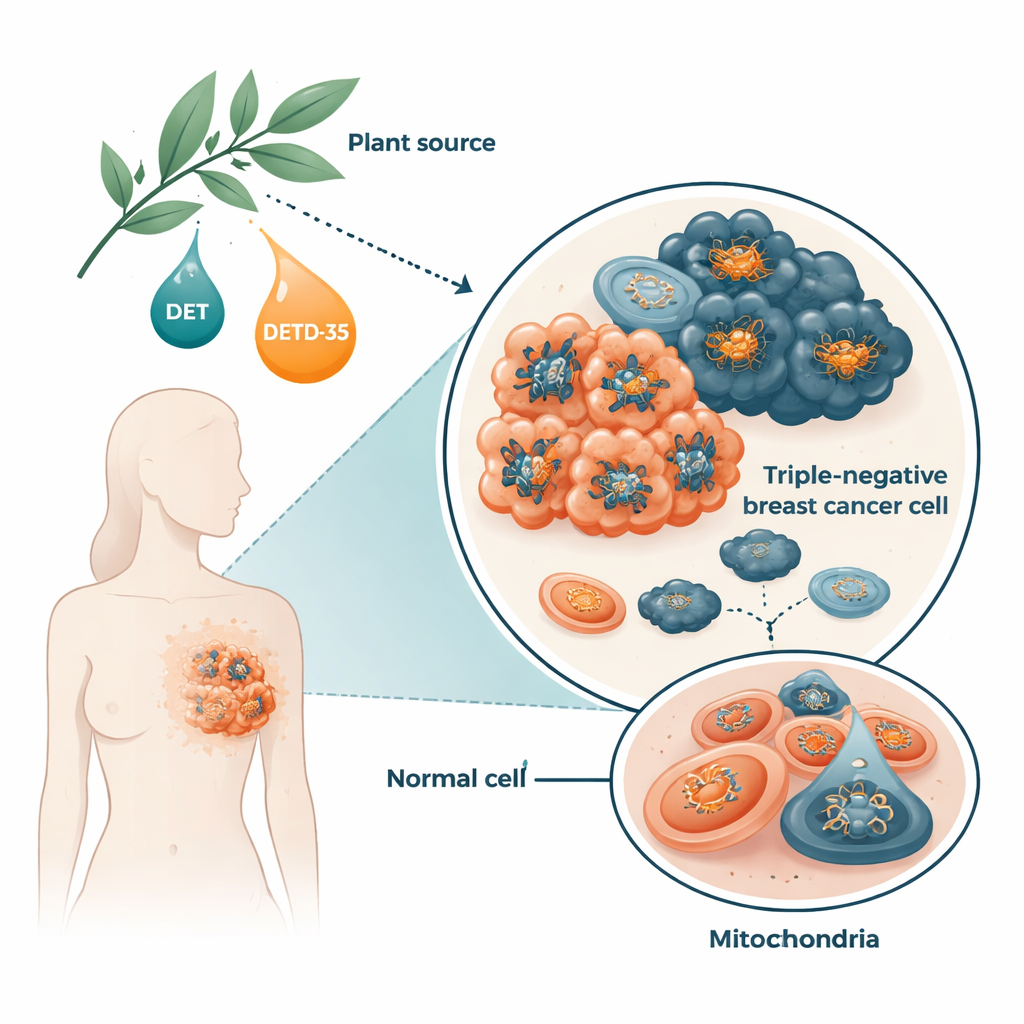
כיצד המולקולות הצמחיות משבשות את מיטוכונדריות תאי הסרטן
בעבודה עם תאי סרטן שד משולש‑שלילי של אדם שגודלו במעבדה, הצוות מצא ש‑DET ו‑DETD‑35 הגבירו במהירות את ייצור סוגי חמצן תגובתי, מעין ״פליטה״ כימית שנוצרת במהלך ייצור האנרגיה. בתגובה, התאים הגבירו ביטוי של אנזימים מגנים מסוימים, אבל לא די כדי לשחזר את האיזון. התרכובות גם הכריחו פתיחה של תעלת מעבר חדירה בממברנת המיטוכונדריה, הידועה כ‑permeability transition pore, שינוי הקשור לנפיחות, אובדן מטעני ממברנה ושלבי־התחלה של מוות תאי. בתוך שעות ספורות רמות ה‑ATP בתוך תאי הסרטן צנחו באופן חד. כשהחוקרים הוסיפו אנטי‑אוקסידנט מראש, ההשפעות המזיקות הופרו ברובן, מה שמראה שמתח חמצוני הוא מרכיב מרכזי בתהליך.
מיפוי הנזק לחלבונים ולמטבוליזם
כדי להבין את התמונה הרחבה, המדענים שילבו שתי גישות «אומיות» עוצמתיות. הם קטלגו אלפי חלבונים מיטוכונדריאליים ומדדו מטבוליטים קטנים רבים בתאים מטופלים לעומת לא‑מטופלים. התצפית המשולבת חשפה ש‑DET ו‑DETD‑35 הפריעו לחלבונים המעורבים ב phosphorylative oxidative, הדרך העיקרית שבה המיטוכונדריות מייצרות ATP, והפעילו איתותים הקשורים למוות. במקביל, נתיבים מטבוליים מרכזיים המטפלים בחומצות אמינו, בשומנים ובאבני הבניין של ה‑DNA עברו תכנות מחדש. ליפידים מסוימים שתורמים לעיצוב הממברנה הפנימית של המיטוכונדריה, וכן מולקולות הקשורות להגנה אנטי‑חמצונית ולפירוק סוכרים, השתנו באופן התואם לתאים לחוצים ומורגזי אנרגיה. באופן מהותי, שינויים נרחבים אלה לא נצפו בתאי רקמת שד נורמליים שנחשפו לאותם מינונים, דבר שמרמז על מידת סלקטיביות כלפי תאי הגידול.
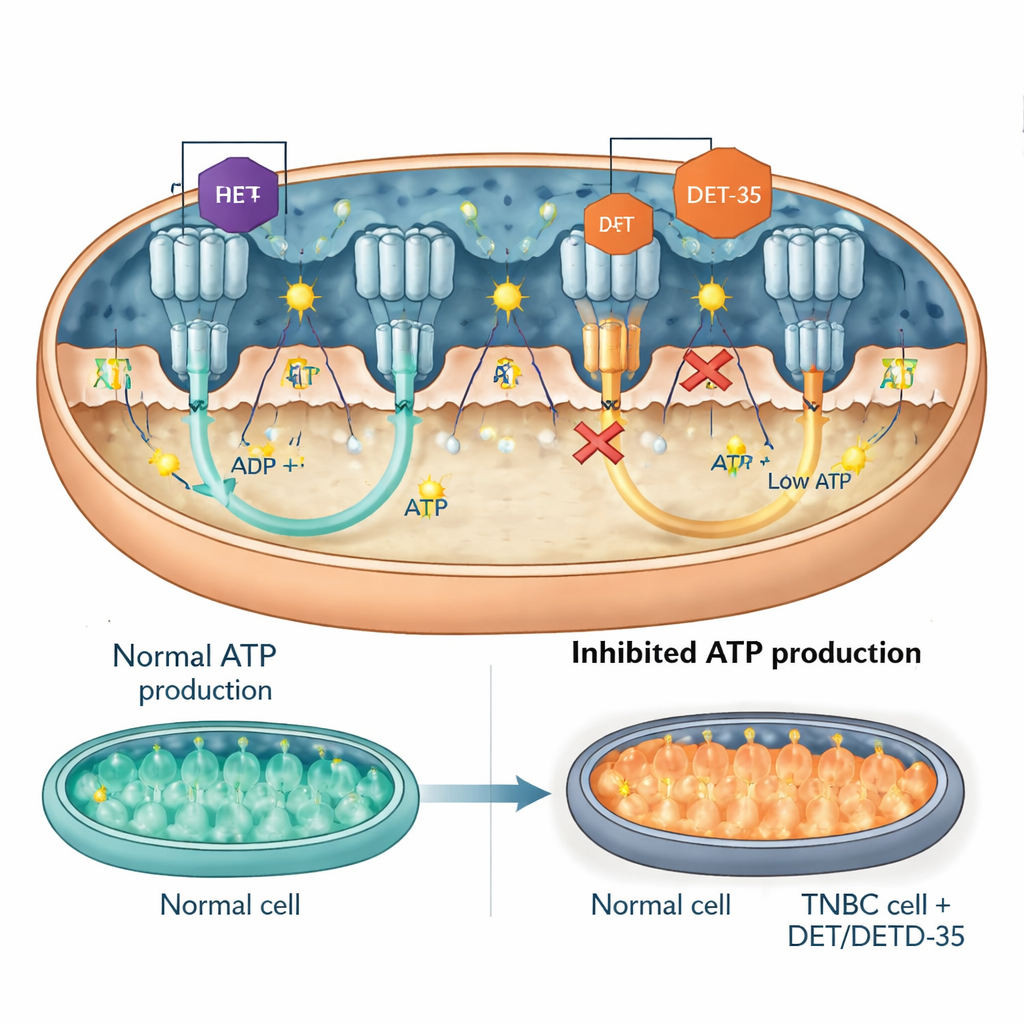
חלבון איתות מפתח וטורבינת ה‑ATP עצמה
בהמשך הצוות התרכז במשתתפים ספציפיים בתוך הרשתות המופרעות האלה. אחד מהם היה PRKCA, חלבון איתות שיכול לעבור למיטוכונדריה ולהשפיע הן על תפוקת האנרגיה והן על תגובות למתח. DET ו‑DETD‑35 הגבילו את רמות PRKCA בתאי הסרטן. כאשר החוקרים דיכאו גנטית את PRKCA, התרופות הפכו לפחות רעילות: תאי הסרטן שרדו יותר, ייצרו יותר ATP והציגו סימנים פחותים של ליקוי מיטוכונדריאלי ואפופטוזה. מוקד נוסף היה ATP סינתאז, ה״טורבינה״ המולקולרית הסובבת ליצירת ATP. מדידות הראו ש‑DET ו‑DETD‑35 הקטינו ישירות את פעילות ה‑ATP סינתאז במיטוכונדריות של תאי הסרטן. מודלים ממוחשבים של דוקינג הציעו ששתי התרכובות מתחפרות בממשקים קריטיים של האנזים, אותם אזורים כלליים שבהם נקשרים גם תרופות ידועות החוסמות את ה‑ATP סינתאז, מה שמפריע תפקידו המכניסטי וחותך את תפוקת ה‑ATP. בעכברים נשאים גידולים משולש‑שליליים של אדם, טיפול באחת מהתרכובות הוריד את רמות רכיבי ה‑ATP סינתאז ברקמת הגידול, תומך בממצאים מהמבחנה.
מה זה עשוי להצביע לגבי טיפולים עתידיים בסרטן
בסך הכל, המחקר מצייר תמונה עקבית: תרכובות מוצאות‑צמחיות אלה דוחפות תאי סרטן שד משולש‑שלילי למשבר אנרגטי על‑ידי הצפתם במתח חמצוני, פתיחת נקבי מעבר במיטוכונדריה וחסימת מכונת יצירת ה‑ATP באופן ישיר. ככל ש‑ATP דל ומטבוליזם מבולגן, תאי הסרטן מאבדים את יכולתם לגדול ולהישאר בחיים, בעוד שתאי שד נורמליים נשארים ברובם בלתי מושפעים באותם תנאים. לקורא שאינו מומחה, המסקנה היא שאפשר לנצל את התלות הניכרת של הסרטן בתחנות הכוח הפנימיות שלו, בעזרת מולקולות מתוכננות בקפידה—חלקן בהשראת צמחים—כדי לרוקן את סוללות התאים הסרטניים בלי לנתק את הרקמה הבריאה. נדרש עוד הרבה עבודה לפני שהסוכנים הללו עשויים להגיע לקליניקה, אבל התמונה המשולבת של חלבונים, מטבוליטים וזרימת אנרגיה מספקת מפת דרך מבטיחה.
ציטוט: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
מילות מפתח: סרטן שד משולש‑שלילי, מיטוכונדריה, ATP סינתאז, מוצרי טבע, מטבוליזם של סרטן