Clear Sky Science · he
חיידקים ממזונות וממיקרוביום המעי מייצרים מתילגליאוקסל ומהמטבוליט הזה נוצרות אלקלואידים פעילי‑ביולוגי מסוג 1‑אצטיל‑β‑קרבולין
מדוע מעבדה הכימית של מעי־הבטן חשובה
בתוך המעי שלנו ובמזונות רבים מותססים, טריליוני חיידקים ממירים באופן מתמיד את הסוכרים שאנו אוכלים לשורת תוצרי לוואי כימיים. המחקר הזה בוחן לעומק מסלול אחד כזה: כיצד חלק מהחיידקים הנפוצים הופכים סוכרים לצבען תגובתיות גבוהה שנקרא מתילגליאוקסל, ואחר כך למשפחה של מולקולות ביואקטיביות הנקראות 1‑אצטיל‑β‑קרבולינים. מאחר וחומרים אלה מקושרים גם לתהליכי מחלה וגם לאפשרויות תרופתיות חדשות, הבנת מתי וכיצד חיידקים מייצרים אותם עשויה לשנות את הדרך שבה אנו חושבים על מזון, המיקרוביום והבריאות.
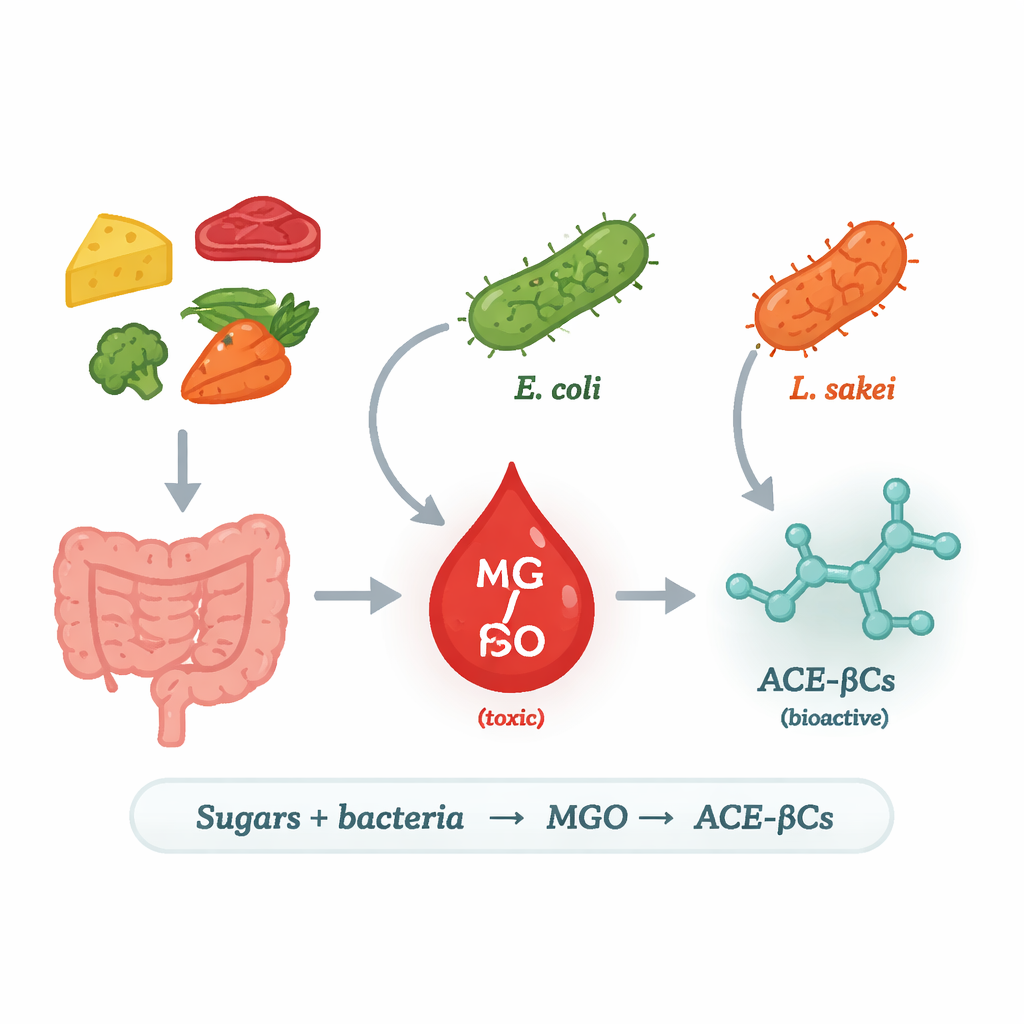
מסוכרים יומיומיים למולקולה מסוכנת
החוקרים התמקדו במתילגליאוקסל (MGO), תוצר לוואי של פירוק סוכר שהוא מאוד תגובתי ורעיל. בבני אדם, עודף של MGO מקושר לסוכרת, מחלות לב ולניו־דגנרציה עצבית, כי הוא יכול לפגוע בחלבונים וב‑DNA. התאים שלנו בדרך כלל שומרים על MGO תחת שליטה באמצעות מערכות לנטרול רעלים, אך הם אינם המקור היחיד: חיידקים גם יכולים לייצר MGO. בחלק מהמיקרובים, אנזים בשם מתילגליאוקסל סינתאז (MgsA) ממיר ישירות ביניים של עיבוד סוכר ל‑MGO, ויוצר "קיצור דרך" במטבוליזם האנרגטי. הצוות שאל אילו חיידקי מזון ומעי משתמשים בדרך זו, באילו תנאים, ומה קורה ל‑MGO שהם משחררים.
מי המפיקים החיידקיים?
כדי לענות על כך, המדענים גדלו כמה זני חיידקים חומצתיים שנפוצים במזון, יחד עם זן מעבדה של Escherichia coli, בתווך מבוקר containing או גלוקוז או גלקטוז. הם עקבו אחר MGO ושני אלקלואידים קרובים בנוזל התרבית לאורך זמן באמצעות כרומטוגרפיה ומסת‑ספקטומטריה ברזולוציה גבוהה. רק E. coli והמין הקשור לבשר Lactilactobacillus sakei ייצרו כמויות משמעותיות של MGO והאלקלואידים; חיידקי החומצה החלבית האחרים שנבדקו לא עשו זאת. חיפוש גנומי גילה את ההבדל המכריע: ל‑E. coli ול‑L. sakei יש את הגן ל‑MgsA, בעוד שרוב קרוביהן של חיידקי החומצה החלבית לא נושאים אותו. כאשר החוקרים הוסיפו את הגן mgsA מ‑L. sakei לזן שלא ייצר, אותו חיידק מהונדס החל לייצר הן MGO והן את האלקלואידים, וקשר חד־משמעי בין MgsA למסלול זה נקבע.
כיצד MGO הרעיל הופך לאלקלואידים ביואקטיביים
השאלה הבאה הייתה מה קורה ל‑MGO לאחר שנוצר. הצוות התרכז באלקלואידים 1‑אצטיל‑β‑קרבולין (ACE‑βCs), מולקולות קטנות שהודווחו כבעלות פעילות אנטימיקרוביאלית, אנטי‑דלקתית ואנטי‑סרטנית. הם הראו שכאשר חיידקים מייצרי MGO גודלו בנוכחות חומצת האמינו L‑טריפטופן, רמות של שני ACE‑βCs — 1‑אצטיל‑β‑קרבולין וצורת החומצה הקרבוקסילית ב‑3 — עלו באופן חזק. הוספת MGO נוספת לתווך גם הגביר את היווצרותם. זה מצביע על כך ש‑MGO דולף החוצה מהתאים ומגיב באופן ספונטני עם L‑טריפטופן בנוזל הסובב, ללא צורך באנזימים נוספים, כדי לייצר את התרכובות הביואקטיביות הללו. במילים אחרות, אותה כימיה שהופכת את MGO למסוכן גם הופכת אותו למולקולות מורכבות יותר שעשויות להיות להן השפעות מועילות.
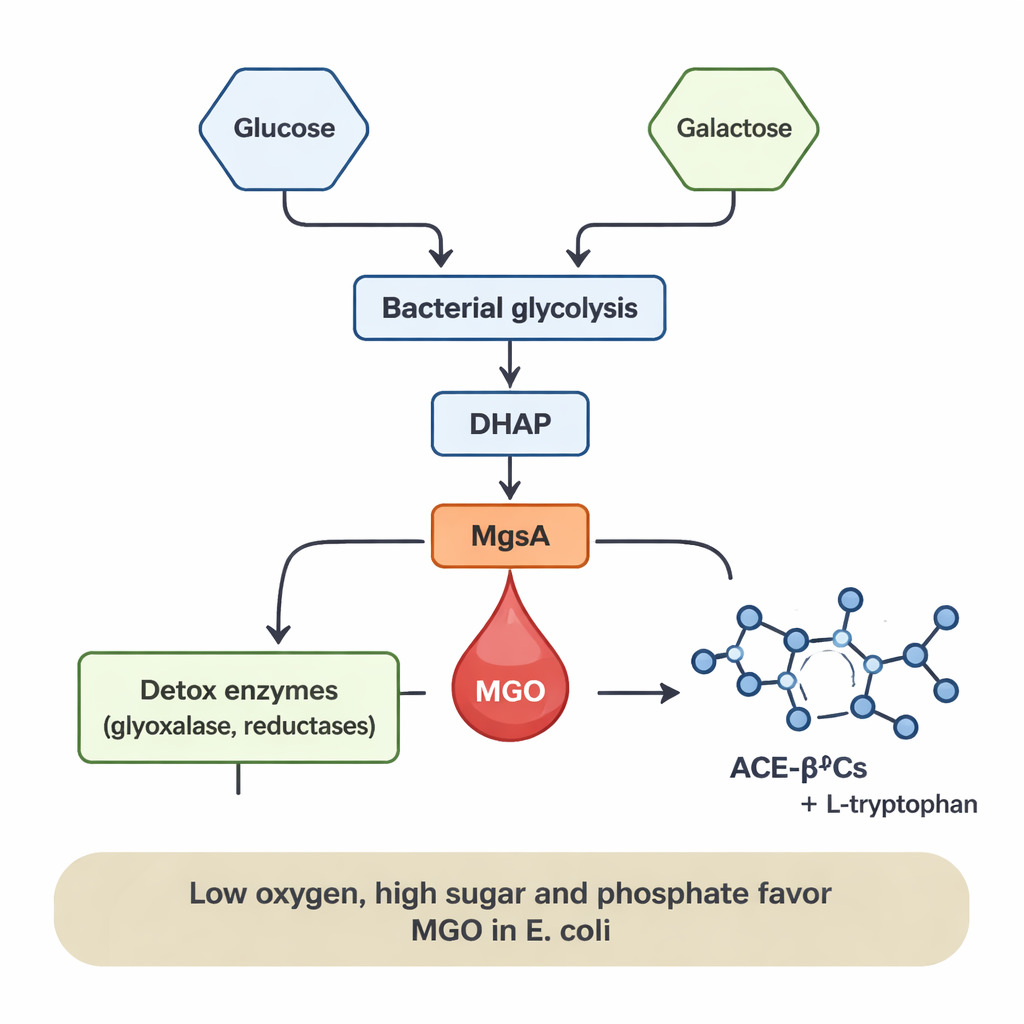
מה מעלה ומוריד את הייצור
ייצור ה‑MGO לא היה קבוע; הוא תלוי חזק בתזונה ובסביבה של החיידקים. ב‑E. coli, MGO הופיע רק כאשר גלוקוז היה נוכח, ורמותיו עלו ככל שריכוז הגלוקוז גדל. הוספת פוספט, מינרל תזונתי שכיח, הגבירה אף יותר את היווצרות ה‑MGO במספר מונים, כנראה כי היא מעודדת הצטברות של ביניים מסוכרים מזורחנים שמזינים את קיצור הדרך של MgsA. תנאי חוסר חמצן (אנאירוביים) — דומים לאלה במעי האנושי — העדיפו גם הם שחרור MGO, בעוד שתנאי חמצון גבוהים ומאווררים היטב הקטינו אותו באופן חד אף שהחיידקים המשיכו לגדול היטב. לעומת זאת, L. sakei ייצר בעיקר MGO כאשר גודל על גלקטוז, והייצור עלה עם רמות גלקטוז גבוהות יותר. דפוסים אלה מציעים שכשזרימת הסוכר במטבוליזם החיידקי גבוהה והחמצון מוגבל, MGO יכול לפעול כ"שסתום לחץ" המשחרר את המתח של הצטברות ביניים סוכריים.
מה משמעות הדבר למזון ולבריאות
הממצאים מרמזים שלא כל החיידקים במעי או במזון שווים ביכולתם לייצר MGO ו‑ACE‑βCs. מינים הנושאים את האנזים MgsA, כגון זנים מסוימים של L. sakei ו‑E. coli, יכולים להיות תורמים משמעותיים, במיוחד בסביבות עשירות בסוכר ובעלות חמצון נמוך כמו המעי או חלק מהתסיסות. ה‑MGO שהם מפרישים עשוי להוסיף לעומס הכימי הכולל על רקמות המארח, אך המרה שלו לאלקלואידי ACE‑βC עשויה גם לחלקית "לספוג" את המולקולה התגובתית הזו תוך יצירת מולקולות בעלות השפעות ביולוגיות משלהן. למרות שהמחקר נערך בתרביות מעבדה, הוא מדגיש מסלול סביר שבו תזונה, הרכב המיקרוביום ומטבוליזם חיידקי מעצבים יחד את האיזון בין חומרים מזיקים ופוטנציאליים מועילים בגופנו, ומצביע על ACE‑βCs כסמנים אפשריים לייצור MGO חיידקי במזון ובמעי.
ציטוט: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
מילות מפתח: מיקרוביום המעי, מתילגליאוקסל, מטבוליזם חיידקי, תסיסה של מזון, אלקלואידי β‑קרבולין