Clear Sky Science · he
חומצת חלב מסדירה את ציר YTHDF2-FTH1 כדי לקדם פרופתוזיס של מיוציטים ולהחמיר פגיעה איסכמית-שחזורית בלב
מדוע מטופלים לבביים צריכים לשים לב לכימיה הזו
כאשר רופאים משחיתים עורק חוסם בלב אחרי התקף לב, גל הדם הטרי מציל שריר אך עלול גם לגרום לנזק נוסף, המוכר כנזק איסכמיה–שחזור. מחקר זה חושף חשוד מפתיע בתוך תאי הלב: תוצר מטבולי נפוץ — חומצת חלב. המחברים מראים שחומצת החלב יכולה להדליק מתג מולקולרי שמדחף תאי לב לעבר סוג מסוים של מוות תאי המונע על ידי ברזל, ובכך מחמיר את הנזק. הבנת המסלול המוסתר הזה עשויה להצביע על דרכים חדשות לפיתוח תרופות שיגן טוב יותר על הלב במהלך טיפול חירום.
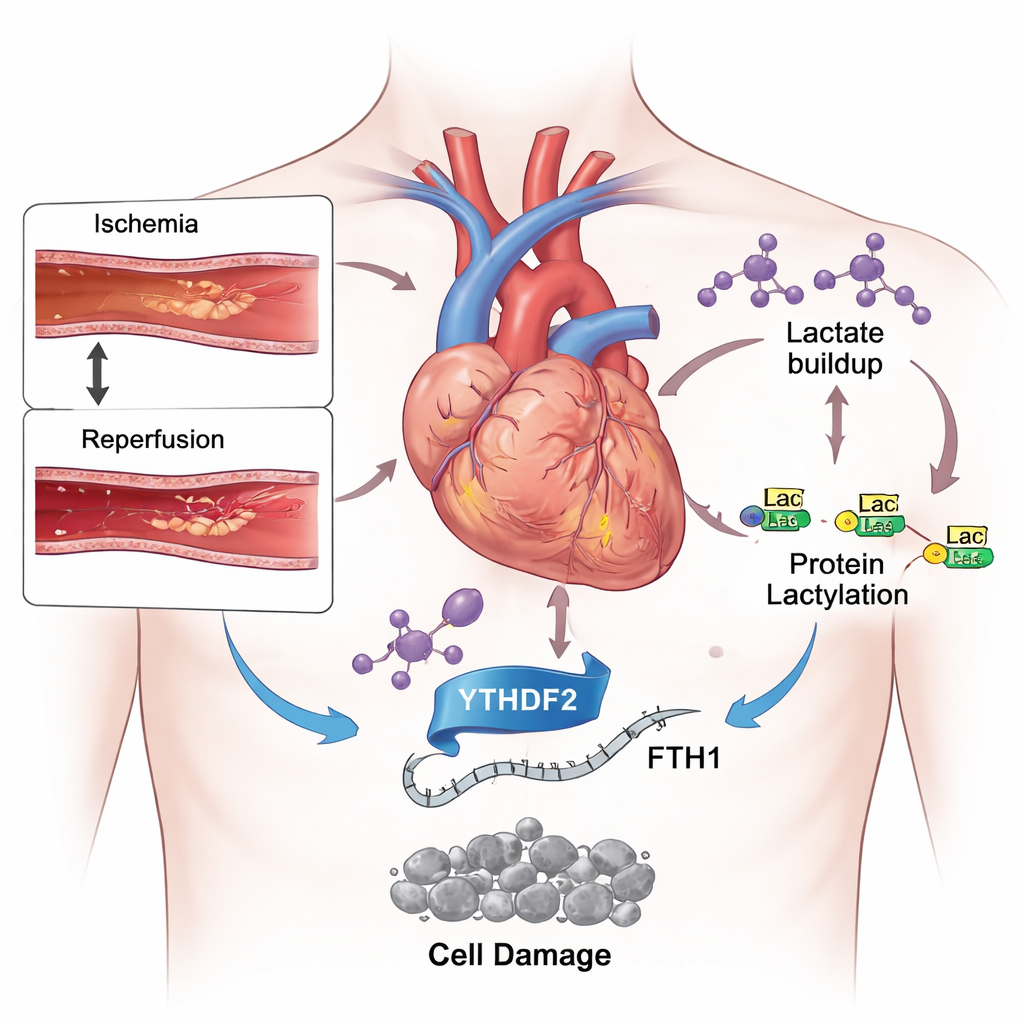
חרב פיפיות בטיפול בהתקף לב
הרפואה המודרנית השתפרה מאוד בפתיחה מהירה של עורקי קורונרי סתומים, ובכך מגבילה את הנזק ההתחלתי של התקף לב. עם זאת, מטופלים עדיין עלולים לאבד שטחים נרחבים של שריר הלב לאחר החזרת זרימת הדם. סיבה אחת היא שחזרת החמצן והמזון היוצרת סערה של מתח כימי בתוך תאי הלב. בין כמה סוגי מוות תאי המופעלים בהקשר זה, סוג חדש יחסית בשם פרופתוזיס (ferroptosis) משך תשומת לב. בניגוד לצורות מוכרות יותר כמו אפופטוזיס, פרופתוזיס תלוי בברזל ובהתהליכים חמצוניים מושתקים שתקפים שומנים בממברנות התאים, מה שעלול להחליש את הלב באופן קבוע.
כיצד חומצת החלב הופכת ליותר מסתם "שריפת שריר"
במהלך התקף לב, שריר הלב הרעב משנה את שימושו בדלק לעבר גליקוליזה, מערכת גיבוי שמפרקת סוכר במהירות אך מייצרת כמות גדולה של חומצת חלב. בעכברים שעברו חסימה קצרה ואחריה פתיחה של עורק לב, ובתאי לב בתרבית שנחשפו לחוסר חמצן ואז להחמצה מחדש, החוקרים מצאו עליות חדות ברמות חומצת החלב. בו זמנית גילו עלייה בתגי חמצון מסוג לקטילציה על חלבונים רבים ועל היסטונים, המרכיבים שמארגנים את ה-DNA. כאשר נתנו לבעלי החיים תרופה שעוצרת גליקוליזה ומפחיתה ייצור חומצת חלב, נזק הלב הצטמצם, סמני דם של נזק ירדו, והאיזון בין ברזל מזיק לנוגדי חמצון מגנים השתפר. ממצאים אלה מרמזים שחומצת חלב עודפת אינה רק תוצר לוואי של מתח אלא מנהלת פעילה של נזק.
מתג מולקולרי שמשחרר את הרסן מהברזל
בחפירה עמוקה יותר, הקבוצה התמקדה ב-YTHDF2, חלבון שקורא סימנים כימיים על RNA ומחליט כמה מהר מסרים מסוימים יהרסו. הם גילו שאיסכמיה–שחזור וחומצת חלב חיצונית הגבירו את רמות YTHDF2 והעלו לקטילציה סביב הגן המקודד אותו, מה שהגביר את ייצורו. אחד היעדים המרכזיים של YTHDF2 התגלה כבעל RNA של שרשרת הכבדת הפאטיטין 1 (FTH1), רכיב ליבה בכלוב האחסון של הברזל בתא. FTH1 בדרך כלל מאחסן ברזל בצורה בטוחה, ומונע ממנו להזין תגובות מזיקות. בתאי לב תחת לחץ, YTHDF2 התקשר חזק יותר ל-RNA של FTH1 והאיץ את מפורקתו, מה שהותיר את התאים עם פחות כלובי פריטין, יותר ברזל חופשי, מתח חמצוני גובר וסימנים קלאסיים לפרופתוזיס.
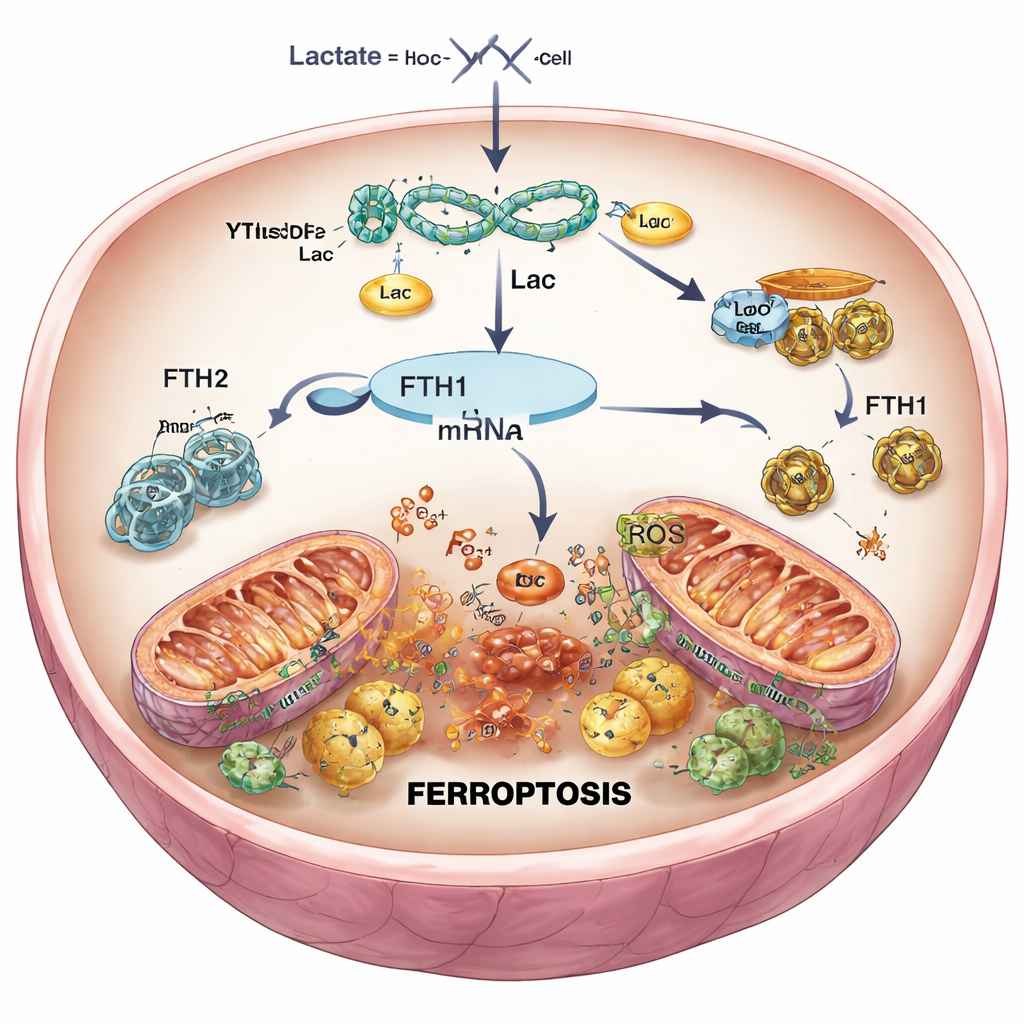
הנמכת אות המוות בתאי לב
לצורך בדיקת סיבה ותוצאה, החוקרים השתמשו בכלים גנטיים כדי לצמצם באופן סלקטיבי את YTHDF2 בתאי לב ובעכברים. כאשר YTHDF2 הושתק, רמות FTH1 חזרו, הברזל ורדיקלים חופשיים ירדו, המיטוכונדריה שמרה על צורה תקינה יותר, והשרידות הכוללת של התאים השתפרה לאחר שחזור מדומה של אספקת הדם. בעכברים, פחות YTHDF2 משמעותו צלקות התקף לב קטנות יותר ורקמה מראה בריאה יותר. יחד עם זאת, כאשר FTH1 הופחת במקביל, היתרונות הללו נעלמו ברובם: הברזל עלה שוב, הנזק החמצוני חזר, וגודל הנמק גדל. הדבר אישר ש-YTHDF2 מקדם פרופתוזיס בעיקר על ידי דיכוי FTH1, ומשחרר את השליטה על הברזל בתוך תאי הלב.
מה משמעות הדבר לטיפולי לב בעתיד
כאשר מרכיבים את החלקים, המחקר מתאר שרשרת אירועים חדשה: עורק שחסם ואז נפתח מייצר הצטברות חומצת חלב; חומצת החלב מעלה את YTHDF2 דרך לקטילציה; YTHDF2 הורס אז את הוראות ה-RNA לחלבון השומר על הברזל FTH1; והעומס שברזל שנוצר מפעיל פרופתוזיס ומעמיק את נזק הלב. עבור מטופלים, המסר מעודד: המסלול הזה מציע כמה נקודות חדשות להתערבות. תרופות שמגבילות איתות חומצת חלב מזיק, חוסמות את המודיפיקציה הספציפית של YTHDF2, או ששומרות על פעילות FTH1 עשויות להפוך את שחזור הזרימה לחירום לבטוח יותר ולהגן על יותר מרקמת לב. למרות שממצאים אלה עדיין זקוקים לאישור ברקמות אנושיות, הם פותחים נתיב מעניין לעבר טיפולים עדינים ויעילים יותר לניצולי התקפי לב.
ציטוט: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
מילות מפתח: התקף לב, חומצת חלב, מוות תאי מונע־ברזל, נזק איסכמיה־שחזור, הגנה על מיוציטים