Clear Sky Science · he
רשת עצבית גרפית מודעת פיזיקה כדי להעריך אפיניות קשירה מבוססת דוקינג עבור DYRK2 במחקרי שינוי שימוש בתרופות לאלצהיימר
מדוע זה חשוב עבור אלצהיימר
שכיחות מחלת האלצהיימר עולה ברחבי העולם, אך רוב התרופות הקיימות מרככות תסמינים בלבד במקום לעצור את המחלה. בדיקות תרופות במעבדה איטיות ויקרות, במיוחד עבור חלבונים מוחיים פחות מוכרים שעשויים להיות חשובים בזיכרון ובבריאות העצב. המחקר הזה חוקר קיצורי דרך חכם: שימוש במודל בינה מלאכותית המודע לחוקי הפיזיקה כדי לחזות עד כמה תרופות קיימות לאלצהיימר עשויות להיקשר לחלבון פחות נחקר בשם DYRK2, ובכך לפתוח מסלולים חדשים לטיפול.
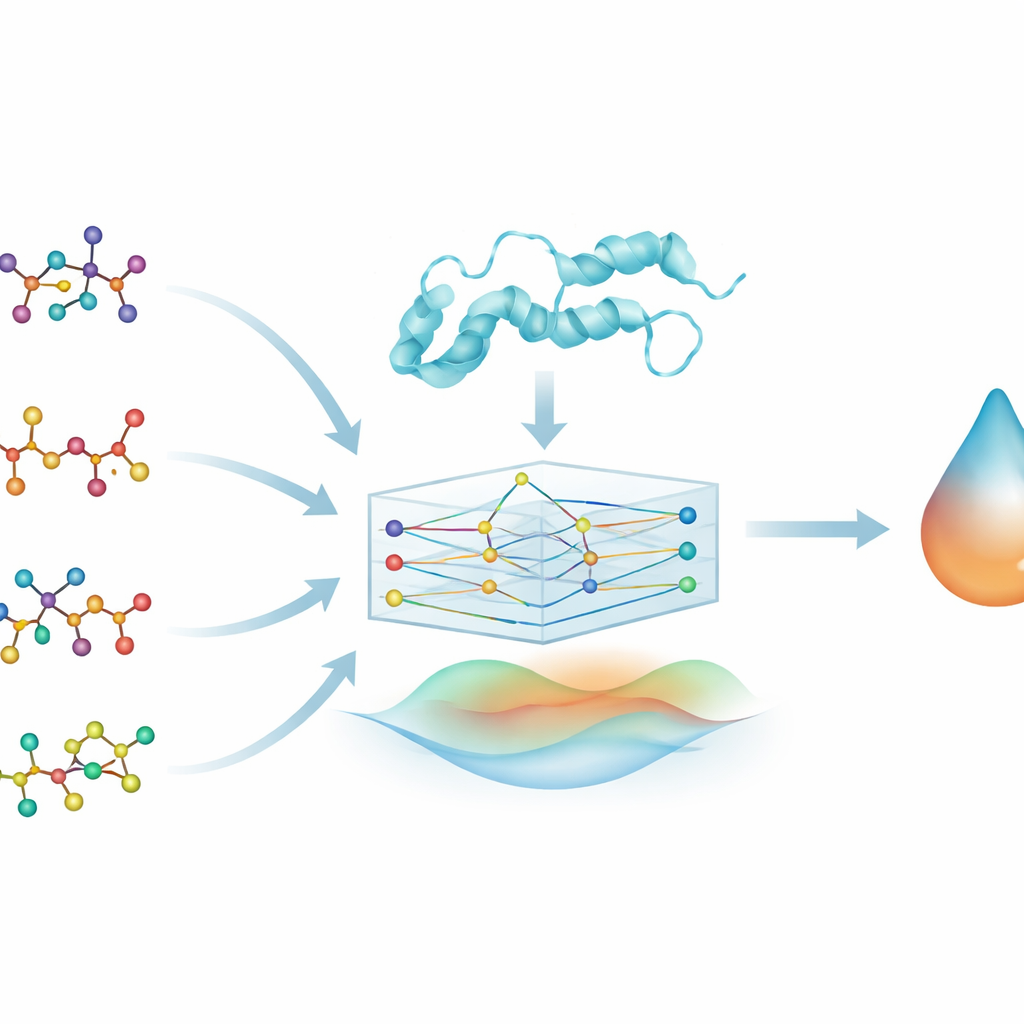
דרך חדשה להסתכל על תרופות ישנות
במקום לעצב תרכובות חדשות מאפס, החוקרים מתמקדים בשינוי שימוש בתרופות — מציאת שימושים חדשים לתרופות שכבר מאושרות וידועות כבטוחות יחסית. הם בוחנים ארבע תרופות מוכרות לאלצהיימר (brexpiprazole, donepezil, galantamine ו‑rivastigmine) ושואלים עד כמה כל אחת מהן עשויה להיקשר בחוזקה ל‑DYRK2, קינאזת חלבון המעורבת בצמיחה ותפקוד תאי עצב. DYRK2 נחקר בקושי במחלת האלצהיימר, אך ראיות מוקדמות מקשרות אותה לסינפסות, אקסונים וזיכרון, מה שהופך אותה למטרה מעניינת שיכולה להשלים את הטיפולים הקיימים.
הפיכת מולקולות לרשתות
כדי לחקור את יחסי התרופה–חלבון הללו, הצוות ממיר כל מולקולת תרופה לגרף: אטומים הופכים לנקודות וקשרים כימיים לקווים שמחברים ביניהם. הם עושים דבר דומה עבור חלבון DYRK2, ומייצגים את רצף חומצות האמינו שלו כשרשרת של יחידות מחוברות. סוג של מודל למידת מכונה הנקרא רשת עצבית גרפית (GNN) מתאים מטבעו לעבודה עם קלטים בצורת גרפים אלו, מעביר מידע לאורך הקישורים ולומד דפוסים של צורה וכימיה. זה מאפשר למודל, בשם PhysDual‑GCN, "לקרוא" גם את התרופה וגם את DYRK2 כרשתות שמתקשרות זו עם זו במקום כמחרוזות או רשימות תכונות פשוטות.
שילוב פיזיקה עם בינה מלאכותית
רוב כלים של למידה עמוקה בגילוי תרופות לומדים רק מתוך נתונים, מה שיכול להקשות על פענוח אופן פעולתם הפנימי. כאן המחברים משולבים בכוונה רעיונות פיזיקליים בסיסיים על אינטראקציות בין אטומים. לצד התכונות הלימודיות של הגרף, PhysDual‑GCN מחשב שני אפיקים אנרגטיים קלאסיים: אחד המתאר משיכה ודחייה חשמלית בין מטענים חלקיים, והשני המתאר את כוחות הוואן דר ואלס של דחיפה ומשיכה. אנרגיות מבוססות־פיזיקה אלו משולבות עם הייצוג הפנימי של ה‑GNN לפני שהמודל מפיק חיזוי עוצמת קשירה. למעשה, המודל מאומן לחקות את התנהגות תוכניות דוקינג סטנדרטיות — במיוחד AutoDock Vina וכלים קשורים — אך לבצע זאת מהר יותר ובבעקביות עם עקרונות פיזיקליים מוכרים.
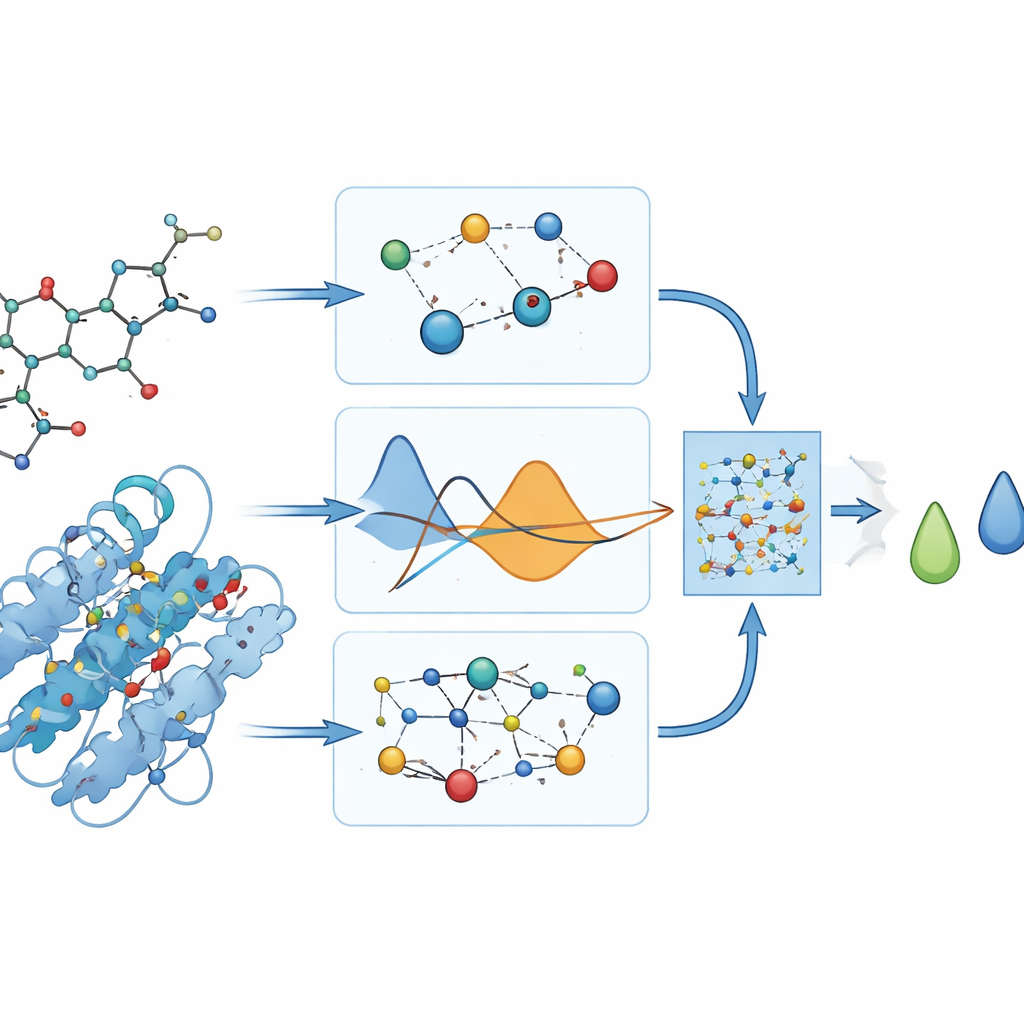
מה המודל בעצם חוזה
מכיוון שאין מדידות מעבדתיות הקיימות לעוצמת קשירה של תרופות אלו ל‑DYRK2, המחברים מסתמכים על תוכניות דוקינג כדי לספק "נקודות ייחוס" של ציוני קשירה ביחידות אנרגיה. הם נמנעים בקפידה מהזנת ציונים אלה לתהליך האימון, ומשתמשים בהם רק לאחר מכן כדי להעריך עד כמה PhysDual‑GCN למד היטב. עבור ארבע התרופות לאלצהיימר, המודל משכפל את ערכי הדוקינג עם שגיאות ממוצעות קטנות (בערך שליש קילוקלוריות לפרול) ומדורג נכון את התרכובות: donepezil ו‑brexpiprazole מופיעות ככאלו עם קשירה חזקה יותר, בעוד galantamine ו‑rivastigmine נראות חלשות יותר אך עדיין יציבות במידה סבירה. תוצאות אלה מראות כי ה‑GNN המודע לפיזיקה יכול להחליף באופן חישובי ריצות דוקינג איטיות יותר.
הבטחות ומגבלות הגישה
למרות המספרים המעודדים הללו, המחברים מדגישים שלמחקרם יש גבולות ברורים. נבדקו רק ארבע תרופות, וכל ההערכות מתבססות על תוכניות מחשב אחרות במקום ניסויים ביוכימיים אמיתיים. חלבון DYRK2 מוצג בעיקר כגרף חד־ממדי של רצף, ולא כמבנה תלת־ממדי מלא, כך שהמודל עדיין אינו יכול להתחשב בצורה המפורטת של כיסי קשירה. האנרגיות הפיזיקליות עצמן מפושטות, ומשתמשות בפרמטרי שדה כוח וחתכים סטנדרטיים. כתוצאה מכך, יש לראות בעבודה זו הוכחת קונספט: היא מראה כי רשתות עצביות גרפיות מודעות פיזיקה יכולות לעקוב מקרוב אחרי ציוני דוקינג קלאסיים בסביבת נתונים דלה, אך עדיין אינה מוכיחה שהחיזויים תואמים את המציאות במבחנה או במרפאה.
מה זה אומר למחקר אלצהיימר בעתיד
בעבור קהל לא‑מומחה, המסר המרכזי הוא כי אלגוריתמים חכמים ומודעים לפיזיקה עשויים לעזור למדענים לחקור מטרות אלצהיימר חדשות כמו DYRK2 הרבה יותר מהר משיטות מסורתיות לבדן. על ידי הדגשת donepezil ו‑brexpiprazole כמתמודדות מבטיחות לקשירת DYRK2 והצעת דרך שקופה להעריך תוצאות דוקינג, PhysDual‑GCN מספק נקודת פתיחה למחקרים מעבדתיים מעמיקים יותר. עם ספריות תרופות רחבות יותר, מידע חלבוני תלת־ממדי עשיר יותר ואימות ניסיוני, סוג כזה של מודל יכול להפוך לכלי מעשי לסינון טיפולים מועמדים ולהנחיית מאמצי שינוי שימוש בתרופות שמטרתם להאט או לשנות את מהלך מחלת האלצהיימר.
ציטוט: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
מילות מפתח: מחלת אלצהיימר, שינוי שימוש בתרופות, רשתות עצביות גרפיות, קשירת חלבון–ליגנד, קינאזת DYRK2