Clear Sky Science · he
המבנה הגבישי של ציסטטין B של Echinococcus multilocularis חושף מאפיין חדש בסטפינים הקלאסיים
מדוע נשק סודי של טפיל בכבד חשוב
אקינוקוקוז אלוואולרי הוא שם מסורבל לזיהום טפיל קטן שמתנהג רבות כמו גידול איטי בכבד. הוא לעתים קרובות קטלני, והתרופות הקיימות פועלות באופן לקוי ואולי גורמות לתופעות לוואי חמורות. המחקר הזה בוחן מולקולה מסוימת שמייצר הטפיל, חלבון בשם EmCystatin-B, כדי להבין כיצד הוא עשוי לסייע לתולעת להתחמק מההגנות שלנו — וכיצד בעתיד אפשר להפוך אותו למטרה לטיפולים חדשים.
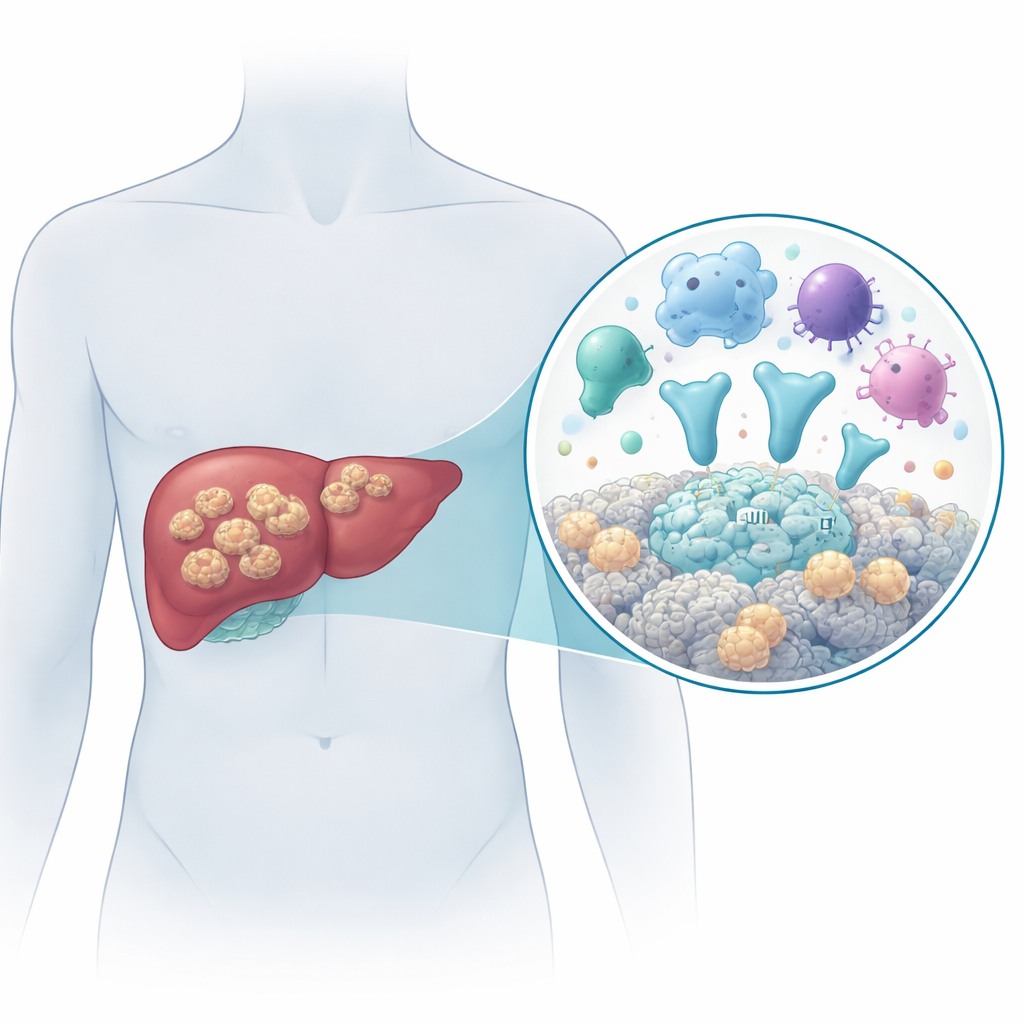
תולעת מסוכנת שגדלה כמו גידול
המחלה נגרמת על ידי השלב הלרווי של התולעת Echinococcus multilocularis. בני אדם נדבקים כאשר הם בולעים בטעות ביצי טפילים, למשל במזון או במים מזוהמים. ברגע שהן נכנסות לגוף, הזחלים מתיישבים בעיקר בכבד וגדלים כמספר שקיקים זעירים מלאי נוזלים החודרים לרקמה הסובבת, מתפשטים לאברים סמוכים כמו הטחול, ולעיתים מגיעים לאתרים מרוחקים כמו הריאות או המוח. ללא טיפול אפקטיבי, יותר מ‑9 מתוך 10 חולים מתים בתוך 10–15 שנים. ניתוח בשילוב עם טיפול אנטיפרזיטי ארוך טווח הוא כיום האפשרות הטובה ביותר, אך האבחון המוקדם קשה והתרופות אינן מרפאות באופן אמין. לכן חיוני להבין באיזה אופן הטפיל מתקשר עם גוף האדם ברמת המולקולות.
חלבון טפילי שמנטרל אנזמי חיתוך
בעלי חיים רבים, כולל בני אדם, מייצרים משפחה של חלבונים שנקראים ציסטטינים, המשמשים כמנעולים בטיחותיים על אנזמי עיכול עוצמתיים הידועים כציסטאינים־פרוטאזות. אנזימים אלה יכולים לפרק חלבונים אחרים והם חשובים בתהליכים כמו פירוק רכיבי תא ישנים והפעלת תגובות חיסוניות. הטפילים למדו לייצר חלבונים דמויי ציסטטין משלהם כדי להפריע לאנזימים ולמערכת החיסון של המאכסן. בעבודה זו זיהו החוקרים חלבון דמוי ציסטטין מ‑E. multilocularis וקראו לו EmCystatin-B. הם מצאו שהגן של EmCystatin-B פעיל הרבה יותר בראשי הזחלים הבוגרים של הטפיל (פרוטוסקולקסים) מאשר ברקמת הציסטה הסובבת, ושהחלבון נוכח בציטופלזמה ובגרעין של תאי הטפיל, במיוחד בתאים גרמינטיביים מתחלקים בעלי מאפיינים דמויי גזע. ניסויים במעבדה הראו כי EmCystatin-B יכול לחסום בעוצמה את פעילות הקטפסין B האנושי, שפרוטאזת ציסטאין חשובה המעורבת בחיסון ובחידוש רקמות.
צורה מוכרת עם טוויסט בלתי צפוי
כדי לראות בדיוק כיצד בנוי EmCystatin-B, הצוות הגביש את החלבון המטוהר והשתמש בקריסטלוגרפיית קרני־X כדי לפתור את המבנה התלת־ממדי שלו ברזולוציה קרובה לאטומית. בדומה לשאר בני משפחת הציסטטינים, כל יחידת EmCystatin-B בעלת צורה אופיינית: מקטע הליקלי מרכזי הנתמך במספר גדילים שטוחים הדומים לריבון, היוצרים מעין יתד שבאופן רגיל מתאימה לאתר הפעיל של פרוטאז. בהתבסס על הרצף והיעדר פפטיד אות מובהק להפרשה, EmCystatin-B משתייך לתת‑קבוצה של ציסטטינים הנקראת "סטפינים", שהם בדרך כלל חלבונים קטנים תוך‑תאיים שאינם מכילים קשרי דיסולפיד מייצבים. להפתעת החוקרים, המבנה חשף שלמרות שכל יחידת EmCystatin-B מציגה את הקיפול הצפוי, האופן שבו היחידות הללו מתאספות זו עם זו שונה וייחודי למין בהשוואה לאח הקאוצ'י האנושי, ציסטטין B.
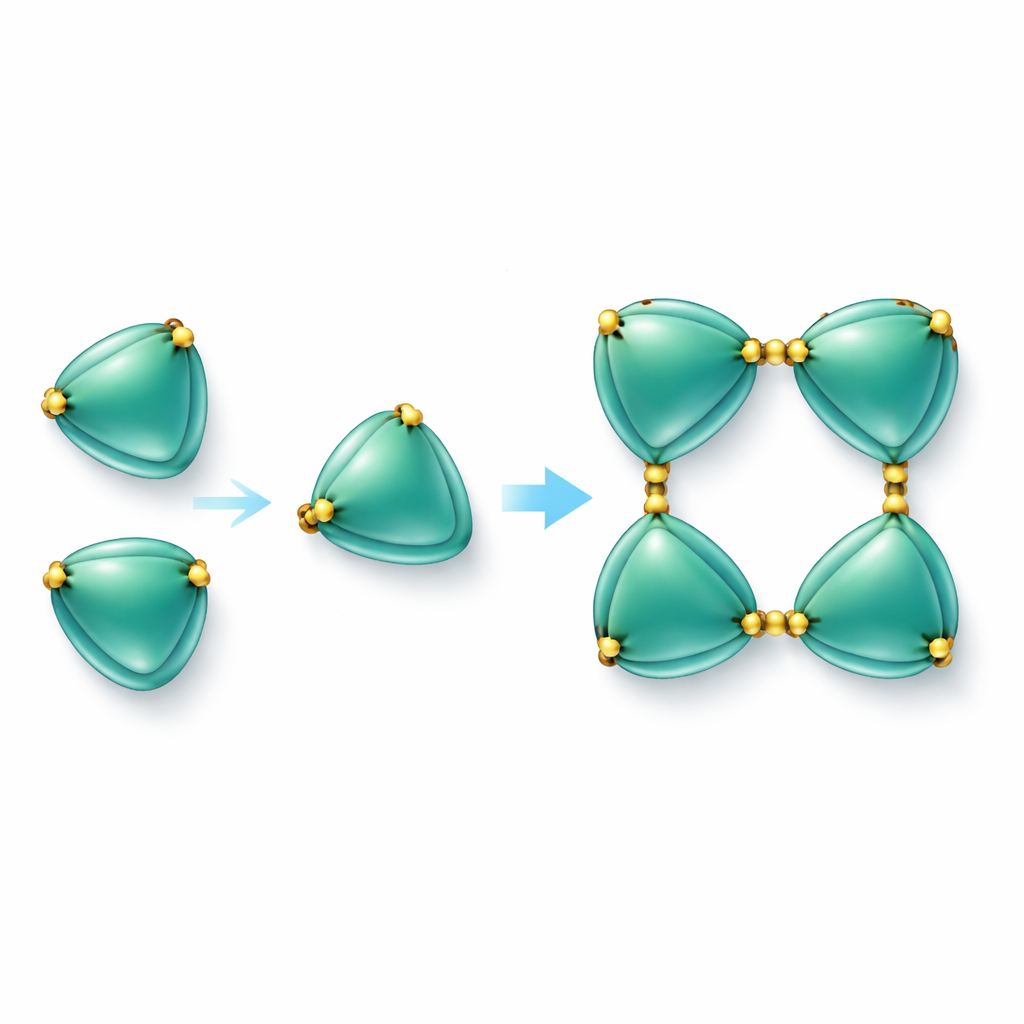
בנייה של שרשראות חלבון בקישורי גופרית
הממצא המפתיע ביותר היה שמולקולות EmCystatin-B אינן פשוט משוטטות כיחידות מבודדות. במקום זאת, הן יכולות להצטרף זו לזו בצורה שלב אחר שלב ליצירת דימרים (זוגות) ולאחר מכן טטראמרים (קבוצות של ארבע). שני מנגנונים שונים מסייעים ביצירת הדימרים הראשוניים. באחד מהם, מקטע של מולקולה אחת מתנדנד ומשלים את המבנה של שכנתה, תופעה המכונה החלפת דומיין. באחר, זוגות מולקולות מקושרות זו לזו על‑ידי גשרים דיסולפידיים — קישורים כימיים חזקים בין חומצות אמינו המכילות גופרית (ציסטאינים). ב‑EmCystatin-B, ציסטאין בעמדה 4 במולקולה אחת יוצר קשר עם ציסטאין בעמדה 76 במולקולה שותפה. ארבעה קישורים צולבים כאלה מייצבים את הטטראמר. שימוש במספר גשרים דיסולפיד בין מולקולות זה חדש לחלוטין בסטפינים הקלאסיים, שלרוב חסרים קישורים כאלה. כאשר החוקרים המירו את הציסטאינים הקריטיים הללו לחומצת אמינו אחרת, החלבון כבר לא הצליח להתאסף ביעילות למורכבות ברמות גבוהות ויכולת העיכוב שלו כלפי קטפסין B ירדה באופן חד.
מה המשמעות של זה למאבק בזיהום
ללא צורך במומחיות עמוקה, המסקנה היא שהטפיל פיתח גרסה מחושבת של משפחה חלבונית שכיחה, המשתמשת ב"יציקות" כימיות נוספות כדי לנעול יחד מספר יחידות מעכבות. הצורה האוליגומרית הזו נראית חשובה להסגת אנזים של המאכסן שהיה אחרת מסייע בשליטה על הזיהום. על ידי גילוי הארכיטקטורה המדויקת של EmCystatin-B והאסמבלות הייחודיות שלה המקושרות בדיסולפידים, המחקר מרחיב את הבנתנו כיצד חלבוני ציסטטין יכולים להיות מותאמים בין מינים. בטווח הארוך, תובנות אלה עשויות להנחות עיצוב של תרופות שיחסמו את השפעת ההגנה של EmCystatin-B על הטפיל או ידמו את תכונות הרגיעה החיסוניות שלו לטיפול במחלות דלקתיות.
ציטוט: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
מילות מפתח: אקינוקוקוז אלוואולרי, Echinococcus multilocularis, ציסטטין B, מבנה חלבון, מודולציה חיסונית