Clear Sky Science · he
TTF2 כביו-סמן אפשרי ומטרת אימונותרפיה באבחון ובתחזית של גליאומה
מדוע המחקר הזה על סרטן המוח חשוב
גידולים מוחיים הקרויים גליאומות הם בין הסרטן הקטלניים ביותר, ורוב המטופלים חיים רק מספר שנים לאחר האבחון. הרופאים זקוקים בדחיפות לשיטות טובות יותר לחיזוי מהלך המחלה ולמטרות חדשות לטיפול, ובמיוחד לטיפולים מודרניים מבוססי חיסון. מחקר זה מתמקד במולקולה שזוכה לתשומת לב מועטה, TTF2, ושואל שאלה פשוטה בעלת השלכות גדולות: האם רמות TTF2 בגידולים מוחיים יכולות לסייע לרופאים לאבחן גליאומה בצורה מדויקת יותר, לחזות הישרדות, ואפילו להנחות אימונותרפיות עתידיות?
אות חדש החבוי בגנים של הגידול
גליאומה אינה מחלה אחת אלא קבוצה מעורבת של גידולים מוחיים השונים במהירות גדילתם ובתגובתן לטיפול. הכלים הקיימים, כגון בדיקה מיקרוסקופית וכמה סמנים גנטיים, אינם מסבירים במלואן מדוע חלק מהמטופלים עושים טוב בעוד אחרים מדרדרים במהירות. החוקרים פנו למסדי נתונים גדולים ציבוריים על גנים של סרטן מארצות הברית וסין בחיפוש אחר רמזים מולקולריים נוספים. הם התמקדו ב‑TTF2, חלבון המשתתף בכיבוי פעילות גנים, שקושר לכמה סרטן אחרים אך לא נחקר לעומק בגליאומה.
TTF2 גבוה — סיכון גבוה יותר
בהשוואת אלפי דגימות מצאו החוקרים שרמות TTF2 גבוהות הרבה יותר ברקמות גליאומה מאשר במוח נורמלי. בתוך הגליאומות, גידולים עם רמות TTF2 הגבוהות ביותר נטו להיות יותר מתקדמים, להשתייך לתת‑סוגים אגרסיביים יותר ולהופיע בחולים מבוגרים יותר. במעקב אחר תוצאות המטופלים נצפתה דפוס ברור: אנשים שלגידוליהם היו רמות גבוהות של TTF2 בדרך כלל חיו פחות זמן בסה"כ וסבלו מהתקדמות מחלה תדירה יותר. גם לאחר התחשבות בסמנים חזקים קיימים כמו דרגת הגידול, מצב מוטציית IDH ושינוי כרומוזומלי הנקרא 1p/19q קודלישן, נותר TTF2 סימן אזהרה עצמאי. הקבוצה בנתה תרשים חיזוי שמשלב את TTF2 עם גורמים סטנדרטיים אלה, והתרשים התאמה לצפי הישרדות של שנה, שלוש וחמש שנים בשני מאגרים נפרדים של מטופלים.
רמזים משכונת הגידול
כדי להבין מדוע TTF2 עשוי להיות קשור לתוצאות גרועות, בחנו החוקרים אילו גנים נוספים עולים ויורדים יחד איתו ומהם התהליכים הביולוגיים שסטים אלה מייצגים. גידולים עם TTF2 גבוה הראו פעילות מוגברת במסלולים הקשורים לאיתות חיסוני, ייצור נוגדנים ותקשורת בין‑תאית, וכן במסלולים מוכרים של סרטן כגון PI3K–AKT. באמצעות כלים חישוביים שמסיקים את הרכב תאי החיסון לפי דפוסי ביטוי גנים, נתחו גם את מיקרו‑הסביבה של הגידול. גליאומות עשירות ב‑TTF2 היו גם עשירות בתאי חיסון מסוימים — תאי Th2 מסייעים, מאקרופאגים ונויטרופילים — שלרוב מקושרים לתגובה אנטי‑גידולית "מעוכבת", והיו בהן פחות תאים דנטריטים פלסמוציטואידים, היכולים לסייע בהפעלת חיסוניות חזקה יותר.
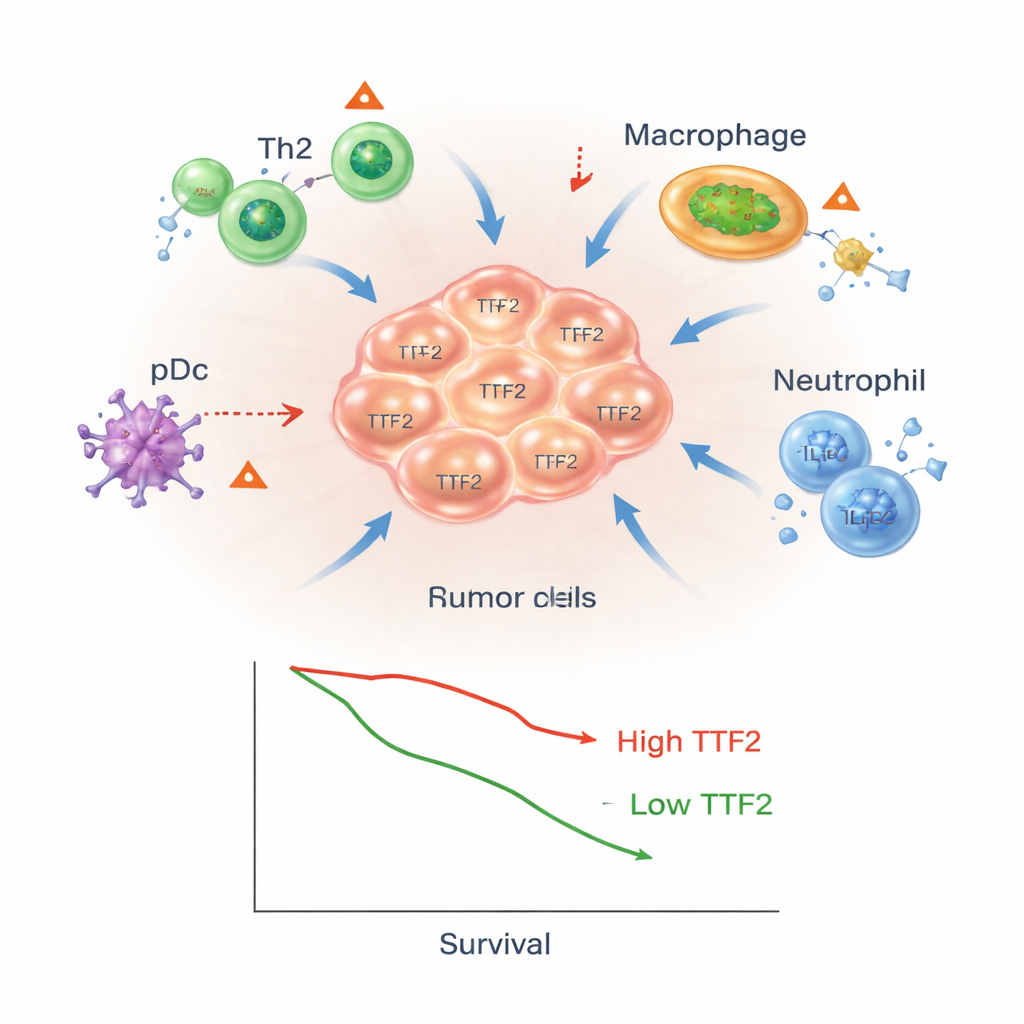
כיצד TTF2 עלול לסייע לגידולים להסתוות
ממצאים אלה מצביעים על כך ש‑TTF2 אינו רק סימן לגידולים מסוכנים; יתכן שהוא מעצב באופן פעיל מגן סביבם. המחברים מציעים כי באמצעות השפעה על כיבוי גנים, TTF2 עלול לשנות את רמות שליחים חיסוניים וכימוקינים מרכזיים — מולקולות שמושכות או דוחקות תאי חיסון. כך עשויה להתרחש פנייה של תאי T למצב דומיננטי של Th2 הפחות יעיל בהריגת תאי סרטן ולעידוד הצטברות של מאקרופאגים ונויטרופילים התומכים בגידול. אמנם רעיונות אלה נובעים מניתוח נתונים ולא ממניפולציה ישירה של TTF2 במעבדה, אך הם מציעים מודל שניתן לבדוק כיצד מולקולה זו עשויה לקדם הן גדילת גידול והן בריחה חיסונית.
מה משמעות הדבר עבור מטופלים
המחקר מסכם ש‑TTF2 מוגבר במידה רבה בגליאומות ושהרמות הגבוהות מקושרות בעקביות להישרדות גרועה ולמאפייני מחלה אגרסיביים יותר. עבור מטופלים הדבר פותח שתי אפשרויות מעודדות. ראשית, מדידת TTF2 בדגימות גידול יכולה לסייע לרופאים לחדד אבחון ולהתאים הערכות סיכון מעבר למה שמאפשרים הבדיקות הסטנדרטיות כיום. שנית, אם מחקרים עתידיים במעבדה יאשרו ש‑TTF2 מסייע לגידולים להתחמק ממערכת החיסון, תרופות החוסמות או מווסתות את TTF2 — או את מסלולי ההורדה שלו — עשויות להפוך לחלק משילובי טיפולים חדשים שישפרו את יעילות האימונותרפיה לחולי סרטן מוח הרסני זה.
ציטוט: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
מילות מפתח: גליאומה, TTF2, ביו-סמן לגידול מוחי, מיקרו‑סביבת הגידול החיסונית, מטרת אימונותרפיה