Clear Sky Science · he
טמפרטורות מעבר לזגוגית בנוזלים טהורים היוצרים זגוגית ותמיסות בינאריות
מדוע האטת נוזלים חשובה בחיי היומיום
חומרים רבים שאנו מסתמכים עליהם — ממסכי טלפונים חכמים ואריזות פלסטיק ועד מזון מיובש בקפיאה ותרופות — טכנית אינם מוצקים אמיתיים אלא זגוגיות: נוזלים שהתנועה בתוכם האטה עד כדי הופעה כקפואה. הבנת הנקודה שבה נוזל זורם הופך לזגוגית, ואיך טמפרטורת ה"הקפאה" הזו משתנה כאשר מערבבים חומרים, קריטית ליצירת מוצרים בטוחים, יציבים ובעלי חיי מדף ארוכים יותר. מאמר זה מציע שיטה חדשה לחשב ישירות את הטמפרטורה המרכזית הזו מתוך האופן שבו מולקולות בחומר נרפות ונעות, ומרחיב את הרעיון לתמיסות כגון תערובות סוכר ומערכות סוכר–מים המשמשות בתעשיית המזון והפרמצבטיקה.
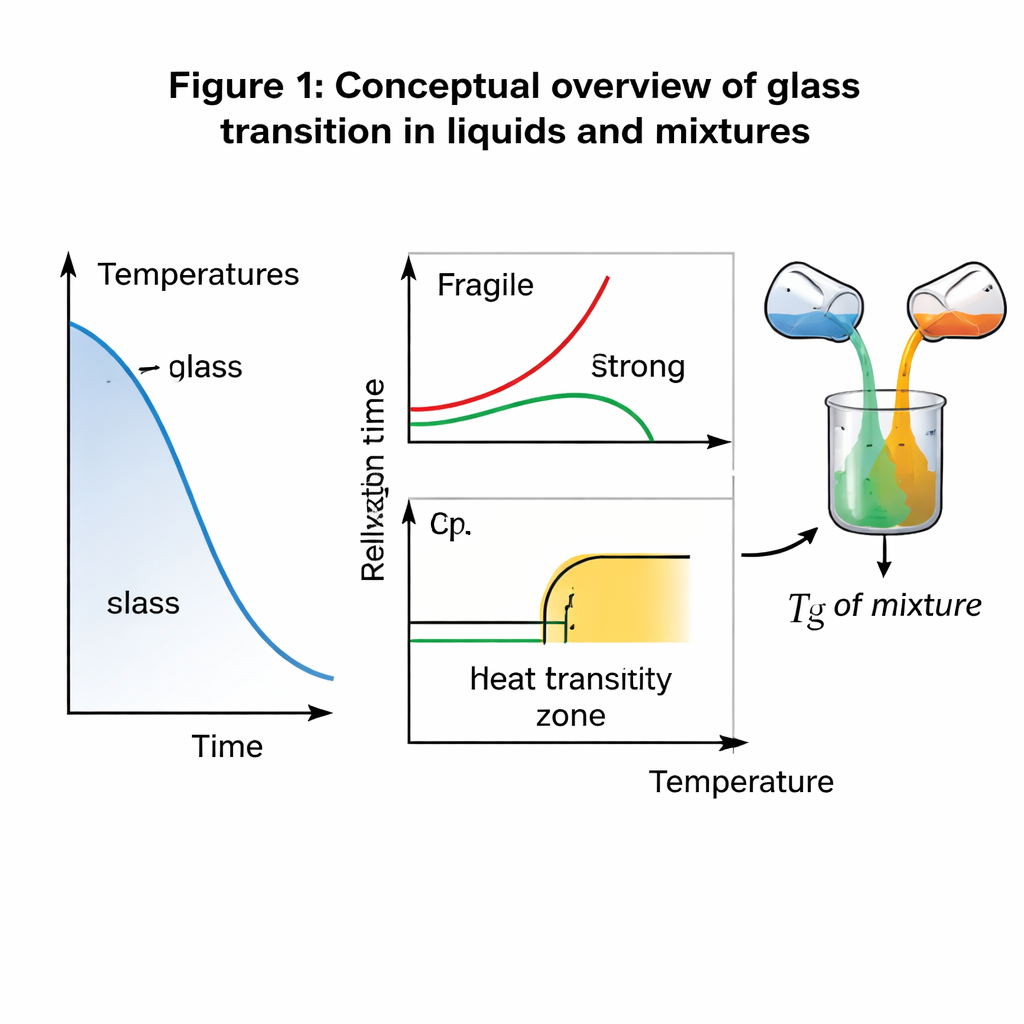
מממסות חדים להקפאות הדרגתיות
גבישים כמו קרח או מלח שולחני נמסים בטמפרטורה ברורה וחדה. זגוגיות מתנהגות אחרת. ככל שנוזל יוצר זגוגית מתקרר, מולקולותיו מאטות בהדרגה עד שבטמפרטורת מעבר הזגוגית (Tg) אינן יכולות להתארגן מהר מספיק כדי לעקוב אחר שינויי הטמפרטורה. החומר יוצא משיווי משקל ומתנהג כמוצק קשיח אך חסר סדר. באופן מסורתי תיארו מדענים את Tg בשתי דרכים: תרמודינמית, על ידי קפיצה בקיבול חום (כמה חום נדרש כדי לחמם את החומר), ודינמית, על ידי הזמן שנדרש להתארגנות מולקולרית. כלל אצבע נפוץ קובע ש‑Tg היא שם שבו זמן הרפיה מבני מגיע לכ־100–1000 שניות — אך זה בעיקר קונבנציה נוחה ולא עקרון מבוסס פיזיקלי חמור.
קשר נקי יותר בין זמן, טמפרטורה וקצב סריקה
המחברים בונים על רעיון קלאסי שמקשר ישירות את קצב שינוי הטמפרטורה בניסוי (קצב הסריקה) לאופן שבו זמן ההרפיה של החומר משתנה עם הטמפרטורה. במובן מה, מעבר הזגוגית מוגדר כנקודה שבה שנות הזמן של ההרפיה המבנית נעשות בדידות לשנות הזמן של סריקת הטמפרטורה. באמצעות מודלים סטנדרטיים המתארים כיצד זמן ההרפיה תלוּי בטמפרטורה, הם הופכים תנאי זה לנוסחאות מתמטיות מפורשות עבור Tg. נוסחאות אלה כוללות פונקציה מתמטית מיוחדת (פונקציית למברט W) שזמינה לאחרונה בתוכנות מדעיות רבות, מה שהופך פרוצדורה זו לפרקטית לפתרון אנליטי במקום להסתמך רק על התאמות נומריות.
מדוע שיעת הזגוגית "העולמית" הוא מיתוס
בעזרת המשוואות החדשות מראים המחברים כי זמן ההרפיה במעבר הזגוגית, שלרוב מניחים כערך "מעבדה" קבוע, תלוי במידה רבה בקצב הסריקה ובאנרגיית ההפעלה של החומר — מחסום האנרגיה האפקטיבי ששולט בתנועת המולקולות. עבור מהירות סריקה נתונה, חומרים עם אנרגיות הפעלה גבוהות יותר או עם ערכי Tg גבוהים יותר יכולים להציג זמני מעבר זגוגית השונים בסדרי גודל. סימולציות באמצעות מודלים נפוצים למעבר זגוגית מאשרות שלמרות שדרכים שונות להגדיר את Tg (למשל המקום שבו העקומת קיבול החום מתעקלת ביותר) אינן זהות, הן מניבות טמפרטורות דומות מאוד, ובאותו הזמן מדגימות בבירור שאין זמן הרפיה יחיד ואוניברסלי החולש על כל יוצרי הזגוגית.
כיצד תערובות של יוצרי זגוגית חולקות תכונות
חומרים בעולם האמיתי נדירים כשם שהם טהורים. בתערובות פולימריות, במוצרי מזון או בתרופות אמורפיות מערבבים שניים או יותר חומרים יוצרי זגוגית, ויצרנים זקוקים לדעת כיצד Tg של התערובת תלויה בהרכב. באופן אמפירי זאת מתוארת לעתים קרובות על ידי משוואת גורדון–טיילור, שמשתמשת בקבוע התאמה שמשמעותו הפיזיקלית לא ברורה ונדונה. המחברים מציעים חלופה דינמית: הם מניחים שפרמטרים קינטיים מרכזיים — כגון אנרגיות הפעלה אפקטיביות וכמויות קשורות — מערבבים באופן פשוט המבוסס על חלק מסת כל מרכיב. מתוך "חוקי ערבוב דינמיים אידיאליים" אלה הם גוזרים ביטוי כללי ל‑Tg של התערובת ומראים כי, במצב גבולי, הנוסחה המוכרת של גורדון–טיילור מופיעה באופן טבעי, כאשר קבוע ההתאמה נובע מקשר לאנרגיות ההפעלה או לפרגיליות של המרכיבים (מדד לרמת ההאטה היותר חדה של ההרפיה בקירור).
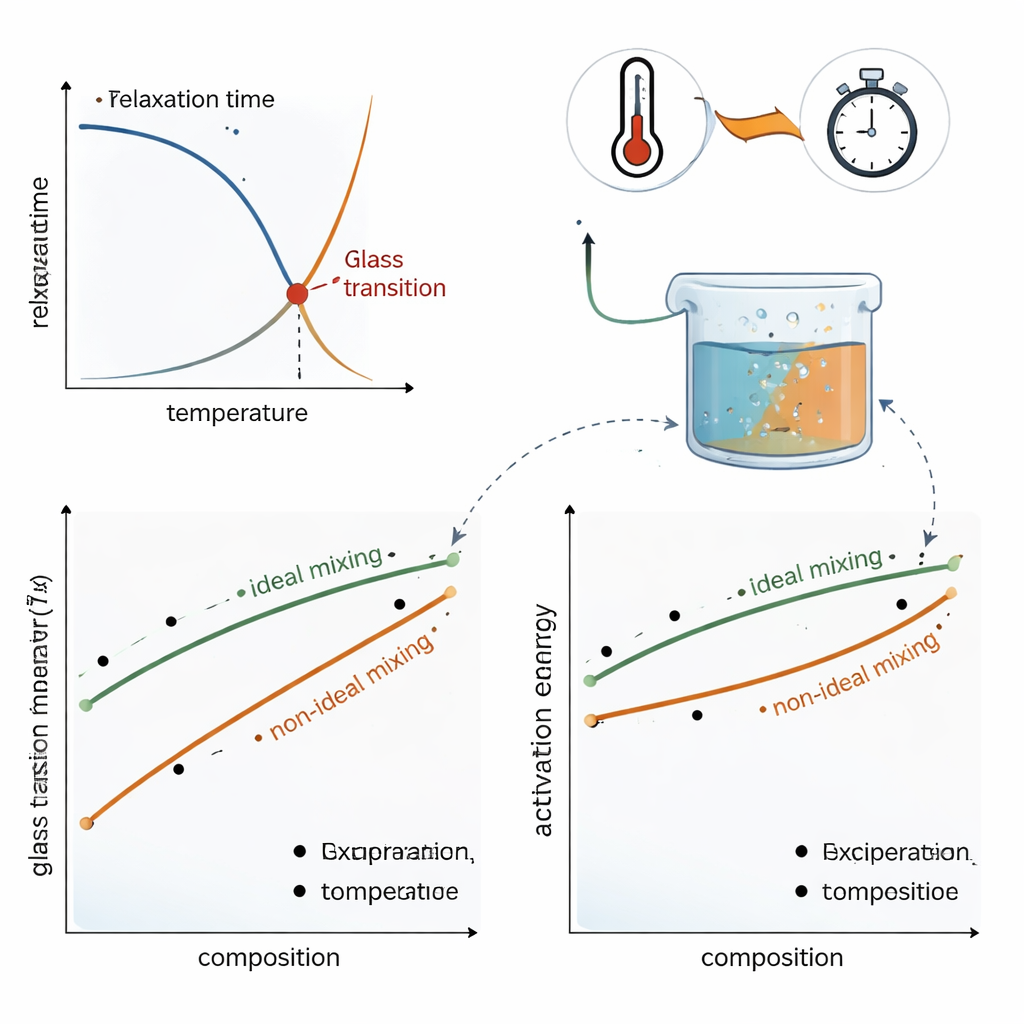
תערובות אמיתיות: מתי החוקים האידיאליים קורסים
בכדי לבחון את המסגרת שלהם, המחברים בודקים נתונים משתי מערכות בעלות חשיבות פרקטית. בתערובות הסוכרים סוכרוז וטרהלוז — נפוצות בשימור מזון וביולוגיה — Tg הנמדדת ואנרגיית ההפעלה משתנות רק במעט ממה שחוקי הערבוב הדינמיים האידיאליים מנבאים; התאמות מתונות לכללי הערבוב תופסות את העקומות הנצפות. בתערובת סוכרוז–מים, לעומת זאת, ההתנהגות חזקות אינה אידיאלית: הוספת אפילו כמות מועטה של מים מקטינה את אנרגיית ההפעלה ו‑Tg הרבה יותר ממה שממוצע פשוט היה מרמז. באמצעות כך שהופכים את חוקי הערבוב ללא־ליניאריים, המודל החדש יכול לשחזר את התלות המלאה והמעוקלת של Tg ואנרגיית ההפעלה בהרכב, ומשקף כיצד המים משחררים באופן דרמטי את הרשת המולקולרית של זגוגית הסוכר.
לקח למעצבים של חומרים ומוצרים יומיומיים
פשטות היא המסר: עבודה זו מראה שטמפרטורת המעבר שבה נוזל הופך לזגוגית אינה נובע משעון זמנים קסום יחיד, אלא מהאופן שבו התנועות הפנימיות של הנוזל מגיבות למהירות קירור או חימום נתונה. אותו היגיון קינטי מתרחב באופן טבעי לתערובות, שבהן יחס גורדון–טיילור המשמש לעתים קרובות מתגלה כמקרה פרטי של חוקים דינמיים כלליים יותר. למהנדסים המעצבג מסכי טלפון עמידים יותר, מזונות בעלי חיי מדף ארוכים יותר או תרופות יציבות יותר, מסגרת זו מציעה דרך מבוססת פיזיקלית יותר לחזות ולכוון את טמפרטורות מעבר הזגוגית בחומרים טהורים ובתערובות מורכבות כאחד.
ציטוט: Kocherbitov, V., Argatov, I. Glass transition temperatures of pure glass-forming liquids and binary mixtures. Sci Rep 16, 1317 (2026). https://doi.org/10.1038/s41598-026-35024-4
מילות מפתח: מעבר לזגוגית, זמן הרפיה, פרגיליות, תמיסות יוצרות זגוגית, משוואת גורדון–טיילור