Clear Sky Science · he
הבסיס המבני של דיוסגנין כאגוניסט הפוך של קולטן היתומים הקרוב לחומצת הרטינואית RORγ
למה תרכובת צמחית ומתג חיסוני חשובות
מצבים כרוניים רבים — ממחלות אוטואימוניות כמו טרשת נפוצה ופסוריאזיס ועד השמנת יתר וסוכרת מסוג 2 — נגרמים על ידי אותות חיסוניים פעילים מדי ואיתותים מטבוליים שמטושטשים. מדענים חיפשו זמן רב תרופות בטוחות יותר שיכולות לכוונן אותות אלה במדויק. המחקר הזה בוחן כיצד דיוסגנין, מולקולה טבעית המצויה בצמחים רפואיים ובפטריות יאם, נקשרת לחלבון המווסת את המערכת החיסונית RORγ ומעבירה אותו למצב פחות פעיל. הבנת האינטראקציה הזו ברזולוציה אטומית עשויה לפתוח דרך לטיפולים עדינים וממוקדים יותר המבוססים על שלד צמחי מוכר.
כפתור ראשי למערכת החיסון והמטבוליזם
RORγ הוא חלק ממשפחת גדולה של "קולטנים גרעיניים" — חלבונים בתאים שמדליקים או מכבים גנים בתגובה למולקולות קטנות. החלבון הזה הוא בקרה מרכזית על קבוצת תאי חיסון הנקראת Th17, שמייצרת את האות הדלקתי IL-17A וקושרה למחלות אוטואימוניות כגון טרשת נפוצה, פסוריאזיס, דלקת מפרקים ראומטואידית ומחלת קרוהן. RORγ משפיע גם על התפתחות תאי שומן ועל תגובת הגוף לאינסולין, ובכך מקשר אותו להשמנה ולסוכרת. בשל טווח ההשפעה הרחב הזה, RORγ הפך למטרה מבטיחה לתרופות, אך מולקולות סינתטיות רבות שנקשרו אליו נתקלו בבעיות של בטיחות, סלקטיביות או יעילות בבני אדם.
מרשם מסורתי מניב כיוון מבטיח
דיוסגנין היא מולקולה דמוית סטרואיד שמופקת מצמחים כולל מיני Dioscorea (יאם בר) וכמה עשבי מרפא מסורתיים. היא נחקרה בהקשרים של פעילות אנטי‑דלקתית, אנטי‑סרטן, אנטי‑סוכרת ויתרונות קרדיו‑וסקולריים במודלים של תאים ובעלי חיים. עבודות קודמות הציעו שדיוסגנין יכול להשפיע על מסלול RORα/γ ולהשפיע בדיכוי תגובות Th17 מזיקות, אך לא היה ברור האם הוא נוגע ישירות ל‑RORγ או כיצד הוא מעצב את התנהגות החלבון. כדי לענות על כך, החוקרים סרקו ספרייה של תרכובות טבעיות באמצעות בדיקת קשירה רגישה וזיהו את הדיוסגנין כקשור חזק לאזור קשירת הליגנד של RORγ.
כיצד דיוסגנין דוחף את RORγ להפוך
החוקרים בחנו כיצד דיוסגנין משפיע על יכולת RORγ לגייס חלבוני עזר שמגבירים (קואקטיבטורים) או מדכאים (קורפרסורים) את פעילות הביטוי הגנטי. מפתיע שדיוסגנין עודד את RORγ לקשור את שני סוגי השותפים, דפוס השונה משל אנטגוניסט טבעי ידוע בשם חומצת אורסולית. בבדיקות מדווחות מבוססות תאים שמעקבות אחרי עיתוק גנים, דיוסגנין הוריד בעקביות את הפעילות המנוהלת על ידי RORγ באופן תלוי מינון, בעוצמה בטווח של תת‑מיקרומולרי. התנהגות זו מתאימה לפרופיל של "אגוניסט הפוך": תרכובת שלא רק חוסמת פעילות בסיסית אלא גם דוחפת את הקולטן למצב כבוי, אפילו כשהוא היה צפוי להיות מופעל.
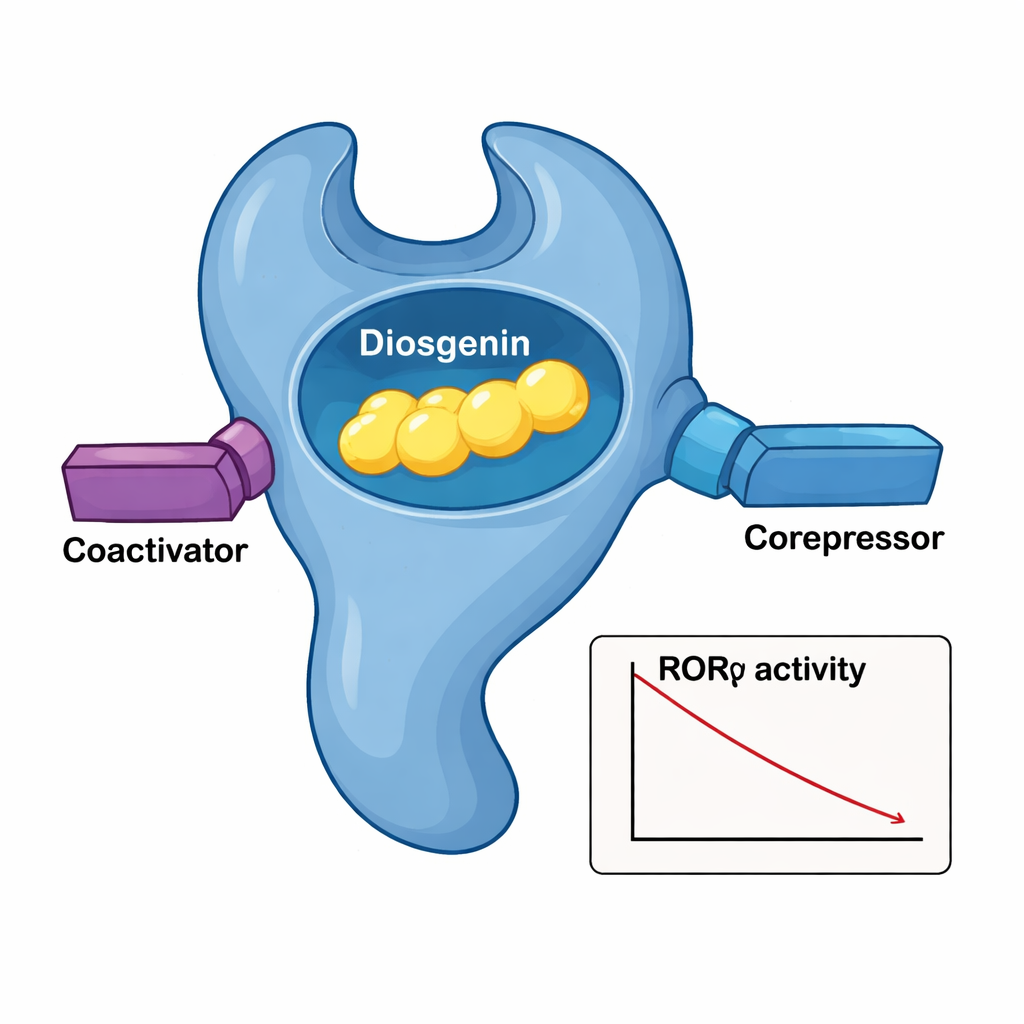
מבט מקרוב על לחיצת היד המולקולרית
כדי לראות בדיוק כיצד דיוסגנין משתלב ב‑RORγ, הקבוצה פתרה את המבנה הגבישי התלת‑ממדי של תחום קשירת הליגנד של החלבון עם דיוסגנין בתוך הכיס. הקולטן מתקפל לאשכול שכבות של הליקסים, ויוצר כיס שמחרז את גוף הסטראויד של דיוסגנין. רשת של מגעים הידרופוביים הדוקים ממספר חומצות אמינו פועלת כמו כפפה מותאמת סביב השלד המולקולרי, בעוד שקבוצת הידרוקסיל קריטית על הדיוסגנין יוצרת קשרים מימיים של מימן עם שתי שיירות ארגינין. כאשר שיירי הכיס שונו אחד‑אחד, יכולת הדיוסגנין לשתק את RORγ ירדה, מה שאישר את חשיבותם. השוואות מבניות עם קומפלקס RORγ–חומצת אורסולית הראו שדיוסגנין משמר את הליך הזנב המרכזי (AF‑2) במצב "כמראה פעיל" אפילו כשהוא עדיין דוחף את התעתוק הכולל למטה, מה שמסביר מדוע הוא יכול למשוך בו‑זמנית גם קואקטיבטורים וגם קורפרסורים.
ממבנה גבישי לתרופות עתידיות
התמונה המפורטת של אינטראקציית דיוסגנין–RORγ מדגישה שתי יתרונות בולטים לעיצוב תרופות. ראשית, כיס הקולטן מראה מספיק גמישות כדי לזהות צורות ליגן שונות, כלומר הכימאים יכולים לכוונן את שלד הדיוסגנין כדי לשפר סלקטיביות ל‑RORγ ולהפחית קשירה לא רצויה לקולטנים גרעיניים אחרים. שנית, המקור הטבעי של דיוסגנין והרעילות הנמוכה המוכרת שלו במודלים פרה‑קליניים הופכים אותו לנקודת פתיחה מושכת בהשוואה לחלק מהמולקולות הסינתטיות המלאות שנתקעו בניסויים. בפשטות, עבודה זו מראה כיצד מולקולה ממקור צמחי יכולה להיצמד למתג מרכזי בחיסון ובמטבוליזם ולדחוף אותו להפעלה הפוכה, ומספקת תבנית מבנית לפיתוח טיפולים בטוחים ויעילים יותר למחלות הקשורות ל‑RORγ.
ציטוט: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
מילות מפתח: ROR גאמה, דיוסגנין, מחלות אוטואימוניות, קולטן גרעיני, אגוניסט הפוך