Clear Sky Science · he
אופיינות טרנסקריפטומית של ספlicing אלטרנטיבי חריג בשרירי שלד של חולי סרקופניה
מדוע שרירים מזדקנים מאבדים כוח
סרקופניה — אובדן הדרגתי של מסת שריר וכוח עם הגיל — היא אחת הסיבות המרכזיות שהופכות פעולות יומיומיות לקשות עבור מבוגרים, מטיפוס במדרגות ועד נשיאת קניות. המחקר הזה חופר לתוך שריר מזדקן ברמת ה‑RNA, ההודעות שמדריכות את התאים אילו חלבונים לייצר. החוקרים מראים שבתוך סרקופניה רבות מההודעות האלה נחתכות ונדבקות מחדש בדרכים חריגות, מה שעלול להפריע לייצור אנרגיה בשריר ולהצביע על מטרות טיפול חדשות.
אובדן שריר ומערכת "עריכת" הגנים של הגוף
הגנים שלנו כתובים ב‑DNA, אבל התאים פועלים על פי העתקים של אותם גנים ב‑RNA. לפני שמשתמשים בהודעת RNA, התאים בדרך כלל גוזרים ומחברים אותה — בדומה לעריכה של סרט — כך שגן אחד יכול לייצר כמה גרסאות של חלבון. תהליך זה, שנקרא חיתוך אלטרנטיבי, פעיל במיוחד בשריר, שנדרש לחלבונים מורכבים ומדויקים להתכווצות, תיקון והסתגלות לאימון. כשחיתוך מטעה, עלולות להיווצר גרסאות חלבון לא תקינות או חשובים עלולים להיעלם, תורמים למחלות כמו דיסטрофיה השרירית וכמה הפרעות מוחיות. החוקרים חשבו ששכבה מוסווית דומה של עריכת RNA שגויה עשויה להניע את הסרקופניה.
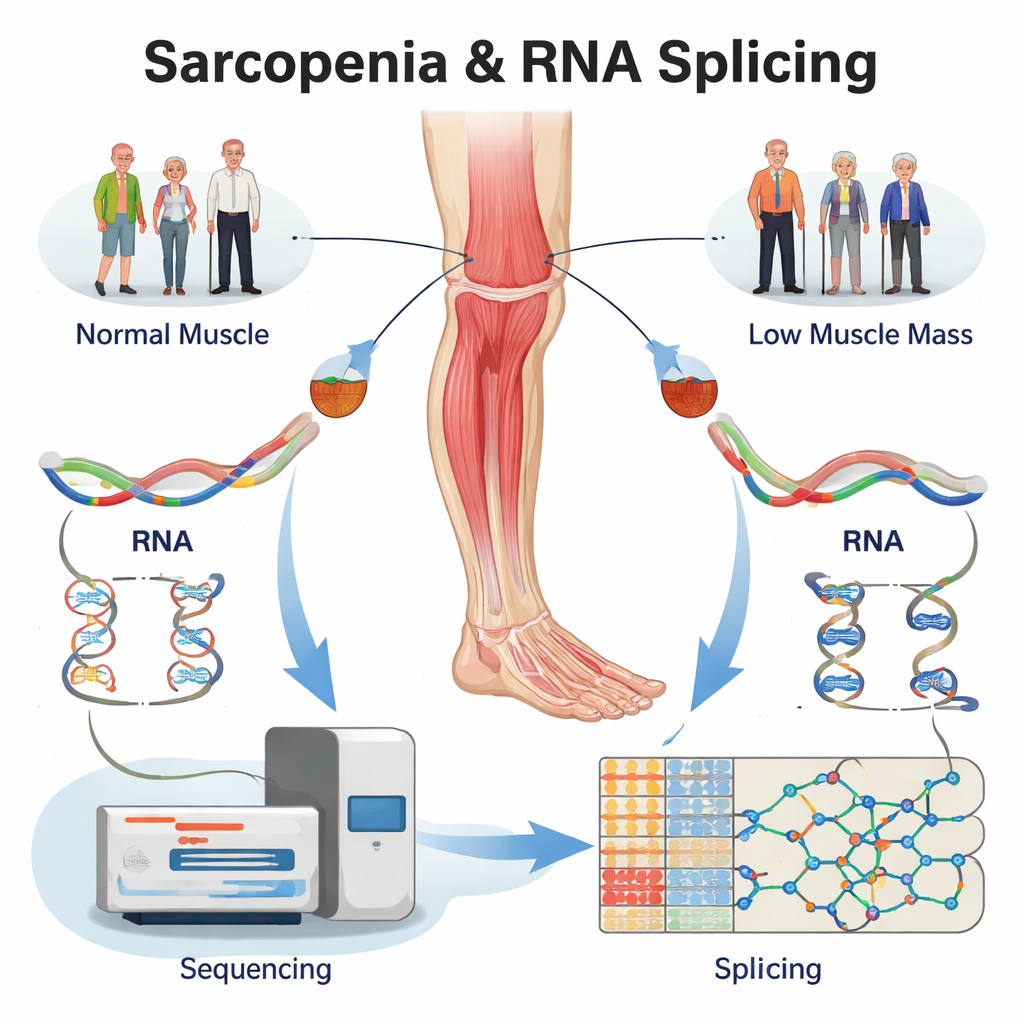
קריאה מחדש של נתונים קיימים כדי למצוא שגיאות RNA נסתרות
במקום לגייס מתנדבים חדשים, הצוות ניתח מחדש מאגר גדול של רצפי RNA מדגימות ביופסיה של שריר הירך האנושי. הדגימות הגיעו מארבע קבוצות: מבוגרים עם סרקופניה מלאה, אנשים עם ירידה במסת שריר בלבד, אנשים עם ירידה בכוח בלבד ובקרות בריאותיות תואמות גיל. באמצעות תוכנה מיוחדת הם אישרו תחילה שמאות גנים הועלו או הוסרו בביטוי בשרירים החולים. חשוב מכך, הם בחנו כיצד RNA של כל גן מחולק וחובר, ורשמו יותר מ‑5,000 שינויים בחיתוך אלטרנטיבי בשלוש קבוצות הבעיה בהשוואה לשריר בריא. שינויים אלה התרכזו בכמה סוגים בסיסיים — כגון דילוג על אקסון או בחירה באתר חיתוך חלופי — דפוסים שנודעו לשנות משמעותית את מבנה החלבון.
מפעלי האנרגיה ונתיבי "מד האנרגיה" של התא מופרעים
שינויים בחיתוך הופיעו בגנים שממוקמים בליבת הביולוגיה של השריר. רבים מהגנים המושפעים בונים חלקים במיטוכונדריה, מפעלי האנרגיה הזעירים שמניעים את התכווצות השריר. בשריר סרקופני, 16 גנים המעורבים בפוספורילציה חמצונית — התהליך שממירה חומרי תזונה לאנרגיה ניתנת לשימוש — הראו חיתוכים משתנים, במיוחד רכיבי קומפלקסי המיטוכונדריה שמנהלים העברת אלקטרונים ושאיבת פרוטונים. שינויים נוספים הופיעו בגנים שמייצרים או משתמשים ב‑NAD⁺, מולקולה מפתח לאנרגיה ותיקון תאיים. במקום שינויים בכמות בלבד, אנזימים חשובים כגון CD38, PARP2 וכמה סירטואינים ייצרו וריאנטים שונים של RNA, מה שמרמז שהאיזון בין ייצור לצריכה של NAD⁺ מעוות ברמת החיתוך. הגנים המושפעים התקבצו גם במסלולי איתות שריר ידועים, כולל AMPK ו‑FoxO, שמתפקדים כמדי דלק של התא ומגיבים ללחץ.
דפוסים משותפים בשלבים שונים — וגם בין מינים
באופן בולט, רבים מאותם גנים הראו שינויים בחיתוך לא רק אצל אנשים עם סרקופניה מלאה, אלא גם אצל אלה שהיו בעלי מסת שריר נמוכה בלבד או כוח נמוך בלבד. זה מציע שחיתוך חריג מתחיל מוקדם וחותך מעל פני הפנים הקליניות השונות של המחלה. כדי לבדוק האם שינויים אלה ניתנים לשחזור במודל חייתי, החוקרים גרמו לניוון שרירי בעכברים בעזרת הסטרואיד דקסמתזון, שיטה מקובלת לחקות חלק מהמאפיינים של סרקופניה. בעכברים התפתחו אחיזה חלשה וביצועים ירודים במבחני ריצה ושיווי משקל. כאשר הקבוצה רצפה את RNA של שרירי העכבר, הם שוב מצאו מאות גנים עם חיתוכים משתנים. בערך חמישית מהם חפפו עם גני הסרקופניה האנושיים, ורבים היו מעורבים בשליטה על שעתוק, מבנה כרומטין וחיתוך עצמם — מתגים ברמה גבוהה שיכולים לעצב מחדש את תפוקת החלבון כולה של התא.
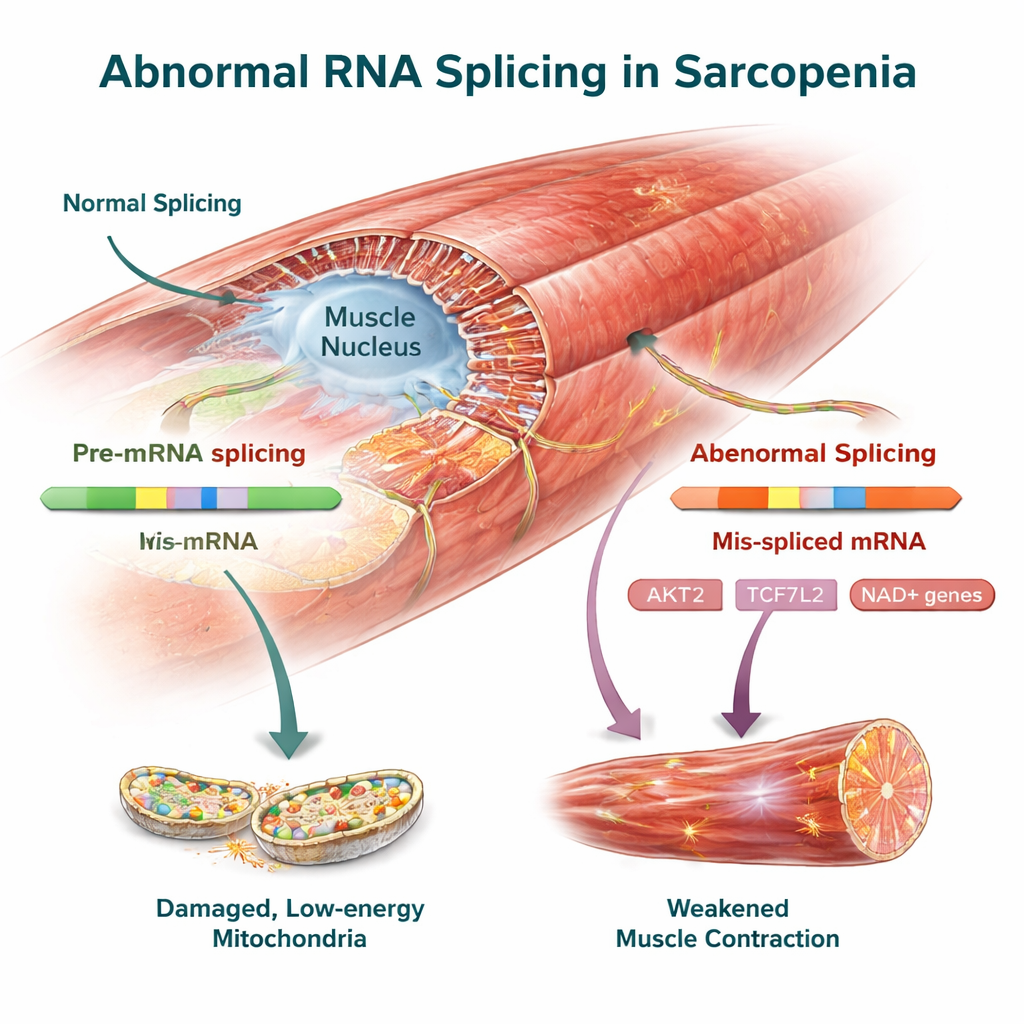
גני בקרה מרכזיים בשריר כמטרות טיפול פוטנציאליות
בין השינויים החוצים מינים היו מספר גנים שכבר קושרו לבריאות השריר. AKT2, רגולטור מרכזי של גדילה ובניית חלבון בשריר, הראה תזוזות חיתוך בולטות גם בבני אדם וגם בעכברים שעשויות להחליש את יכולתו לשמר מסת שריר. TCF7L2, חלק ממסלול האיתות Wnt, יחד עם FMNL2 ו‑USP40, המסייעים בארגון השלד הפנימי של השריר ובבקרת איכות החלבונים, גם הם נשאו וריאנטים RNA משונים. הצוות אישר את שינויים אלה בניסויים בשריר עכבר, מה שמחזק את המקרה שאלו מאפיינים אמיתיים של המחלה ולא ארטיפקטים של ניתוח נתונים.
מה המשמעות של זה למניעת שבירות
עבור קוראים שאינם מומחים, המסר הוא שסראקופניה אינה רק על "בלאי" של השרירים או על גנים שמדולקים או מכובים. היא כוללת גם עריכת יתרה של הודעות RNA שבונות ומתחזקות את המערכות של תאי השריר, במיוחד המערכות שמייצרות אנרגיה וחושבות לחץ. מאחר שניתן, בעקרון, לתקן חיתוך עם תרופות מבוססות RNA מתוכננות בדיוק, שגיאות החיתוך השמורות שנמצאו כאן — בפרט בגנים כמו AKT2 ו‑TCF7L2 — מציעות מערך חדש של קווים מנחים לפיתוח טיפולים שיסייעו לשרירים מזדקנים להישאר חזקים לאורך זמן רב יותר.
ציטוט: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
מילות מפתח: סרקופניה, הזדקנות שריר, חיתוך RNA, מיטוכונדריה, AKT2