Clear Sky Science · he
מודל פננומנולוגי של ייצוב טראנסטיירטין
מדוע זה חשוב עבור מטופלים ומשפחותיהם
אמילואידוזיס טראנסטיירטין היא מחלה חמורה שבה חלבון דם תקין, טראנסטיירטין (TTR), מתפרק וחלקיו עלולים להצטבר בצורה מזיקה בלב ובעצבים. תרופות חדשות כמו טפאמידיס ואקוראמידיס נועדו לשמור על החלבון בצורתו הבטוחה של רביעייה (טטראמר), והן כבר שיפרו תוצאות עבור אנשים רבים. עם זאת, רופאים מבחינים בהשפעה מבלבלת במטופלים המטופלים: רמות TTR בדם עולות ביותר מ-30%, ולא ברור מדוע. מאמר זה משתמש במודל מתמטי מצומצם כדי לחקור מה עשוי להתרחש בתוך הגוף ומה משמעות הדבר לגבי אופן הפעולה של התרופות הללו.
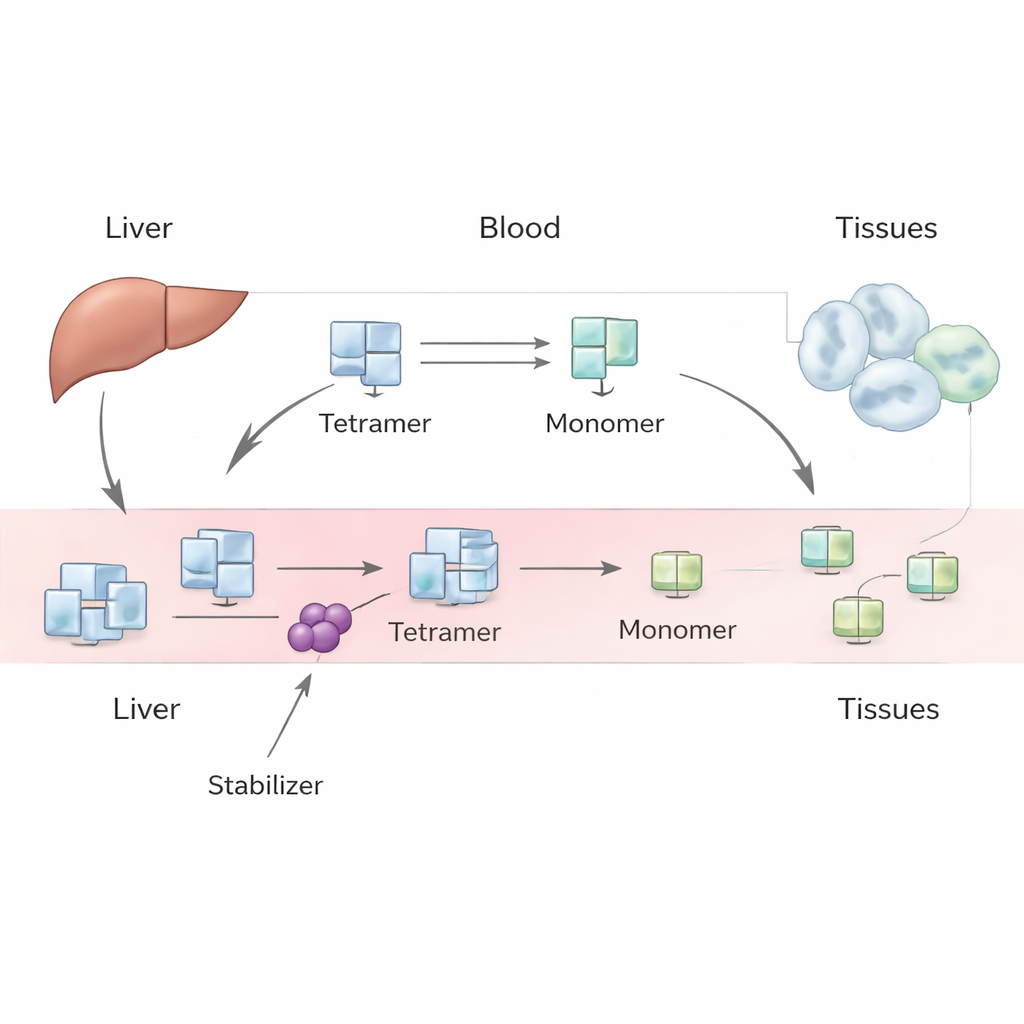
חלבון שיכול לעזור או להזיק
TTR מיוצר בעיקר בכבד ובדרך כלל נע בדם כעשירייה יציבה של ארבע יחידות זהות, המכונה טטראמר. הוא מעביר את הורמון התריס וויטמין A. בתנאים מסוימים, כולל הזדקנות או וריאנטים גנטיים תורשתיים, טטראמר זה עלול להתפרק ליחידות בודדות, מונומרים. מונומרים אלו עלולים לקמול בצורה שגויה ולהדבק זה לזה כשרשראות אמילואידיות, שפוגעות ברקמות ומובילות לאמילואידוזיס טראנסטיירטין של הלב (קרדיומיופתיה) או של העצבים (נוירופתיה). תרופות כמו טפאמידיס ואקוראמידיס נועדו לקשור את הטטראמר ולהקשות על פירוקו, ובכך להאט את התקדמות המחלה. אך כשהמטופלים מתחילים טיפול בתרופות אלו, מדידת רמות TTR בדם עולה באופן אמין, והעלייה הזו גדולה יותר ממה שניסויים מעבדתיים פשוטים היו חוזים.
בניית תמונה פשוטה של מערכת מורכבת
המחברים מתמודדים עם התעלומה הזאת באמצעות מודל פננומנולוגי — כזה שמתמקד בהתנהגות כללית ניתנת לצפייה במקום בכל פרט מיקרוסקופי. במסגרת שלהם, הכבד מייצר טטראמרים של TTR בקצב יציב, שמכנסים למחזור הדם. ברגע במחזור, טטראמרים יכולים להיפרד למונומרים ולהתרכיב מחדש, ושניהם — טטראמרים ומונומרים — יכולים להיות מוסרים מהדם באמצעות קליטה לרקמות ופירוק. על ידי כתיבת זוג משוואות מאזן-מס לטטראמרים ולמונומרים, הצוות חוקר תרחישים שונים: מצב שבו המונומרים ברובם מצטרפים חזרה לטטראמרים, מצב שבו הם מוסרים במהירות, ומקרה ביניים שבו שני התהליכים חשובים. הם משתמשים במחקרי טרייסר אנושיים היסטוריים ובנתוני מעבדה מודרניים להערכת כמויות מרכזיות, כמו קצב ניקוי הטטראמרים, קצב פירוקם וכמה החומרים מאטים את הפירוק הזה.
מדוע יציבות הטטראמר לבדה אינה מספיקה
מצוידים בהערכות אלו, החוקרים שואלים שאלת מפתח: אם תרופה תוכל למנוע באופן מושלם את פירוק הטטראמרים, כמה תעלה רמת ה-TTR בדם? בכל התרחישים הסבירים, התשובה צנועה — בדרך כלל סדר גודל של עד כ-15% במקרה של ערכי פרמטר טיפוסיים, ולעתים פחות, תלוי כיצד מתייחסים למונומרים. זה רחוק מהעלייה של מעל 30% שנצפתה במטופלים המטופלים. החוסר בהתאמה נותר גם אם מאפשרים אי ודאות רחבה בפרמטרים הידועים. המודל מציע אפוא כי האטת פירוק הטטראמרים לבדה אינה מסבירה את ההשפעה הקלינית המלאה. תהליכים נוספים הקובעים כמה מהר TTR מיוצר, נלקח על ידי תאים או מפורק חייבים גם הם להשתנות בנוכחות תרופות מייצבות.
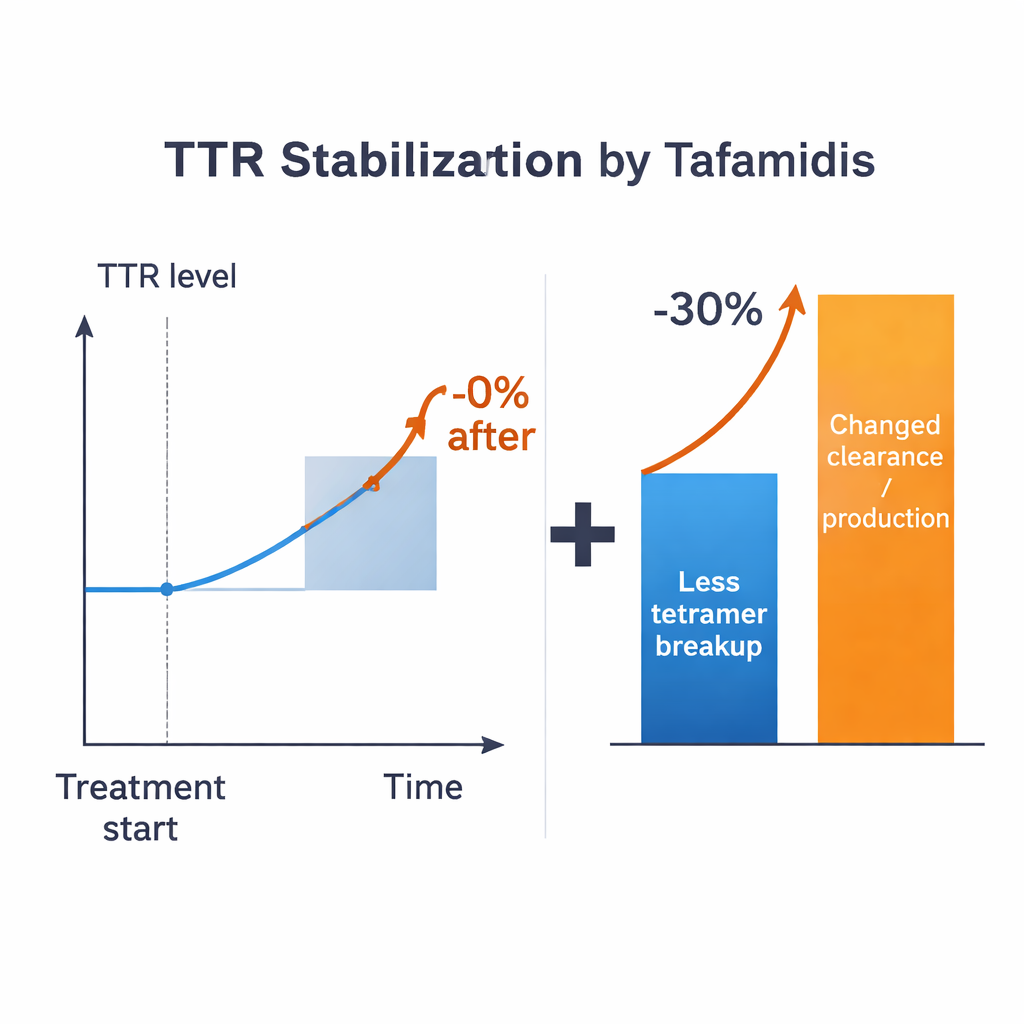
רמזים מרמות תרופה וניסויים חכמים
כדי לקשר בין החשיפה לתרופה להתנהגות ה-TTR, המחברים משלבים מודל פרמקוקינטי בסיסי של טפאמידיס (כיצד התרופה נעה בגוף לאורך זמן) עם בדיקות ייחודיות של "החלפת תת-יחידות". בניסויים אלה מערבבים טטראמרים של TTR מסומנים ונטולי תווית בפלזמה אנושית, והחלפת התת-יחידות בהדרגה חושפת כל כמה זמן טטראמרים מתפרקים. מדידת התהליך ברמות תרופה שונות מניבה קישור ישיר ומבוסס נתונים בין רמת הטפאמידיס ליציבות הטטראמר היעילה, מבלי צורך לדעת כמה תרופה קשורה לאלבומין או להורמון התריס. קישור פננומנולוגי זה מוזן למודל ומקצר בצורה נקייה הרבה מהלא-ידועים הביוכימיים. אך גם עם היתרון הזה, החישובים עדיין מגבילים את העלייה הצפויה ב-TTR לכמעט חצי מהעלייה הנצפית קלינית, ומחזקים את הרעיון ששינויים בניקוי, בקליטה פנימית, בפירוק או אפילו בסינתזה חייבים להיות חלק מהסיפור.
מה משמעות הדבר להמשך הדרך
לקהל שאינו מומחה, המסר המרכזי הוא שתרופות המייצבות האלה ככל הנראה עושות יותר מאשר רק "להדביק" טטראמרים של TTR זה לזה. סביר שהן גם משפיעות על אופן ייצורו, הסרתו או מחזורו של החלבון בגוף. המחברים טוענים שמודלים פשוטים ושקופים כשלם חזקים מכיוון שהם חושפים פערים כאלה בהבנה שלנו ומצביעים על ניסויים קונקרטיים — למשל מדידה ישירה של מהירות ניקוי המונומרים, כמה מהר צורות שונות של TTR נלקחות על ידי תאים, או האם TTR הקשור לתרופה מטופל אחרת מאשר החלבון החופשי. תשובות טובות יותר לשאלות אלו לא רק ישפרו את הטיפול באמילואידוזיס טראנסטיירטין אלא עשויות גם לחשוף כללים כלליים על מחלות אחרות שבהן חלבונים נורמליים הופכים למצבורי נזק.
ציטוט: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
מילות מפתח: אמילואידוזיס טראנסטיירטין, ייצוב חלבון, טפאמידיס, דוגמנות פרמקוקינטית, מחלות אמילואיד