Clear Sky Science · he
גישת למידה מצטברת לסגמנטציה סמנטית של תמונות היסטולוגיה של העור
מדוע חשוב ללמד מחשבים לקרוא דגימות עור
סרטן העור הוא אחד מסוגי הסרטן הנפוצים ביותר בעולם, וברופאים נעזרים לעתים קרובות בפרוסות דקות של רקמה הנבחנות במיקרוסקופ כדי להעריך את חומרת הגידול וכיצד לטפל בו. קריאת השקופיות האלה היא עבודה איטית ותובענית שיכולה להשתנות ממומחה למומחה. המחקר הזה בוחן כיצד לבנות מערכות מחשב שלומדות לזהות רקמות וסוגי סרטן שונים בתמונות מיקרוסקופיות של העור, וחשוב לא פחות — ממשיכות להשתפר עם הזמן כאשר סוגי תמונות חדשים מתווספים, בדומה ללומד אנושי שממשיך לצבור ניסיון לאורך הקריירה.
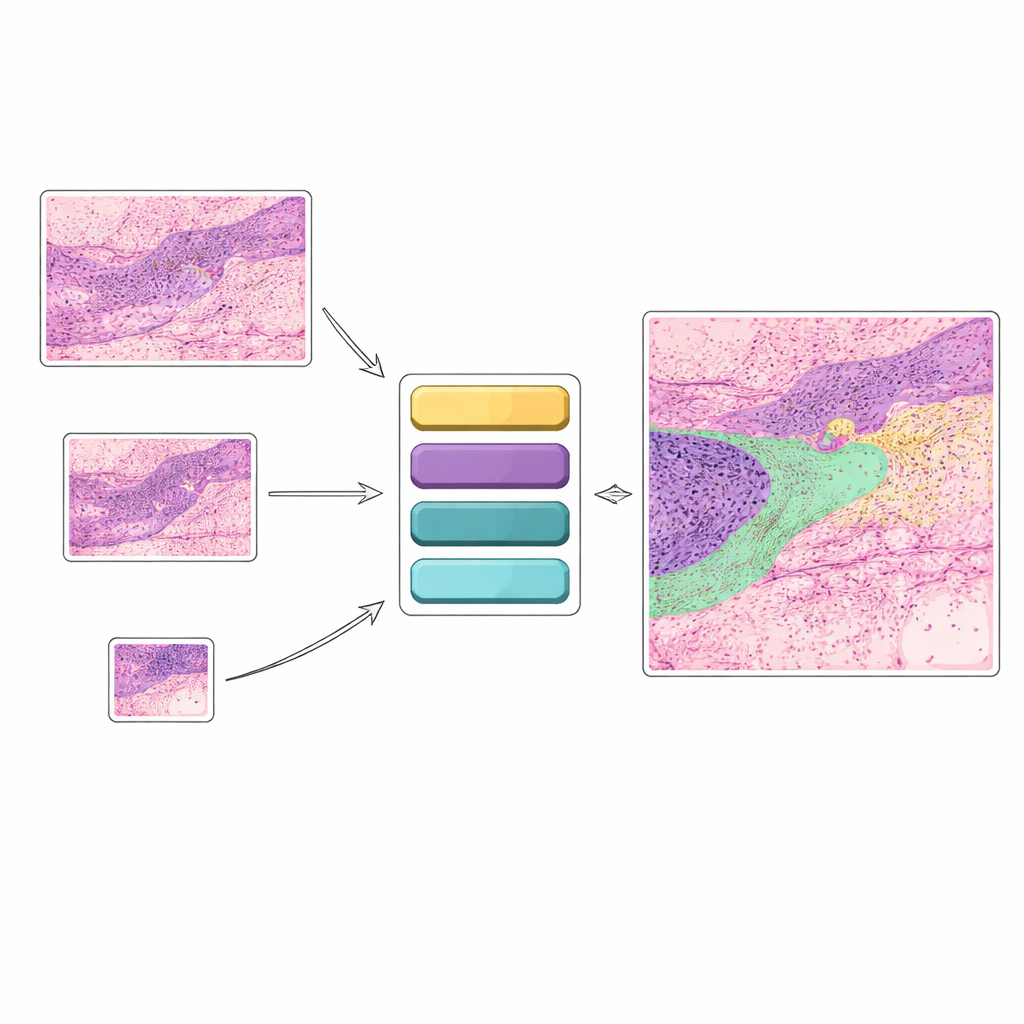
ממענה כן–לא פשוט למפות רקמות מפורטת
כלים רבים המבוססים על בינה מלאכותית לזיהוי סרטן העור מסתכלים על תמונה ועונים על שאלה צרה כמו "סרטן" או "אין סרטן". בעוד שגישה כזו שימושית, היא אינה לוכדת את העושר והפרטים שהפתולוגים רואים. בפועל, רופאים מתעניינים במספר רב של מבנים בו־זמנית: סוגי סרטן שונים, שכבות עור תקינות, זקיקי שיער, בלוטות, אזורים דלקתיים ועוד. מחקר זה מתמקד במקום זאת ב'סגמנטציה סמנטית', שבה כל פיקסל בתמונת ההיסטולוגיה מועדף לאחת מתריסר קטגוריות רקמה. זה מייצר מפה מקודדת בצבעים שמראה בדיוק היכן נמצאים הגידולים והמרקמות התקינות, ומספק הנחיה ברורה יותר לאבחון ותכנון טיפול.
מדוע מערכות חכמות נוכחיות מתקשות להסתגל
מודלים חזקים של למידה עמוקה כיום מניחים בדרך כלל שכל נתוני האימון זמינים בבת אחת. לאחר האימון הם נוטים "להיאחז" בידע שלהם. אם מאוחר יותר מתווספים נתונים חדשים עם מאפיינים שונים — למשל תמונות במגדיל שונה — האפשרות הבטוחה ביותר היא לעיתים קרובות לאמן את כל המודל מחדש מאפס. זה יקר ואיטי, ומהווה בעיה גדולה יותר: הוספת מידע חדש עלולה לגרום ל'שכחה קטסטרופלית', שבה הביצועים על משימות קודמות מתדרדרים בשקט. בסביבות קליניות, לעומת זאת, הנתונים משתנים כל הזמן כאשר הסורקים מתעדכנים, הגדרות הדימות משתנות ובתי חולים אוספים דגימות מסוגים חדשים. כלי בינה מלאכותית שאינו מסוגל לספוג שינויים אלה בצורה חלקה קשה לאמץ בשגרה הקלינית.
אסטרטגיית למידה מדורגת בהשראת אופן הלמידה של בני אדם
המחברים בונים על ארכיטקטורת הטרנספורמר חזותי מודרנית בשם SegFormer והופכים אותה למערכת "למידה מצטברת" עבור סרטן עור שאינו מלנומה. במקום לראות את כל הנתונים בבת אחת, המודל מאומן בשלבים באמצעות שקופיות היסטולוגיה ממאגר ציבורי של אוניברסיטת קוינסלנד. בתחילה הוא לומד מתמונות במגדיל גבוה (10×), שבהן הפרטים הקטנים ברורים. מאוחר יותר מתווספות תמונות ב־5× ואז ב־2× מגדיל, בעוד ששיעור מסוים מהנתונים המפורטים המקוריים נשמר בתמהיל. פונקציות אובדן מיוחדות מסייעות לגרסה החדשה של המודל לשמר את מה שלמד קודם על דפוסי רקמה, גם כשהוא מסתגל לתצפיות גסות יותר ומרוחקות. ה'למידה ללא שכחה' הזאת מונחית על ידי טכניקה הנקראת הידרשת ידע (knowledge distillation), שבה מודל קודם משמש כמורה למודל החדש, וכן באמצעות מונח של הידרשת הדדית שמכוון את הייצוגים הישנים והחדשים להישאר בהרמוניה.
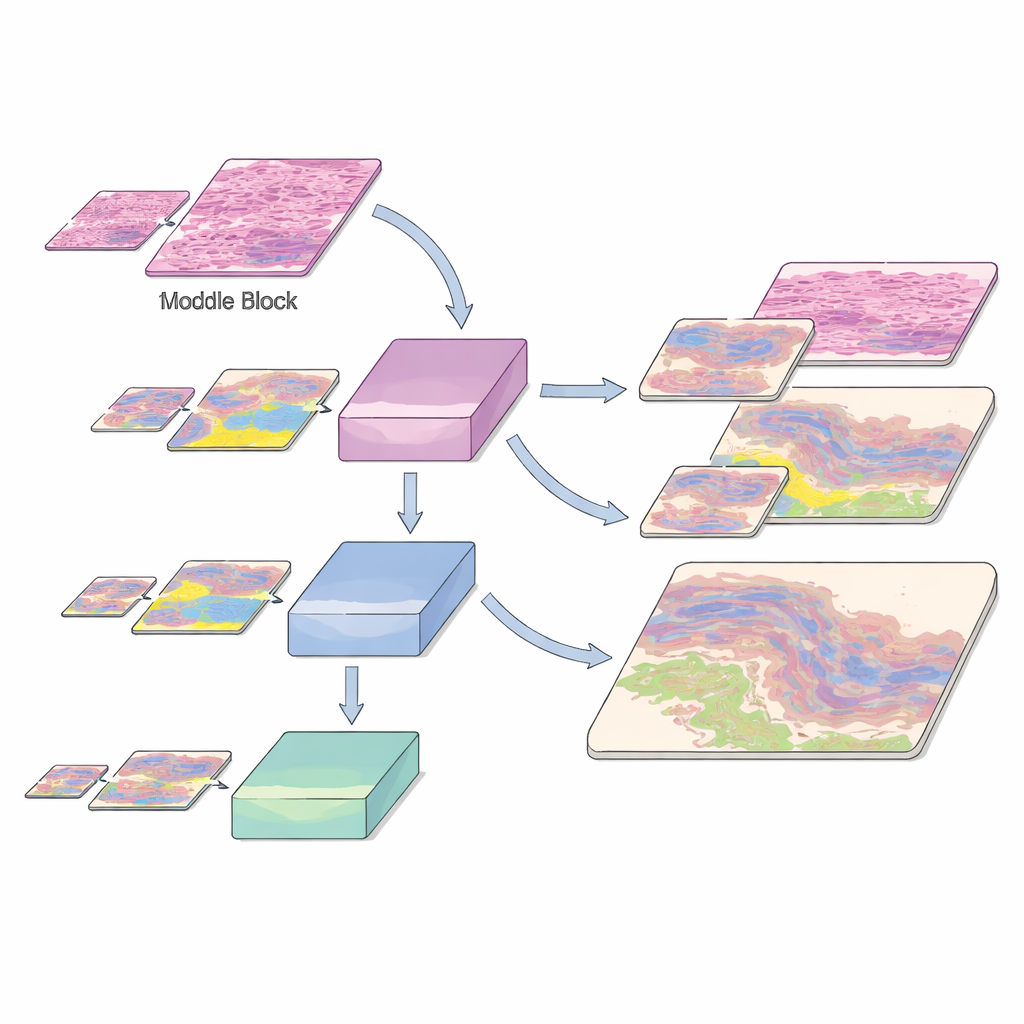
למידה על פני רמות זום וסוגי רקמה נדירים
תמונות היסטולוגיה מאתגרות לא רק בגלל שיש הרבה סוגי רקמות, אלא גם מכיוון שחלק מהמבנים החשובים הם נדירים. מאגר הנתונים כולל סרטן נפוץ כגון קרצינומה בסיסית (basal cell carcinoma) וקרצינומה של תאי קשקש (squamous cell carcinoma), כמו גם שכבות עור תקינות ודלקתיות, שכל אחת מהן מתויגת ברמת פיקסל על ידי מומחים — תהליך מעייף שלוקח מאות שעות. המחברים חותכים את השקופיות הענקיות לטלאים קטנים ומאמנים את המודל שלהם באמצעות חלוקה קפדנית לסטי אימון, ולידציה ובדיקה, תוך שמירה על תמהיל מחלקות הרקמה בכל מגדיל. כדי לסייע למערכת לזהות אזורים נדירים אך קליניים מכריעים, הם מגבירים את הכמויות של קטגוריות מוחלשות על ידי סיבוב הטלאים וכן חושפים את המודל לאותן רקמות בכמה רמות זום. חשיפה זו ברזולוציות מרובות עוזרת ל־AI לזהות את אותו מבנה ביולוגי בין אם הוא מופיע כתקריב חד או כצורה רכה ומרוחקת יותר.
מה המודל משיג בהשוואה לכלים קודמים
במבחנים בנפרד, דגמי SegFormer מאומנים בכל מגדיל משיגים כבר ביצועים עדיפים על עיצובים קונבולוציוניים קודמים כגון U‑Net ברבות מקטגוריות הרקמה. אבל כאשר מיישמים את סכמת הלמידה המצטברת — אימון תחילה ב־10×, אחר כך ב־10× וב־5× יחד, ולבסוף ב־10×, 5× ו־2× ביחד — השיפורים בולטים. הדיוק הכולל עולה מכ־89% בזמן אימון רק עם תמונות ב־10× ליותר מ־95% לאחר שכל שלוש רמות המגדיל כלולות. מדדי חפיפה בין אזורים חזויים לאמיתיים משתפרים גם הם בהתמדה, וביצועים על סוגי סרטן כגון קרצינומה בסיסית וקרצינומה של תאי קשקש, כמו גם על שכבות תקינות מרכזיות כגון אפידרמיס ודורמיס פפילר, עולים על אלה של שיטות מתחרות. באופן חשוב, עם הוספת כל רמת זום חדשה, המודל אינו שוכח את מה שלמד קודם; במקום זאת, הבנתו את מבנה הרקמה נעשית חזקה וכללית יותר.
כיצד עבודה זו מקרבת אבחון בסיוע AI אל הקליניקה
ללא מומחיות מיוחדת, המסר המרכזי הוא שהמחברים יצרו "ממפה" של רקמות העור שיכול להמשיך ללמוד סוגי תמונות חדשים מבלי לאבד את כישוריו הישנים. על־ידי עיצוב קפדני של אופן הלמידה בשלבים ושל האופן שבו המודל מחזיר את הידע העבר שלו, הם מראים שניתן לבנות כלים של בינה מלאכותית שמתאימים את עצמם ככל שפרקטיקות הדימות הרפואי משתנות. אמנם יש צורך באימות נוסף ברחבי בתי חולים וסוגי מחלות שונים, אך הגישה המצטברת המבוססת על טרנספורמרים מצביעה על מערכות AI שיכולות להישאר מעודכנות עם נתונים משתנים, לספק הסברים חזותיים מפורטים על מיקום הגידולים, ולבסוף לתמוך בפתולוגים בקבלת החלטות טיפוליות בטוחות ועקביות יותר.
ציטוט: Fatima, S., Salam, A.A., Akram, M.U. et al. Incremental learning approach for semantic segmentation of skin histology images. Sci Rep 16, 9593 (2026). https://doi.org/10.1038/s41598-025-31553-6
מילות מפתח: סרטן העור, תמונות היסטולוגיה, סגמנטציה סמנטית, למידה מצטברת, טרנספורמרים בלמידה עמוקה