Clear Sky Science · he
הדמיה בחיה של דינמיקת אדנוזין חוץ‑תאי בלב ושינויו הפרמקולוגי במודלים של אי־ספיקת לב בדג הזבר
למה הסיפור של לב הדג חשוב
אי־ספיקת לב נותרת אחד הגורמים המובילים לתמותה ברחבי העולם, ורבים מהחולים מחמירים למרות התרופות הטובות הקיימות כיום. מדענים יודעים שתאי לב תחת לחץ משחררים לסביבתם "אותות מצוקה" כימיים, אך היה קשה לצפות באותות האלה בפעולה בתוך לב פעום. המחקר הזה משתמש בדג הזבר השקוף, שליבותיו הקטנות משקפות תכונות מרכזיות של לב אנושי, כדי לצפות באותות הסכנה בזמן אמת ולבחון דרך חדשה להשקטתם.
אותות מלב במצוקה
כשתאי לב נפגעים, הם משחררים מולקולות נשאיות־אנרגיה כגון ATP ואת תוצר פירוקו אדנוזין למרחב שמחוץ לתאים. מחוץ לתא, מולקולות אלה מפסיקות לשמש כדלק ומתחילות לתפקד כהודעות דחופות שעלולות להסיט ולהעצים תגובות דלקתיות. באי־ספיקת לב כרונית התגובה הדלקתית עלולה להפוך ליתר־פעילה ולפגוע בלב באופן מתמשך. עד כה, עם זאת, חִסר עדות ישירה בתוך הגוף של האופן שבו מולקולות אלה משתנות לאורך זמן בלב נכשל.
הפיכת דג הזבר למצלמת־כימיה חיה
הקבוצה מהנדסת דגי זבר שתאי לבם מייצרים על פני השטח חלבון חיישן זוהר מיוחד בשם GRABAdo. כאשר אדנוזין מצטבר מחוץ לתאים, החיישן זוהר בירוק חזק יותר, וכך כל לב קטן הופך למעשה למצלמת כימיה חיה. החוקרים גרו אי־סיפקת לב בדגי הזבר בעזרת תרפןדין, תרופה הידועה בהפרעת קצב ובעיכוב יכולת הכיווץ. כשהדגים פיתחו סימנים ברורים לאי־ספיקת לב — קצב פעימות איטי יותר, חדרים מוגדלים וחלשים יותר, בצקת סביב הלב וביצועים שחייה ירודים — החיישנים הלבביים שלהם זרחו, וחשפו עלייה משמעותית באדנוזין חוץ־תאי. מדידות כימיות של הזחלים כהלם אישרו שרמות האדנוזין הכוללות היו גבוהות בלבבים הנכשלים.
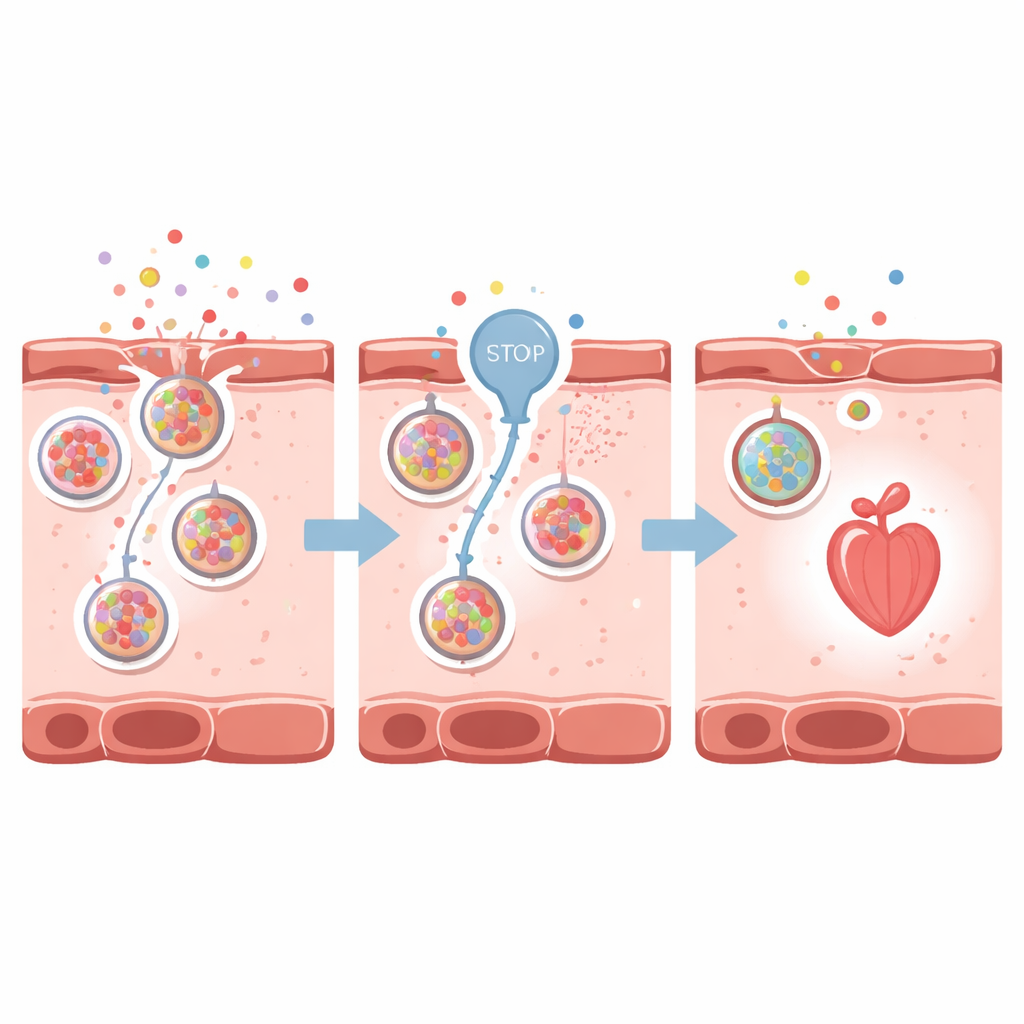
חסימת שסתום השחרור
המדענים שאלו אם השתקת אותות המצוקה האלה יכולה להגן על הלב. הם התמקדו ב‑VNUT, נשא שמטעין ATP לתוך שלפוחות קטנות לשחרור מחוץ לתא. בעזרת קלודרונאט, תרופה החוסמת את VNUT, הם צמצמו את שחרור ה‑ATP ובהמשך את הצטברות האדנוזין סביב תאי הלב. בדגי זבר עם אי־ספיקת לב מונעת תרופתית, חסימת VNUT שמרה על צורת הלב, הקטינה את התרחבות החדרים, שיפרה קצב לב ועוצמת השאיבה, ושמרה על שֶׁטף דם טוב יותר. חיישן האדנוזין הזוהר דעך, מה שהצביע על כך שפחות אות מצוקה היה נוכח מחוץ לתאים. אפקטים מגנים דומים נצפו גם בדגי זבר בוגרים עם צורת אי־ספיקת לב חריפה ומהירה התפתחות.
מַנּוּעוֹת רגנרטיביות מרובות שמשתפות פעולה
אי־ספיקת לב מערבת יותר מנתיב אחד, ולכן החוקרים בחנו כיצד חסימת VNUT מתקשרת עם שחקנים ידועים אחרים. תרופות החוסמות קולטנים מסוימים לאדנוזין ולקולטני ATP, וכן תרכובת שמגבילה זליגת ATP פסיבית דרך תעלות ממברנה, כל אחת תרמה לשיפור בלבי דג הזבר. בשילוב עם חסימת VNUT, רבות מהטיפולים האלה נתנו תועלות צבריות, מה שמרמז שכיבוי האיתות הפוריני בנקודות רבות יכול להיות רב עוצמה במיוחד. חסימת VNUT גם סייעה לשחזר איזון סידן בתאי לב, שהוא חיוני לפעימה תקינה, והקטינה הן את מוות התאים והן את פעילות הגנים המקושרים לדלקת. יחד, תוצאות אלה מציירות את VNUT כמפסק מרכזי שמקשר בין שחרור ATP, דלקת, בלבול בטיפול בסידן, ונזק לב מתקדם.
ממצברי דגים לטיפולים עתידיים
בהירות לציבור הרחב היא שהמחקר מדמה באופן ישיר אות כימי של מתח שעולה בלבבים נכשלות ומראה שחסימת שחרורו יכולה להגן על תפקוד הלב בחיה חיה. למרות שליבות דג הזבר פשוטות יותר מלב אנושי, הן חולקות מספיק ביולוגיה כדי להוות מגרש ניסוי רב עצמה לרעיונות חדשים. על ידי חשיפת VNUT כמטרה מבטיחה בצומת שבין דלקת לחוסר יציבות חשמלית, עבודה זו מרמזת שטיפולים עתידיים באי־ספיקת לב עשויים לעשות יותר מלתמוך בזרימת הדם — הם עשויים גם להירגע באופן פעיל את השיחות התאית המזיקות שמדחפות את הלב לעבר כשל.
ציטוט: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
מילות מפתח: אי־ספיקת לב, אותות אדנוזין, מודל דג הזבר, דלקת, הגנה קרדיאלית