Clear Sky Science · he
אמצעי G-קוואדרופלקס בטלומרים שחשפו על-ידי ניתוח רשת מרקוב מורכבת
קשרים נסתרים בקצוות ה-DNA שלנו
בקצות הכרומוזומים שלנו נמצאים כובעים מגנים הנקראים טלומרים, שלעיתים משווים אותם לקצוות הפלסטיק של שרוכי נעליים. באזורים אלה ה-DNA יכול להתקפל לצורת קשרים יוצאי דופן בעלי ארבעה סלילים, הידועים כ-G-קוואדרופלקסים. מבנים זעירים אלה יכולים להשפיע על האופן שבו הגנים שלנו מתנהגים ועל קצב ההזדקנות של התאים או הופעת הסרטן. המחקר הזה מציץ מאחורי הקלעים של האופן שבו קשר כזה מתפרק בהדרגה, באמצעות סימולציות ממוחשבות מפורטות וניתוח נתונים מתקדם, כדי לחשוף צורות חולפות שקשה כמעט לתפוס בניסויים.
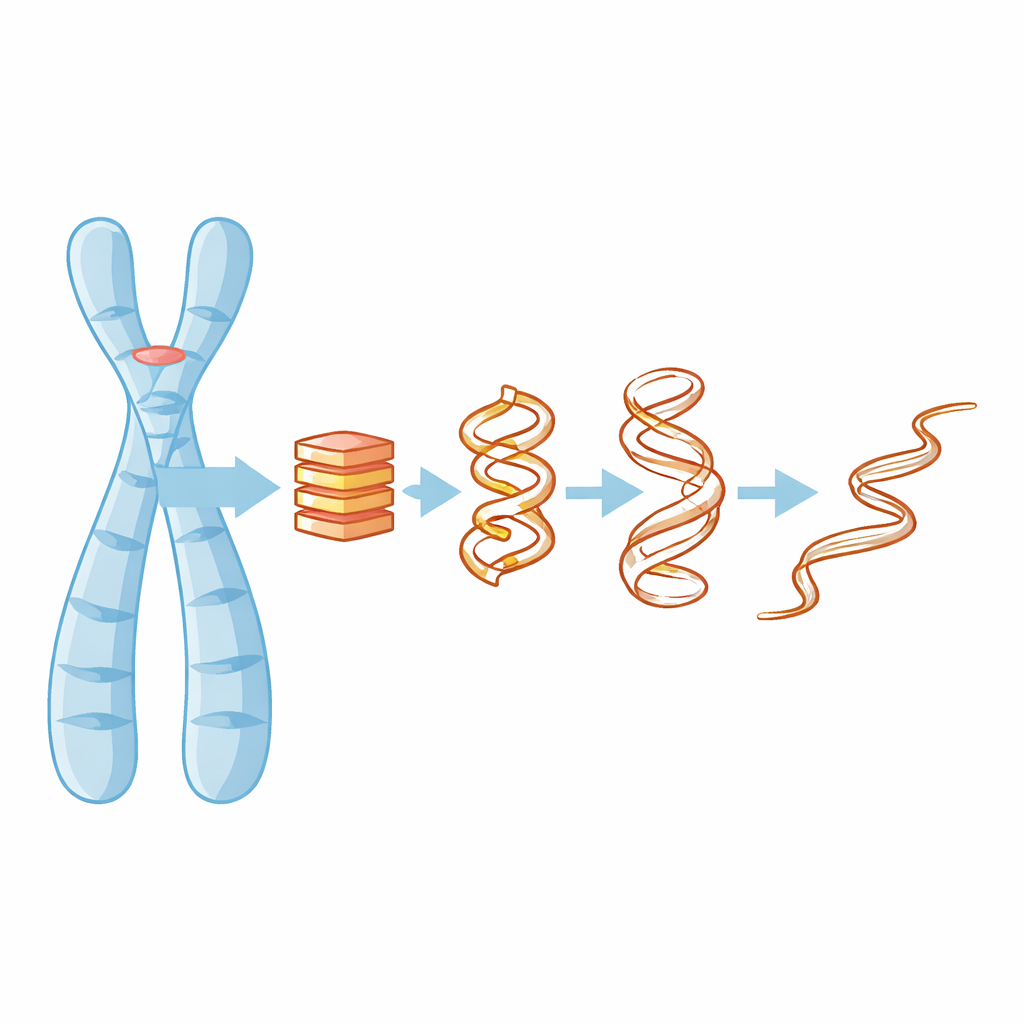
מדוע קשרי DNA ארבע-סליליים חשובים
רובנו לומדים ש-DNA הוא סליל כפול, אך במקטעים עשירים בגואנין—כמו אלה בטלומרים—המולקולה יכולה להתקפל לערימות קומפקטיות בעלות ארבעה סלילים הנקראות G-קוואדרופלקסים. ערימות אלה מחוברות יחד על ידי שכבות מישוריות של בסיסי גואנין ויונים טעונים חיובית זעירים, כמו אשלגן, היושבים במרכז ועוזרים להדביק את המבנה. כאשר G-קוואדרופלקס נוצר או מתפרק, הוא יכול לחסום או לחשוף חלקים מהגנום, להשפיע על פעילות גנים, שכפול DNA ואפילו על האופן שבו תאי סרטן מתחזקים את הטלומרים שלהם. לכן, הבנת האופן שבו מבנים אלה מאבדים את צורתם היא מפתח להבין איך לכוון אותם באמצעות תרופות או לחזות מתי הם עלולים לכשל.
צפייה בקשר מולקולרי שמתפרק
החוקרים התרכזו ב-G-קוואדרופלקס טלומרי אנושי שבו ארבעה מקטעים של שורת DNA אחת מסתדרים במקביל ומערימים לעמוד קומפקטי. הם השתמשו בסימולציות דינמיקה מולקולרית ברזולוציית כל-אטום—ניסויים וירטואליים שעוקבים אחרי תנועת כל אטום—והחממו שמונה עותקים של המבנה הזה לטמפרטורות בסמוך לנקודת ההיתוך שלו. כדי לעזור למערכת לחקור צורות שונות השתמשו באסטרטגיה שנקראת החלפת רפליקה, שבה סימולציות בטמפרטורות שונות מחליפות מדי פעם קונפיגורציות. בשבע מתוך שמונה המקרים ה-G-קוואדרופלקס נשאר יציב; באחד הוא התמוטט לחלוטין. אירוע ההתמוטטות הנדיר הזה הפך למקרה-מבחן מפורט, והראה לא רק את הלפני והאחרי אלא רצף של צורות ביניים לאורך התהליך.
התפקיד הקריטי של היונים הזעירים
ממצא מרכזי הוא שהיונים הקטנים בתוך ה-G-קוואדרופלקס פועלים כמעצורי מרכז. כל עוד לפחות יון אחד נשאר מושקע בין שכבות הגואנין, המבנה נשמר ברובו, אולי משוחרר מעט אך עדיין ניתן לזיהוי. כאשר שני היונים עוזבים לבסוף את התעלה המרכזית, האימה מתפרקת במהירות. שכבות הגואנין מעוותות וחוטים בודדים מתקלפים, וה-DNA הכולל הופך למוארך וגמיש יותר. מולקולות סימולציה אחרות שאיבדו רק יון אחד נכנסו למצבים מתנדנדים אך חלקית מסודרים, דבר שמרמז שההתמוטטות המלאה דורשת את איבוד שני היונים היציבים—רמז מדוע כמה G-קוואדרופלקסים כה עמידים בתא.
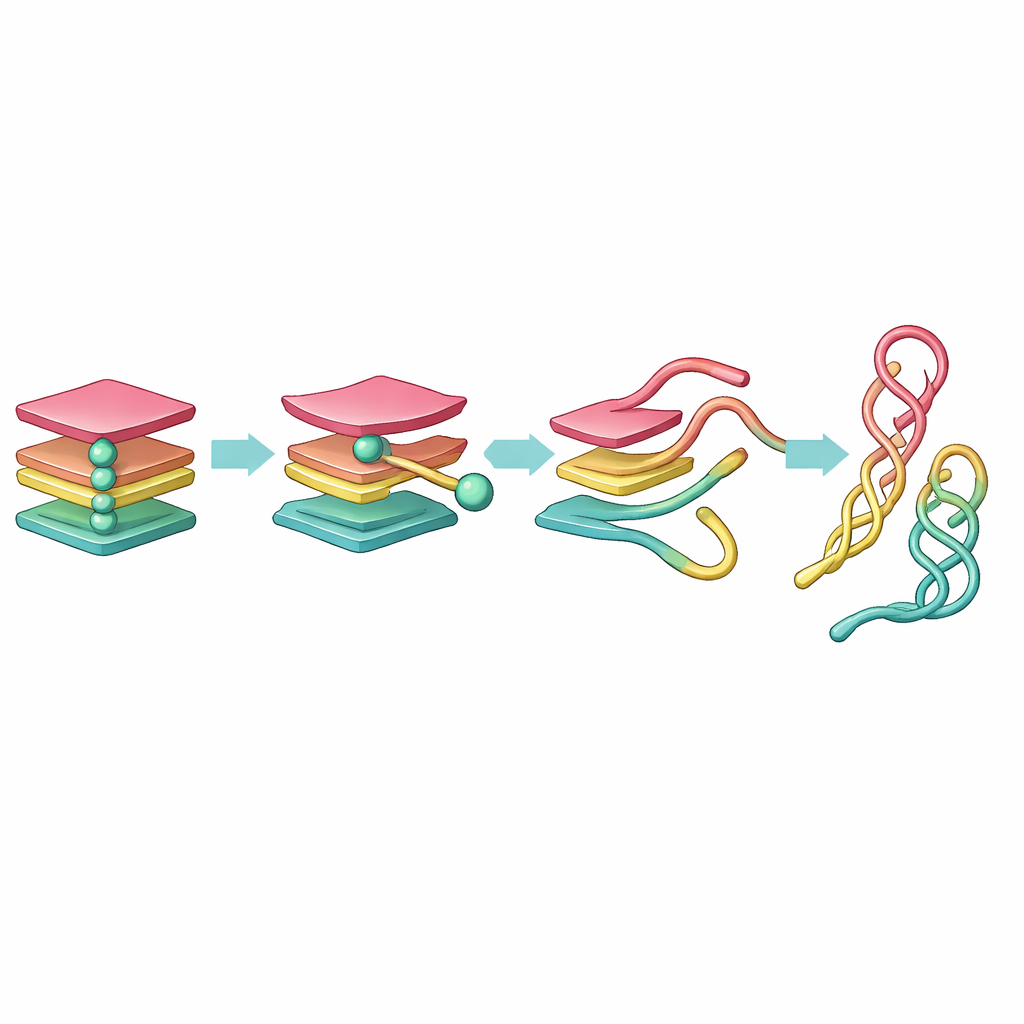
חשיפת נקודות דרך נסתרות במסע
הסימולציות הגולמיות ייצרו כמות עצומה של נתונים, מסובכת מדי כדי לפרש בעין. כדי לרסן זאת קיצרו החוקרים תחילה את ה-DNA על-ידי ייצוג כל בסיס כחרוז בודד, ואז השתמשו בכלים מתמטיים כדי לצמצם את התנועה לכמה קורדינטות מפתח בלבד. הם החילו שתי שיטות: ניתוח הרכיבים העיקריים (PCA), שמדגיש כיוונים של התנועה הגדולה ביותר, וניתוח רכיבים בלתי תלויים בזמן (tICA), שמסנן את השינויים האיטיים וארוכי-החיים שמסמנים מעברים מבניים אמיתיים. מתוך הקורדינטות המצומצמות האלה הם בנו רשתות מרקוב קונפורמציונליות, שבה כל צומת הוא צורת DNA טיפוסית וקישורים מראים כיצד המולקולה קופצת מצד אחת לאחרת.
נתיב מועדף מקשר לחוט משוחרר
מבט זה של הרשת חשף מסלול הבדילה ברור. בהתחלה, מתוך G-קוואדרופלקס מקופל לגמרי, חוט אחד מתנתק ראשון, ויוצר מצב תלת-סלילי שנקרא "טריפלקס". אותו טריפלקס מארגן מחדש לצורת דו-סליל "סיכה" (hairpin) וקבוצת חוטים רופפים בקרבת מקום. הסיכה והסידור הקרוב "צולבת-סיכה" מתגלים כארוכי-חיים למדי, ופועלים כנקודות דרך יציבות במסע מהקשר הצפוף לקונפיגורציית DNA רגועה יותר. בעוד ש-PCA פיצל את ההתקדמות הזו לרבים ממדגמי מצבים בעלי מראה דומה, tICA זקק אותה למערך קטן של צעדים מובחנים בעלי משמעות קינטית, והראה שמצבי טריפלקס דמויי הינם קצרים חיים, בעוד שמצבי סיכה דמויי נשארים לאורך זמן רב יותר.
מה משמעות הדבר לביולוגיה ולרפואה
לעיני לא-מומחה, המסר המרכזי הוא שטלומריים G-קוואדרופלקסים אינם פשוט נשברים ממצב מקופל למתפרק. במקום זאת, הם נמסים דרך רצף של צורות קצרות-וחיים וארוכות-חיים, כאשר יונים זעירים משמשים כשומרי סף של היציבות. הסימולציות מציעות כי מצבי תלת-סליל הם חולפים, בעוד שדו-סלילים בצורת סיכה וצורות צולבות הם נקודות מנוחה יציבות יותר. מכיוון שמצבים ביניים אלה עשויים להופיע גם בכיוון ההפוך—תהליך הקיפול—הם סביר שיהיו קריטיים באופן שבו G-קוואדרופלקסים נבנים, משתנים ומתקשרים עם תרופות פוטנציאליות. מיפוי נוף הצורות הנסתר הזה מקרב את המדענים צעד נוסף לעיצוב מולקולות שייצבו או יפגעו בבחירה בקשרים אלה של ה-DNA במאבק בסרטן ומחלות נוספות.
ציטוט: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
מילות מפתח: G-קוואדרופלקס, DNA טלומרי, דינמיקה מולקולרית, קיפול DNA ללא חלבונים, תרופות נגד סרטן