Clear Sky Science · he
HMI-LUSC: מאגר תמונות היפרספקטרליות היסטולוגיות עבור קרצינומה של תאי קשקש בריאה
להבחין בסרטן בצבעים חדשים
סרטן הריאות נשאר אחד המחלות הקטלניות בעולם, בין היתר מכיוון שזיהוי כל תא סרטני בשקופית מיקרוסקופ קשה וגוזל זמן. פתולוגים בדרך כלל מסתמכים על רקמות צבועות בוורוד ובסגול הנצפות במיקרוסקופ — שיטה שתופסת מבנה אך מפספסת רמזים כימיים עדינים. מאמר זה מציג את HMI‑LUSC, האוסף הזמין בפומבי הראשון של תמונות מיקרוסקופיות של קרצינומה של תאי קשקש בריאה, שנלקחו לא רק בשלושה צבעים אלא בעשרות פסי צבע צרים, ומעניקות למחשבים ולרופאים מבט עשיר הרבה יותר על מה שמבדיל תאים סרטניים מהשכנים הבריאים שלהם.
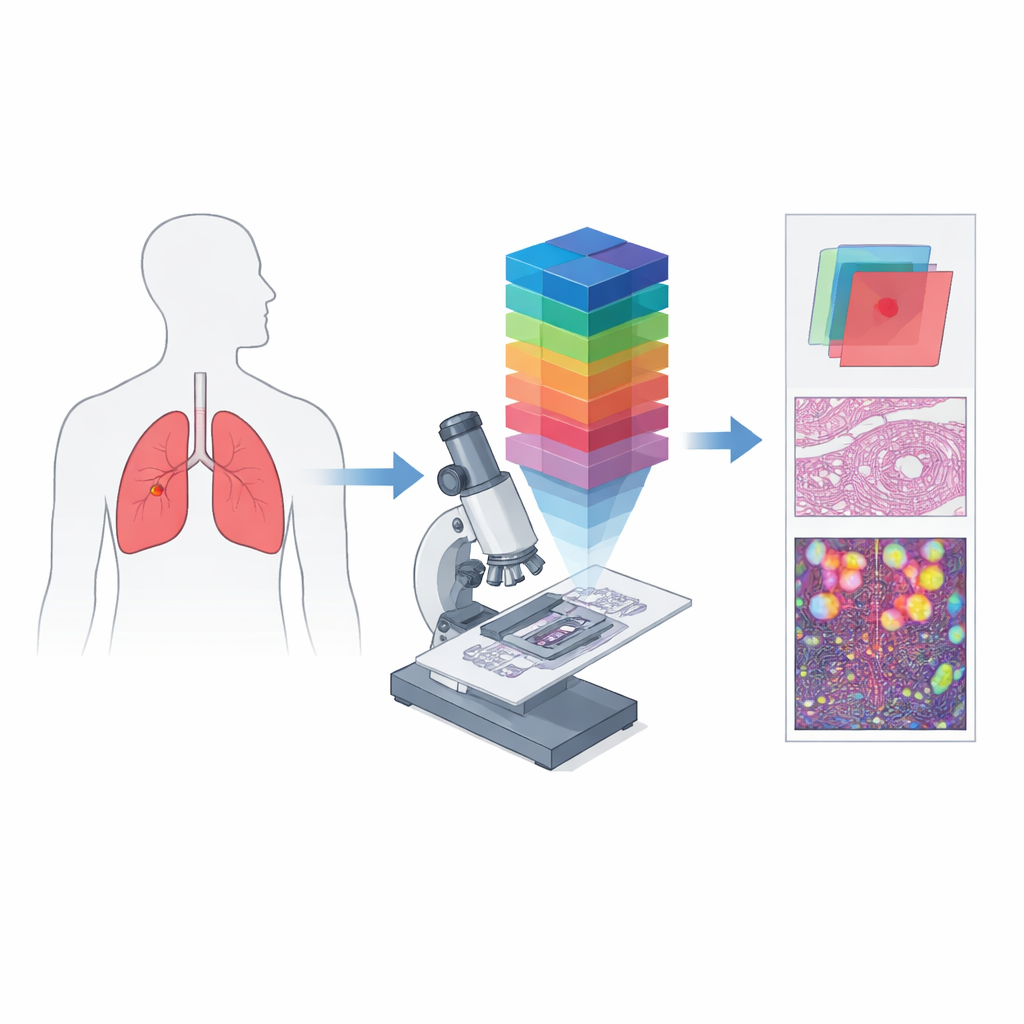
מ תמונות צבע פשוטות לטביעות אצבע ספקטרליות
פתולוגיה דיגיטלית קונבנציונלית עובדת בדומה למצלמת טלפון: היא מקליטה ערוצי אדום, ירוק וכחול כדי לאמוד מה שהעין רואה. הדמיה היפרספקטרלית הולכת כמה צעדים קדימה על ידי פיצול האור לאורך אורך גל רבים וצפופים, ויוצרת "קוביית נתונים" תלת‑ממדית שבה לכל נקודה זעירה ברקמה יש ספקטרום צבעים מפורט משלה. כשמשלבים רעיון זה עם מיקרוסקופ, נוצרת הדמיה מיקרוסקופית היפרספקטרלית, היכולה לתפוס הן מבנה עדין והן מידע ספקטרלי עשיר ברמת התאים הבודדים. נתונים כאלה יכולים לחשוף הבדלים בדרך שבה רקמות סופגות ומחזירות אור שאינם נראים בתמונות סטנדרטיות, ויוצרים "חתימות" ספקטרליות ייחודיות לאזורים סרטניים ולא-סרטניים.
בניית ספרייה חדשה למחקר סרטן הריאה
המחברים יצרו את HMI‑LUSC כדי למלא פער ברור: לפני עבודה זו לא היה מאגר היפרספקטרלי ציבורי לשקופיות של סרטן הריאה, מה שהקשה על בדיקה והשוואה של שיטות אבחון מבוססות מחשב. הם אספו רקמות מעשרה מטופלים שעברו ניתוח להסרת גידול ריאתי, הכינו שקופיות סטנדרטיות בצביעה המוקסילין־ואזן (hematoxylin‑and‑eosin), וסרקו אותן ברזולוציה גבוהה. פתולוגים מנוסים סימנו אזורי גידול ונורמליים, ואז אזורים מייצגים שוחזרו עם מיקרוסקופ היפרספקטרלי שנבנה בהתאמה אישית. כל תמונה שנוצרה מכסה טלאי קטן של רקמה אך משתרעת על פני 61 אורכי גל בין 450 ל‑750 ננומטר, ברזולוציה של 3088 על 2064 פיקסלים. לכל אזור, המאגר כולל את קוביית הספקטרל הגולמית, הצגה רגילה בצבעי RGB, ומסכות שמציירות את גבולות רקמת הגידול.
הפיכת קווים גסים למפות ברמת התא
בעוד שסימוני שקופית ברמת השקופית שימושיים, אימון אלגוריתמים מודרניים לעיתים דורש מידע ברמת התאים הבודדים. מעקב ידני אחרי כל תא אינו מעשי, ולכן הצוות תכנן זרימת עבודה חצי‑אוטומטית. ראשית, הם קיבצו פיקסלים לאשכולות על בסיס דמיון ספקטרלי באמצעות שיטת ראיית‑מחשב סטנדרטית. לאחר מכן פתולוגים בחנו את האשכולות הללו כשהן חופפות על תמונת הרקמה והקצו אותן לארבע קטגוריות: תאי גידול, תאים לא‑גידוליים, רקמה שאיננה תאים כמו סטרומה או דם, ורקע ריק. פתולוג נוסף עשה סקירה והתאים את התוצאות, וחילוקי דעות הוסדרו בהסכמה. התוצאה היא סט של מסכות מפורטות פיקסל‑אחר‑פיקסל שתופסות תערובות עדינות של סוגי תאים ומחוזות גבול מבלבלים, ומספקות חומר הדרכה עשיר יותר למערכות למידת מכונה.
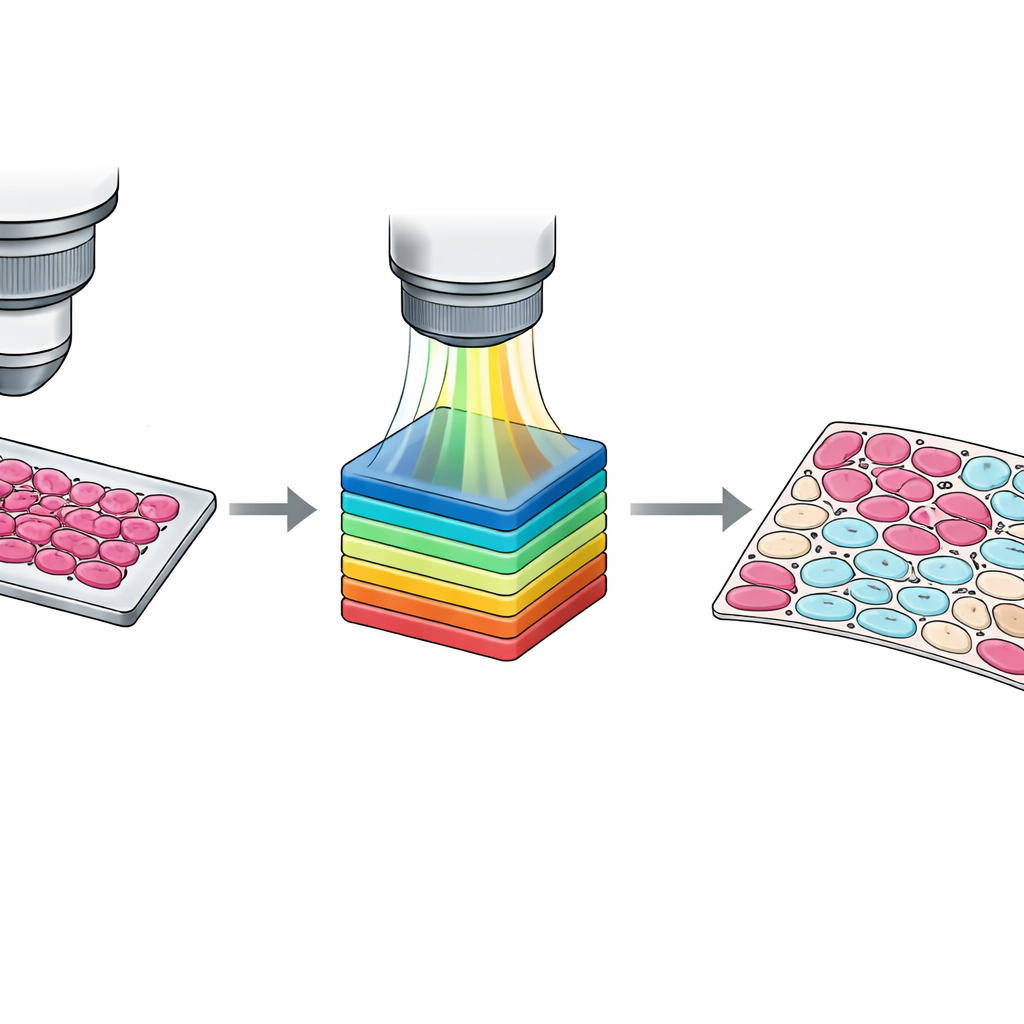
להבטיח נתונים חדים ואמינים
כדי להפוך את המאגר לאמין, המחברים בדקו בקפידה את מערכת ההדמיה שלהם. הם וידאו שהמיקרוסקופ מסוגל לפתור תבניות עדינות עד בערך מיקרון אחד — קטן דיו להבחנה בין תאים בודדים — וששדה הרעש בתמונה נמוך ברוב אורכי הגל. הם גם השוו את הספקטרום הנמדד של מקור אור תקני עם עקומות ייחוס ועם מצלמה היפרספקטרלית מסחרית, ומצאו התאמה מצוינת. לבסוף, הם הדגימו כיצד ניתן להשתמש בנתונים על ידי הרצת מודלים חישוביים בסיסיים, משיטות למידת מכונה קלאסיות ועד רשתות עמוקות פשוטות, לצורך סגמנטציית אזורי הגידול. גם ללא אופטימיזציה מרובה, מודלים אלה השיגו דיוק מוצק, מה שמראה שהמאגר מתאים כקנה מידה להשוואת שיטות עתידיות.
מה זה אומר עבור טיפול עתידי בסרטן הריאה
HMI‑LUSC אינו מחליף אוספים רחבים של שקופיות סטנדרטיות, וגם אינו כלי קליני כשלעצמו בשלב זה. במקום זאת, הוא מציע לחוקרים חלון מתואם בקפידה לתצפית כיצד תאי גידול בריאה שונים מרקמות סמוכות על פני אורכי גל רבים של אור. על ידי הפיכת הנתונים, התוויות והקוד לזמינים באופן פתוח, המחברים מספקים מגרש ניסויים משותף לפיתוח והשוואת אלגוריתמים המשתמשים במידע ספקטרלי, מממייני בסיס פשוטים ועד רשתות נוירונים מתקדמות. בטווח הארוך, עבודה כזו עשויה לעזור למחשבים לסייע לפתולוגים לזהות גידולים בדיוק ובמהירות רבה יותר, ואולי לחשוף דפוסי ספקטרום הקשורים לסוג הגידול או לתגובה לטיפול שאינם נראים בתמונות רגילות.
ציטוט: Yan, Z., Huang, H., Guo, Y. et al. HMI-LUSC: A Histological Hyperspectral Imaging Dataset for Lung Squamous Cell Carcinoma. Sci Data 13, 415 (2026). https://doi.org/10.1038/s41597-026-06766-7
מילות מפתח: הדמיה היפרספקטרלית, סרטן הריאות, פתולוגיה דיגיטלית, סגמנטציה של גידול, מאגר נתוני הדמיה רפואית