Clear Sky Science · he
מיפוי כימרות של רכיבים ניידים-גן, מוצא ותפקיד בהגברת הפלסטיות של הטרנסקריפטום
נוסעים נסתרים ב‑DNA שלנו
חלק ניכר מה‑DNA שלנו מורכב מנוסעים ויראליים קדומים הנקראים רכיבים ניידים—קטעי קוד גנטי שפעם קפצו בגנומים כמו טפילים רודפי טרמפים. המחקר הזה מראה שהשרידים הויראליים הללו אינם רק זבל אילם: הם מסוגלים להשתלב לתוך הגנים שלנו וליצור מסרים היברידיים, לעזור לתאים להסתגל לתנאים משתנים ולפעמים לתמוך במחלות. על ידי מיפוי הכימרות הללו לאורך התפתחות, התבגרות וסרטן, המחברים מגלים דרך מפתיעה שבה ה‑DNA הויראלי ממשיך לעצב את הביולוגיה האנושית גם היום.
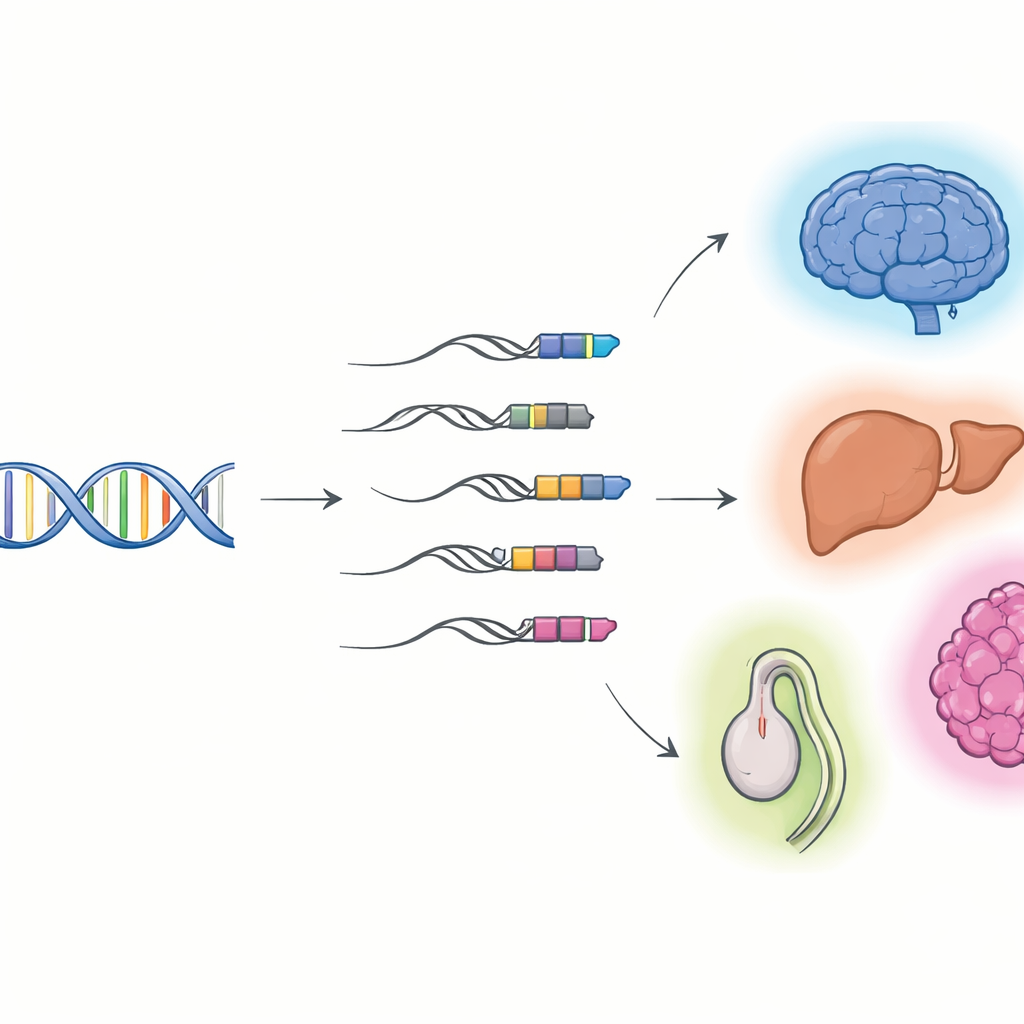
כש‑DNA ויראלי הופך לחלק מהגנים שלנו
החוקרים התמקדו ב"כימרות רכיב‑נייד–גן": מולקולות RNA שמתחילות ברכיב נייד וממשיכות לתוך גן המאכסן. בעזרת רצף ארוך‑קריאה, שיכול ללכוד מולקולות RNA שלמות מקצה לקצה, בשילוב עם רצף קצר‑קריאה סטנדרטי, הם בנו קטלוגים מפורטים של ההיברידים הללו בתאים ואברים של עכבר ואדם. הם מצאו אלפי טרנסקריפטים כימריים שלא היו ידועים קודם, רובם RNA שאינו מקודד ולא מתווה חלבון. רבים מתחילים במחלקה של שרידי וירוסים שנקראת רצפים סופיים ארוכים (LTR), שלעתים קרובות נמצאים בקדמת גנים ויכולים לפעול כמתגים חלופיים של הפעלה/כיבוי. רקמות ואיברים שונים משתמשים בערכות שונות של כימרות אלו, עם פעילות עשירה במיוחד במוח, בכבד ובאשכים, והשימוש בהן משתנה כאשר הרקמות מפתחות משלב עוברי למבוגר.
כימרות בהזדקנות ובסרטן
כדי לבדוק כיצד ההיברידים הויראליים‑מאכסן מתנהגים באוכלוסיות אמיתיות, הצוות חפר במאגרי נתונים אנושיים נרחבים הכוללים עשרות רקמות ממאות אנשים, וכן בדגימות גידול. הם זיהו כמה מאות כימרות באמון גבוה שחוזרות על עצמן בין אנשים. הביטוי שלהן משתנה לא רק בין איברים אלא גם עם הגיל: ברקמות כמו דם ומוח, חלק מהכימרות המונעות על‑ידי LTR יורדות בבוגרים מבוגרים, בעוד שבחלק מהרקמות הפריפריאליות הן עולות. במספר סוגי סרטן, ההיברידים המבוססים על LTR מופעלים באופן נרחב יותר בגידולים לעומת רקמה סמוכה תקינה, ומטופלים שהגידולים שלהם מבטאים יותר מהן נוטים להיפגע יותר. במאגרי נתונים של אנשים עמידים לכימותרפיה או אימונותרפיה, הגנים המושפעים מאקסונים חדשים מונעים‑LTR יושבים לעתים במסלולים קשורים למנגנון הפעולה של התרופות, מה שמרמז שכימרות רכיבים ניידים עשויות לסייע לגידולים להתארגן מחדש תחת לחץ טיפול.
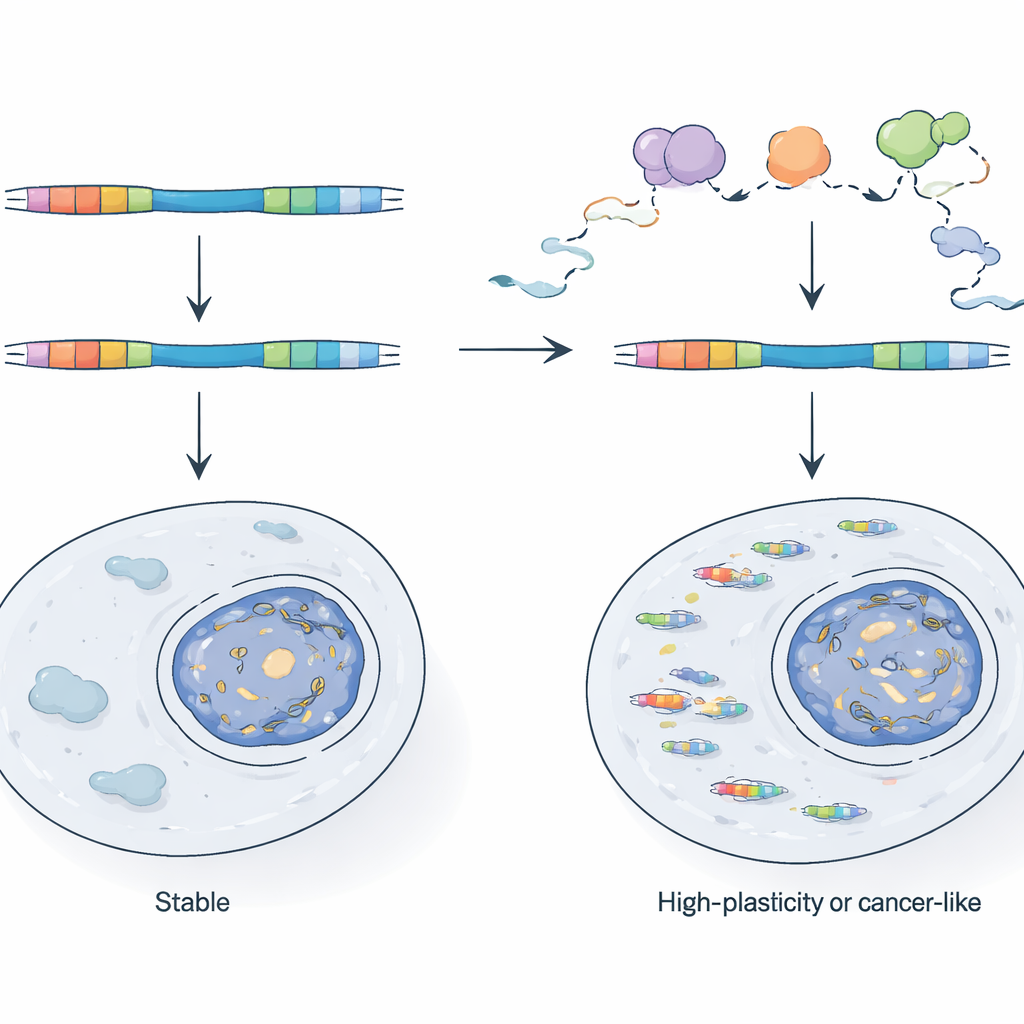
איך התאים שומרים על ההיברידים הויראליים בבדיקה
בהינתן הפוטנטיות שלהן, מדוע כימרות רכיבים ניידים לא מציפות תאים נורמליים? המחברים מראים שהתאים נשענים על מערכת בקרת איכות RNA, שמרכזת סביב קומפלקס האקסוזום גרעיני, לסרוק ולהשמיד רבים מהטרנסקריפטים הללו בזמן יצירתם. כאשר הם משבשים גנטית מרכיב מפתח של האקסוזום בתאי גזע של עכבר, המקדמים המונעים‑LTR נעשים פעילים הרבה יותר ו‑RNA כימרי עולה במידה ניכרת. בהשוואה בין RNA חדש ל‑RNA יציב הם מראים שחלק מה‑LTR מוחזקים בדרך כלל בבדיקה כיוון שהטרנסקריפטים שלהם מתפרקים במהירות, בעוד אחרים נשלטים ברמת תדירות תחילת השעתוק. LTRs פעילות אלה נוטות לשבת באזורים בגנום שכבר נגישים ותדירותית משועתקים, מה שמצביע על כך שהיותן סמוכות להגנה של גן פעיל או לטרנסקריפט אנטיסנס יכולה לעזור לקטע ויראלי להימלט מהשתקה אפיגנטית מסורתית.
ספלייסינג, פלסטיות תאי גזע ו"מפתח" ויראלי
הסיפור מסתבך עוד יותר כאשר מכנית החיתוך (splicing) של התא מופרעת. המחברים מדכאים מספר גורמי ספלייסינג מרכזיים או מעכבים כימית את הספלייסוזום וצופים בתוצאה משותפת לאובדן האקסוזום: עליה חדה בכימרות מונעות‑LTR ובגנים קצרים ודלי‑אינטרונים. בין המתווכים הבולטים נמצא MERVL, רטרו‑וירוס אנדוגני פעיל בעוברים מאוד מוקדמים של העכבר. כשסדרתו הפנימית של MERVL ופקטורי השעתוק שמאחוריה מועלים, תאי גזע נוטים לעבור למצב בעל אופי "טוטיפוטנטי‑דומה" יותר, המזכיר תאים עובריים מוקדמים שיכולים ליצור את כל הרקמות. לעומת זאת, הדגרדת RNA של MERVL באמצעות אוליגונוקלאוטידים אנטיסנס מרככת את המעבר הזה ומפחיתה את פעילות מקדמי ה‑LTR, מה שמעיד ש‑MERVL פועל כמפתח שיכול להצית רשת רחבה יותר של כימרות רכיבים ניידים ופלסטיות מצב‑תאי.
חדשנות ויראלית לאורך האבולוציה
בהסתכלות על ריבוי גנומי יונקים, הצוות עוקב אחר מתי משפחות רכיבים ניידים שונות התחילו לתרום אקסונים לגנים המארחים. הן בבני אדם והן בעכברים, משפחות LTR יחסית צעירות נוטות במיוחד ליצור כימרות בכיוון ה"חוש" שניתן לקרוא כחלק מהטרנסקריפטים של המארח. הדפוס הזה מרמז שגלים חדשים של הוספות TE סיפקו שוב ושוב חומר גלם לרשתות בקרה גנטיות לאורך זמן אבולוציוני. במקום להיות מזיקים בלבד, ההטמעות הללו יכולות להיבדק על‑ידי מכניקת השעתוק והדגרדציה של התא: רובן מושתקות או נהרסות, אך מיעוט מוצא את עצמו במקום ובהקשר הנכון כדי להיות ממנפות כאלמנטים רגולטוריים שימושיים או כהתחלות חדשות של גנים.
מדוע שרידי וירוסים אלה חשובים
ללא‑מומחה, עבודה זו מבהירה שחלק גדול ופעם מזלזל של הגנום שלנו מעצב באופן פעיל כיצד קוראים גנים, כיצד תאים משנים זהות וכיצד מחלות מתקדמות. רצפים ויראליים קדומים יכולים להפוך לדלתות קדמיות חלופיות של גנים, לייצר RNA היברידי שבדרך כלל מפוקח על‑ידי מערכות ניקוי תאיות. כאשר אותה פיקוח או הספלייסינג הרגיל מתקלקלים, ההיברידים הללו יכולים לפרוץ, לדחוף תאי גזע למצבים גמישים יותר או לסייע לגידולים להסתגל ולהתנגד לטיפול. במהלך מיליוני שנים האבולוציה ניסתה שוב ושוב בשדרוגים על גבי השרידים הויראליים האלה, והפכה רבים מהם מטפילים גנומיים לבני‑בנייה של מורכבות רגולטורית—ושארה לנו טרנסקריפטום הרבה יותר פלסטי ודינמי מאשר רשימת גנים פשוטה הייתה מרמזת.
ציטוט: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
מילות מפתח: רכיבים ניידים, טרנסקריפטים כימריים, השגחה על RNA, פלסטיות תאי גזע, התפתחות סרטן