Clear Sky Science · he
המבנה התת-מיקרוסקופי הסיבתי של העיבוי PopZ נחוץ לתפקידו התאי
כיצד תאים משתמשים בטיפות רכות כדי להישאר מסודרים
בתוך כל תא חי, הכימיה צפופה וכאוטית. עם זאת, תאים מצליחים לשמור על מולקולות קריטיות במקום ובזמן הנכונים. דרך אחת לכך היא יצירת טיפות זעירות בדמות נוזל, או עיבויים, שמרכזות חלבונים מסוימים ומוציאים אחרים. המחקר בוחן מקרוב חלבון בונה-טיפות כזה בחיידקים, הנקרא PopZ, ומראה שמסגרת הפנימית שלו העשויה מסיבים זעירים חיונית לשמירה על תהליכים תאיים מכריעים.
מארגן מיקרוסקופי בקוטבי התא
בחיידק Caulobacter crescentus, PopZ מתרכז בשני הקצוות, או הקוטבים, של התא שם הוא יוצר מחיצות מרוכזות. "מיקרודומיינים" עשירים ב-PopZ אלה מסייעים לשלוט במחזור התא על ידי משיכת חלבונים שותפים ספציפיים ועיגון הכרומוזום במהלך החלוקה. כאשר PopZ נמחק, התאים מתקשים להתחלק, מאבדים את צורתם הרגילה ומטפלים ב-DNA בצורה לקויה. מחקרים קודמים הראו שאם טיפות PopZ הן מדי נוזליות או מדי קשיחות, התאים גם כן מתקשים. מה שלא היה ידוע הוא כיצד המבנה המפורט בתוך הטיפות — הדרך שבה מולקולות PopZ מסתדרות לצורות גדולות יותר — מכתיב את תכונות החומר שלהן ואת ההתנהגות התאית הנכונה.
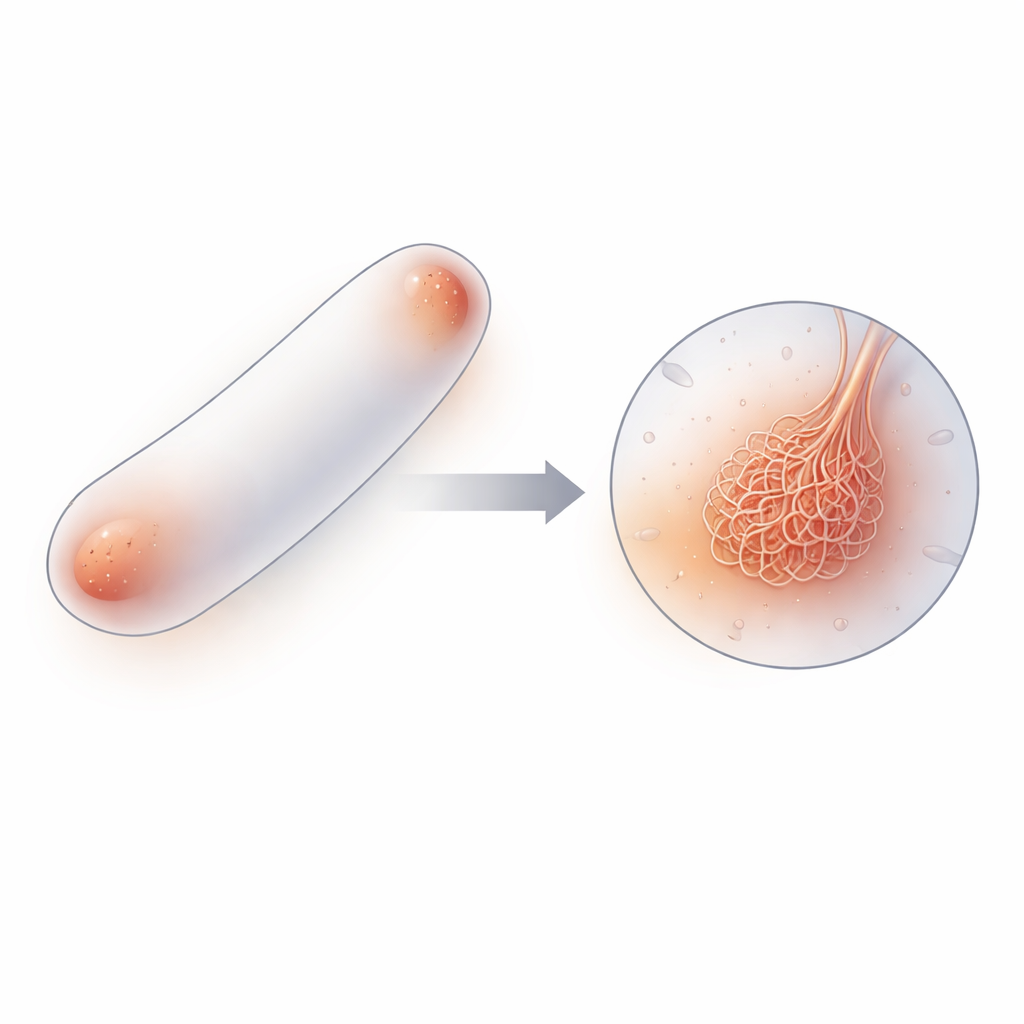
ממולקולות בודדות לרשת סיבית
בעזרת שילוב של טומוגרפיית קריו-אלקטרון (שיטת הדמיה תלת-ממדית בטמפרטורות נמוכות מאוד), בדיקות ביוכימיות, פלואורסצנציה של מולקולות בודדות וסימולציות מחשב, החוקרים מיפו כיצד מולקולות PopZ מרכיבות עצמן בקני מידה שונים. חלבוני PopZ בודדים מצטרפים תחילה ליחידות של שלושה חלקים (טרימרים), אשר לאחר מכן מתמזגות לזוגות ויוצרות יחידות של שישה חלקים (הקסאמרים). הקסאמרים הללו נערמים קצה-לקצה לסיבים קצרים וגמישים באורך של עשרות ננומטרים, ורשתות מסובכות של סיבים אלה מהוות את העיבוי של PopZ. הדמיה של טיפות PopZ מטוהרות ושל PopZ בתאים שלמים הראתה את אותה רשת סיבית, מה שמצביע על כך שהארכיטקטורה הזו אינה ארטיפקט של ניסויי מבחנה אלא תכונה מרכזית באופן שבו PopZ פועל בחיידקים חיים.
בלמים ומתגים מובנים ליצירת טיפות
PopZ מורכב מקטעים מובחנים שכל אחד מהם ממלא תפקיד שונה בקו ההרכבה הזה. מקטע הלבנה קומפקטי בקצה הזנב משמש כמודול המרכזי לאוליגומריזציה ולהיווצרות סיבים, חזק דיו כדי לבנות סיבים וטיפות בפני עצמו. לעומתו, מקטע רפוי ובעל מטען שלילי באמצע נוטה להרחיק מולקולות זו מזו, מה שמקשה על העיבוי. בקצה הנגדי, הליקס קצר מושך חלבוני לקוח ובמצב הממוסס הוא מתקפל בחזרה לגעת בזנב, ובכך ממעיט בצבירה מוקדמת. כאשר התנאים משתנים — למשל בנוכחות מלחים מסוימים — אינטראקציות דוחות אלה מתחלשות. PopZ משנה אז את קונפורמצייתו: הליקס הקושר לקוחות מתרחק מהזנב, ענן המקטעים הלא-מסודרים נפתח, הקסאמרים נערמים בקלות רבה יותר לסיבים, ואינטראקציות בין-סיביות הופכות לנסבלות. שינוי קונפורמציה התלוי פאזה זה אומר שהאזור החלבוני שמנע קישור במצב הממוסס הופך לאתר עגינה פעיל ברגע שנוצר העיבוי.
מה קורה כאשר מסירים את הסיבים
כדי לבדוק כיצד סיבים משפיעים על התנהגות הפיזית של הטיפה, הקבוצה הנדסה מוטנטים של PopZ שיכלו עדיין ליצור הקסאמרים אך לא יכלו לערום אותם לסיבים. וריאנטים אלה אכן יצרו עיבויים, אך עם תכונות שונות במידה ניכרת. במקום ליצור כדורים מסודרים שיושבים על המשטח, הטיפות נשברו והתשטחו, מה שמעיד על מתח שטח נמוך יותר והרטבה חזקה יותר של הסביבה. בתוך העיבויים העניים בסיבים אלה, גם PopZ עצמו וגם חלבוני הלקוח שלו נעו מהר יותר, כפי שנמדד על ידי החלמת פלואורסצנציה אחרי דה-אור (FRAP). במילים אחרות, הסרת הסיבים עשתה את הטיפות רכות ודליפות יותר. כאשר מוטנטים כאלה הוכנסו לתאי Caulobacter, הם שיבשו את התנהגות PopZ הרגילה בקוטבים, הפריעו לעיגון הכרומוזום ופגעו קשות בצמיחה, אפילו בנוכחות PopZ בר-טיפוס. וריאנטים מהונדסים אחרים הראו את חוסר ההתאמה ההפוך: הם יכלו ליצור סיבים אך נכשלו בהתעבות יעילה, וגם הם לא הצליחו להציל במלואה את תפקיד PopZ בתא.
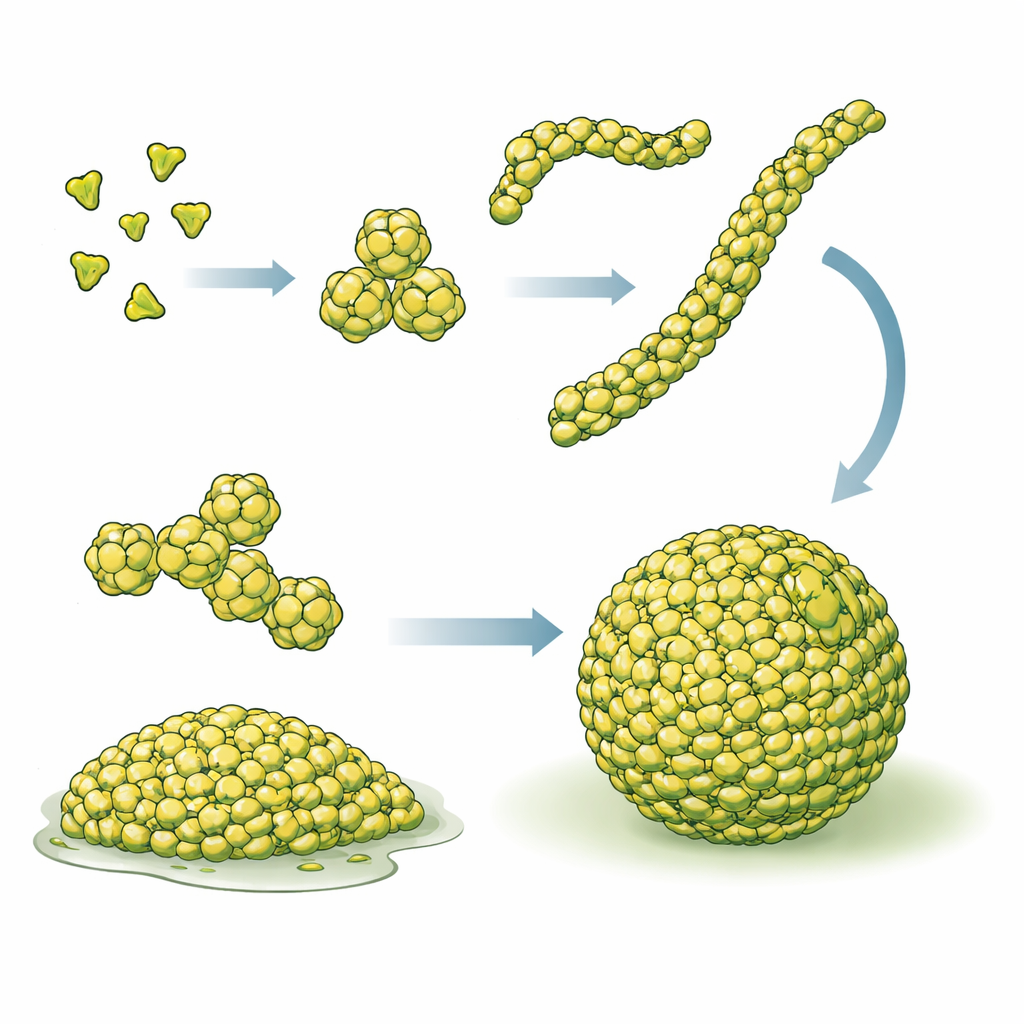
מתכון לטיפות תפקודיות בתא
הממצא מוביל למסר ברור עבור הקוראים הכלליים: אין די בכך שחלבון כמו PopZ יתאסף סתם יחד, וגם לא די ביצירת סיבים בפני עצמם. מה שחשוב לתפקוד התאי הוא אולטרה-מבנה ספציפי מאוד — עיבויים המורכבים בעצמם מסיבים קצרים ומחוברים ביניהם. מסגרת סיבית זו מגדילה את מספר נקודות המגע בין מולקולות, מעלה את מתח השטח של הטיפה, מאט את תנועת הלקוחות המרכזיים, ומספקת מתג מולקולרי מובנה שמאפשר קישור לקוחות רק בפאזה הצפופה. על ידי מעקב אחר שרשרת הסיבה והתוצאה מרצף חומצות אמינו להרכבים מולקולריים ולהתנהגות תא-כוללת, המחקר מציע תבנית כללית לאופן שבו תאים עשויים לכוונן את "התחושה" של הטיפות הרכות הפנימיות שלהם כדי לשלוט בתהליכים חיוניים.
ציטוט: Scholl, D., Boyd, T., Latham, A.P. et al. The filamentous ultrastructure of the PopZ condensate is required for its cellular function. Nat Struct Mol Biol 33, 420–432 (2026). https://doi.org/10.1038/s41594-025-01742-y
מילות מפתח: עיבויים ביומולקולריים, סיבי חלבון, קוטביות תאית, הפרדת פאזה, מחזור התא בחיידק