Clear Sky Science · he
AF2BIND: חיזוי אתרי קשירת מולקולות קטנות באמצעות ייצוג הזוגות של AlphaFold2
איתור מטרות תרופות בים של חלבונים
תרופות מודרניות רבות פועלות על ידי התקשרות לנישות וזוויות זעירות על פני שטח החלבונים בתוך התאים שלנו. עם זאת, אפילו עם קטלוגי המבנים העצומים של היום, קשה למדי לנבא מראש היכן עשויה מולקולה קטנה — תרופה פוטנציאלית — להידבק בפועל. המחקר הזה מציג את AF2BIND, כלי חישובי פשוט אך רב־עוצמה החופר בשכבות הפנימיות של AlphaFold2, חיזוי המבנה פורץ הדרך, כדי להאיר אתרי קשירה נסתרים ומבקשים סבירות לקשירת תרופות על פני אלפי חלבונים אנושיים. מטרתו לצמצם את החיפוש אחר תרופות חדשות ולחשוף נקודות חמות פונקציונליות שהשיטות המסורתיות מפספסות.
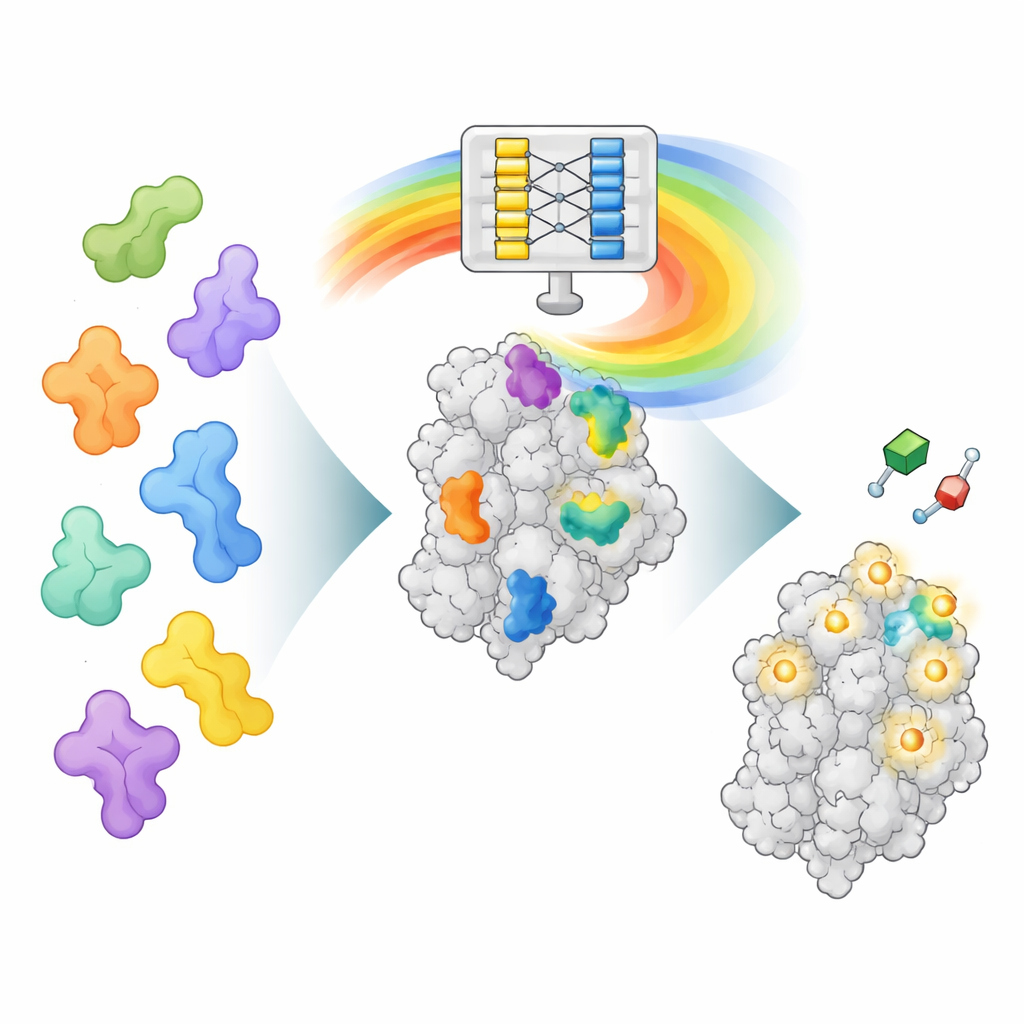
דרך חדשה לקרוא את “המוח” של AlphaFold
AlphaFold2 אומן לחזות כיצד שרשרת חומצות אמינו מתקפלת למבנה תלת־ממדי של חלבון, לא כדי למצוא היכן תרופות נקשרות. עם זאת, בתהליך לימוד הקיפול הוא רכש גם דפוסים עשירים על האינטראקציות בין חלקי החלבון השונים. AF2BIND מנצל אחת משכבות הנתונים הפנימיות הללו, שנקראת ייצוג הזוג (pair representation), שמקודדת כיצד כל זוג מיקומי חומצות אמינו מתקשר במרחב. המחברים מספקים ל‑AlphaFold2 רצף חלבון יחד עם שלד המבנה שלו וגם מצרפים 20 חומצות אמינו נוספות, אחת מכל סוג, כ”פיתיונות” נפרדים. AlphaFold2 מחשב אז כיצד החלבון מתקשר עם כל שייר־פיתיון. דפוסי אינטראקציה אלה הופכים לקלט למודל רגרסיה לוגיסטית פשוט מאוד שמעריך, עבור כל מיקום בחלבון, את ההסתברות שהוא שייך לאתר קשירת מולקולה קטנה.
הפיכת אותות נסתרים לחיזויים מעשיים
אימון AF2BIND דרש מערך מוקפד של כ־1,900 מבני חלבון–ליגנד שבהם מולקולות קטנות נקשרו עם ראיות ניסיוניות באיכות גבוהה. החוקרים הלכו רחוק כדי למנוע “רמאות” על ידי דמיון: הם חילקו את הנתונים כך שחלבוני המבחן לא ישתפו קיפול כולל, רצף, ואף צורת כיס הקשירה עם אלה ששימשו לאימון. בבנצ’מרק המחמיר הזה, ייצוג הזוג של AF2 עלה על מספר אמבדינגים חלופיים של רשתות עצביות, כולל אלה המבוססים רק על רצף או על עיצוב רצף מותנה במבנה. באמצעות תכונות הזוג בלבד, AF2BIND שיחזר כ־שני שלישים מהשיירים הידועים כקשורים בקשירה בתחזיות המדורגות היטב והציג ביצועים חזקים במדדי סיווג סטנדרטיים, תוך עמידות לשינויים מתונים בצורת החלבון ובהתמצאות השרשראות הצדדיות.
קריאת רמזים כימיים מפיתיונות
מכיוון ש‑AF2BIND הוא מודל ליניארי פשוט, החלטותיו שקופות באופן יוצא דופן עבור מערכת בינה מלאכותית מודרנית. כל אחת מ‑20 חומצות ה־פיתיון תורמת כמות מדידה לציון הסופי של קשירה במיקום נתון בחלבון. בבחינת תרומות אלה לאורך כ־2,000 קומפלקסים של חלבון–ליגנד, מצאו המחברים ששילובים מסוימים של פיתיונות נדלקים חזק יותר עבור ליגנדים שמנים, עשירים בפחמן, בעוד שאחרים פעילים יותר מול מולקולות קוטביות, אוהבות מים. במילים אחרות, דפוס ההפעלה של הפיתיונות מתפקד כמו טביעת אצבע כימית גסה של סוגי המולקולות הקטנות שהכיס מעדיף. זה מרמז שבעתיד גישות בדומה ל‑AF2BIND עשויות לא רק לציין היכן ניתן לקשור תרופה, אלא גם לרמז על סוג הכימיה שתתאים ביותר.
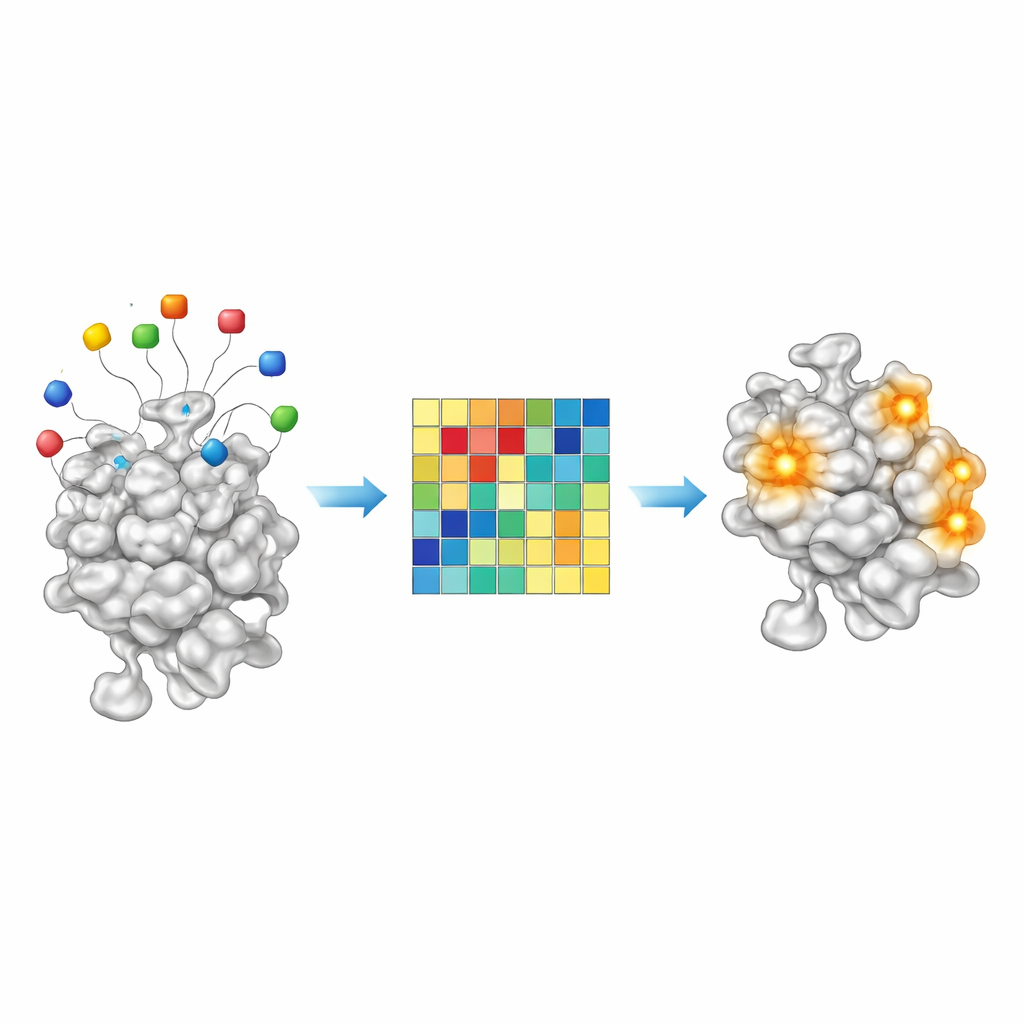
סריקה של הפרוטאום האנושי אחר כיסים חדשים
מצוידים במודל המאומן שלהם, הקבוצה שחררה את AF2BIND על המבנים ש‑AlphaFold חזה של כל הפרוטאום האנושי. לאחר חיתוך אזורים בעלי אמון נמוך וחלוקה של חלבונים גדולים מדי לחתיכות מבניות ניתנות לניהול, הם קיבצו שיירים בעלי ציונים גבוהים סמוכים לאתרי קשירה מועמדים. AF2BIND ניבא מעל 20,000 אתרים כאלה בלמעלה מ‑13,000 חלבונים. באופן מרשים, רובם לא חפפו עם כיסים שחושבו על ידי שיטות מבוססות הומולוגיה כמו AlphaFill, שמעתיקה ליגנדים ממבני קריסטל קרובים, ולא עם כלי מציאת כיסים נפוץ בשם P2Rank. רבים מהאתרים הייחודיים ל‑AF2BIND שטוחים או מפוזרים יותר מאשר כיסים קלאסיים שקבורים ולעתים חופפים לאזורים שקושרים פפטידים, RNA, DNA או חלבונים אחרים — ממשקים שיכולים למרות זאת להיות ניתנים למיקוד על ידי מולקולות קטנות.
השלכות לגילוי תרופות ומחלה
כדי לשפוט עד כמה האתרים המוצעים הללו מבטיחים לעיצוב תרופות, המחברים השתמשו בכלי עצמאי שמדרג “דרגביליות” על סמך גודל הכיס, סוגרוּת והסביבה הכימית. בממוצע, אתרי AF2BIND קיבלו ציונים מעל סף מקובל למטרות תרופות אטרקטיביות, כולל כאלו שנמצאו בחלבונים הקשורים למחלות תורשתיות. כשנבדקו מול ניסויי כימופרוטאומיקה שמסמנים ציסטאינים ריאקטיביים בתאים, AF2BIND ו‑P2Rank יחד הסבירו כמעט חצי מהאזורים שנצפו כניתנים לקשירה, כשכל שיטה קלטה מקרים שהשנייה החמיצה. העבודה מראה שייצוגים פנימיים הנלמדים על ידי רשתות חיזוי מבנה ניתנים לשימוש חוזר כדי למפות אתרי קשירת תרופות בסקלת המונית, ללא ידע מוקדם על ליגנד ספציפי. עבור לא־מומחים, המסר המרכזי הוא שהפריצות בתחום ה‑AI שחוזות צורות חלבון מתחילות גם לחשוף היכן וכיצד תרופות עשויות להיאחז בצורות אלו, מה שעלול להאיץ את החיפוש אחר טיפולים חדשים ולהאיר נקודות בקרה חבויות בחלבונים שלנו.
ציטוט: Gazizov, A., Lian, A., Goverde, C. et al. AF2BIND: predicting small-molecule binding sites using the pair representation of AlphaFold2. Nat Methods 23, 626–635 (2026). https://doi.org/10.1038/s41592-026-03011-2
מילות מפתח: אתרי קשירת חלבון, גילוי תרופות, AlphaFold2, ביולוגיה חישובית, ביואינפורמטיקה מבנית