Clear Sky Science · he
DECODE: מסגרת דיקונבולוציה כללית מבוססת למידה עמוקה לנתוני '-omics' שונים
מדוע המחקר הזה חשוב
הביומדיצינה המודרנית מוצפת במדידות של הרקמות שלנו: אילו גנים פעילים, אילו חלבונים קיימים ואילו מולקולות קטנות מזינות את התאים. עם זאת, רוב המדידות הללו מתבצעות על דגימות מעורבות, שבהן תערובת של סוגי תאים משולבת יחד. המחקר מאחורי DECODE מציג מסגרת בינה מלאכותית חזקה שמסוגלת לפצל את אותות אלה, ולתת אינדיקציה אילו תאים ואילו מצבי תאים קיימים, גם בין סוגי נתונים שונים מאוד. יכולת זו עשויה להאיץ מחקרים בסרטן, חיסון ומחלות מטבוליות תוך שימוש טוב יותר בדגימות ביובנק קיימות.
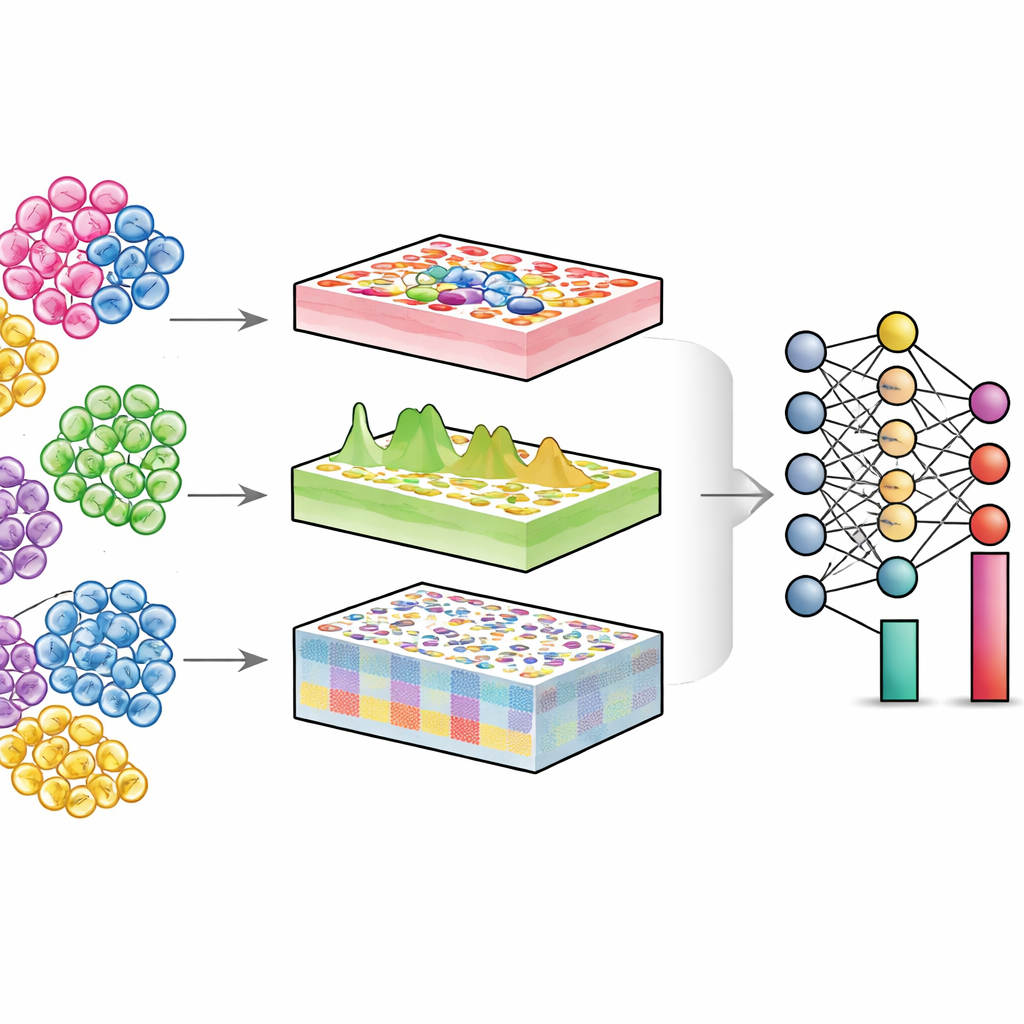
מציצים בתוך רקמות מעורבות
כל איבר הוא קהילה של סוגי תאים שונים—תאי חיסון, תאים מבניים, תאי גזע ועוד. בבריאות ובמחלה, מה שמשתנה לעתים קרובות הוא לא רק מה שכל תא עושה, אלא כמה ממכל סוג נמצא ומה מצבו. טכנולוגיות תאים בודדים יכולות למדוד תאים בודדים ישירות, אך הן יקרות וטכניות מאוד, במיוחד עבור קוהורטים גדולים של חולים או דגימות אחסון ישנות. לעומת זאת, ניסויים “בולק” קונבנציונליים מערבבים אלפי או מיליוני תאים וקוראים אות ממוצע. אלגוריתמי דיקונבולוציה מנסים להפוך את המעורב: בהתבסס על נתוני בולק ומפת התייחסות של תאים בודדים, הם מעריכים את השיעור של כל סוג תא ברקמה.
מגבלות של כלים ממוקדים
כלי דיקונבולוציה קיימים מותאמים ברובם לסוג מדידה יחיד, כגון פעילות גנים (טרנסקריפטומיקה) או חלבונים (פרוטאומיקה). הם מניחים לעתים התנהגויות סטטיסטיות ספציפיות שאינן תקפות עבור סוגי נתונים אחרים, והם מתקשים כאשר ברקמת הבולק קיימים סוגי תאים החסרים בנתוני ההתייחסות. השפעות אצווה חזקות—הבדלים בתורמים, במכשירים או במצבי בריאות—יכולות לטשטש עוד יותר את האותות הביולוגיים. במיוחד, לא הייתה שיטה מעשית למטבולומיקה, חקר המולקולות הקטנות שלעיתים קרובות קרובות להסמפטומים קליניים. כתוצאה מכך, מדענים שחקרו קוהורטים מולטיאומיים נדרשו להפעיל מספר כלים מיוחדים, לכל אחד מהם תכונות משלו, מה שהקשה על השוואת תוצאות בין מחקרים וסוגי נתונים.
מנוע פירוק-מעורב אוניברסלי
DECODE מתמודד עם האתגרים האלה על ידי טיפול בדיקונבולוציה כבעיה גמישה של למידה עמוקה שיכולה להתמודד עם גנים, חלבונים ומטבוליטים באופן מאוחד. ראשית, הוא מסנתז “פסאודורקמות” על‑ידי ערבוב דיגיטלי של פרופילים של תאים בודדים בפרופורציות אקראיות, ויוצר סט אימון עשיר שבו הרכב התאים האמיתי ידוע. שלב למידה אדברסריאלי מלמד אז מקודד למפות גם רקמות אמיתיות וגם פסאודורקמות לייצוג משותף שבו ההבדלים הטכניים ממוזערים אך דפוסים ביולוגיים משמעותיים נשמרים. לאחר מכן, מודול ניקוי רעשים מיוחד, מודרך על‑ידי למידה קונטרסטיבית, לומד להפריד בין אותות רקמה אמיתיים לרעשים מלאכותיים. שלב זה הופך את DECODE לעמיד לחסר סוגי תאים בהתייחסות ולשגיאות מדידה. לבסוף, התכונות הנקיות מועברות למודול דיקונבולוציה שמעריך או שפע מוחלטים או יחסי של סוגי תאים ומצבי תאים, בהתאם למידת השלמות של ההתייחסות.
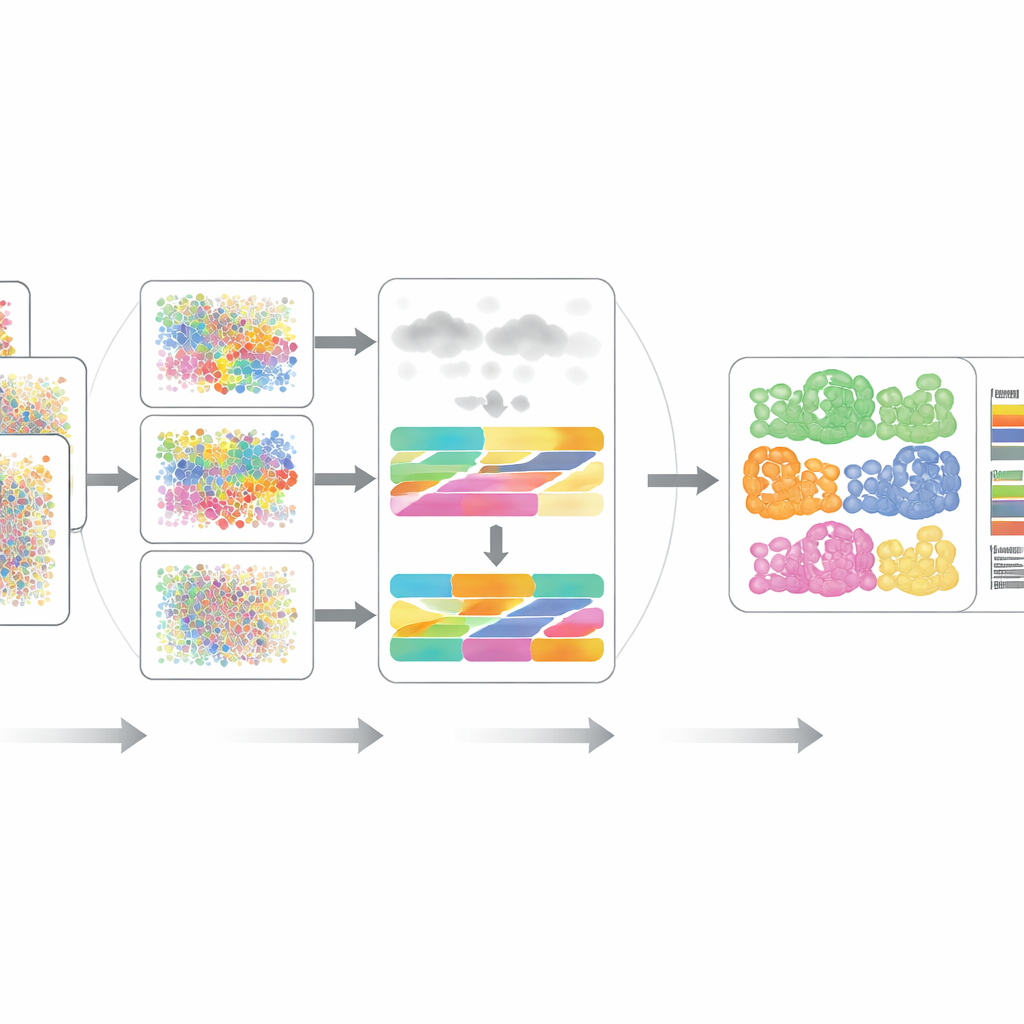
המבחן המעשי של DECODE
המחברים בחנו בקפדנות את DECODE על 15 מערכי נתונים המתפרסים על שבע תרחישים מציאותיים, כולל תורמים שונים, מצבי מחלה, מצבי בריאות, פלטפורמות ניסוי ואפילו מדידות מרחביות. בטרנסקריפטומיקה ובפרוטאומיקה, DECODE בדרך כלל התאפס או עלה על כלים מתקדמים מבחינת דיוק, תוך שמירה על זמן חישוב וזיכרון סבירים. באופן מכריע, DECODE הייתה השיטה היחידה שסיפקה תוצאות אמינות על נתוני מטבולומיקה, שבהם יש פחות תכונות וסוגי תאים יכולים להיראות דומים באופן מפתה. המסגרת הוכיחה גם יכולת מעקב אחרי מצבי תאים—כגון התקדמות לאורך מסלול התפתחותי, שלבי מחזור התא או תגובות לטיפול תרופתי—ולא רק סוגי תאים סטטיים.
עמידות בנתוני עולם‑אמיתי רועשים ולא שלמים
ברקמות אמיתיות לעתים קרובות יש סוגי תאים שלא נתפסו בהפניות של תאים בודדים במעבדה, ורעש ניסויי יכול לעוות כמה תכונות בבת אחת. החוקרים סימלו בעיות אלו על‑ידי הוספת סוגי תאים לא ידועים והכנסת מספר סוגי רעשים ונתונים חסרים בטרנסקריפטומיקה, פרוטאומיקה ומטבולומיקה. ברוב המקרים, DECODE נשארה השיטה המדויקת ביותר ובמטבולומיקה — השיטה היחידה שלא קרסה. הם גם הראו ש‑DECODE נותנת תשובות עקביות מאוד כאשר היא מיושמת על מדידות גנים וחלבונים תואמות מאותם דגימות תאי דם, דרישה מרכזית להשוואת שינויים בסוגי תאים בין שכבות אומיקס בקוהורטים גדולים.
תובנות ביולוגיות חדשות מקוהורטים מולטיאומיים
מצוידים בכלי המאוחד הזה, הצוות חזר על מערכי נתוני מחלות מורכבות. בסרטן השד, הם שילבו קוהורטים טרנסקריפטומיים ופרוטאומיים כדי להראות כיצד תאי חיסון ותאים סטרומליים תומכים משתנים בין גידולים שאינם מייצרים גרורות, גידולים ראשוניים מייצרי גרורות וגרורות במוח. דפוסים כמו ריבוי תאי T ותאים דמויי פריווסקולאריים בפגיעות לא‑מגרינות ועלייה בתאי B במצב מתקדם תואמים ומרחיבים מחקרים ביולוגיים קודמים. בכבד עכבר, DECODE שילבה קוהורטים טרנסקריפטומיים, פרוטאומיים ומטבולומיים כדי לעקוב כיצד הפטוציטים, תאי אנדותל ותאי חיסון מקומיים משתנים תחת דיאטות שונות ומודלים של מחלת כבד, ושיחזרה מגמות ידועות כמו עלייה בשיעור תאי Kupffer בתנאים דלקתיים.
מה משמעות הדבר לעתיד
לקורא שאינו מומחה, המסר המרכזי הוא ש‑DECODE מתפקדת כפריזמה חכמה לנתונים ביומדיציניים: בהתבסס על מדידות מעורבות מרקמות, היא יכולה להפריד את התרומות של סוגי תאים ומצבים רבים, ועושה זאת באופן אמין במספר סוגי מדדים מולקולריים. זה מאפשר למדענים לסחוט הרבה יותר מידע ממערכי מולטיאומיקס וביובנקים קיימים בלי לאסוף נתוני תאים בודדים חדשים עבור כל פרויקט. אף על פי שהשיטה עדיין תלויה באיכות ובטווח של התייחסויות תאים בודדים זמינות, ומשאבי מטבולומיקה מוגבלים עדיין, DECODE מסמנת צעד משמעותי לקראת פירוש שגרתי ברמת התא של מחקרים אנושיים בהיקף רחב, עם יתרונות פוטנציאליים להבנה של מנגנוני מחלה והכוונת רפואה מדויקת.
ציטוט: Zhao, T., Liu, R., Sun, Y. et al. DECODE: deep learning-based common deconvolution framework for various omics data. Nat Methods 23, 596–608 (2026). https://doi.org/10.1038/s41592-026-03007-y
מילות מפתח: דיקונבולוציה מולטיאומיקס, התייחסות תאים בודדים, למידה עמוקה בביולוגיה, ניתוח מטבולומיקה, הרכב סוגי תאים