Clear Sky Science · he
מחוונים רב-צבעוניים בדור הבא להדמייה בתוך הייצור של נוראפינפרין
לראות שליח מוח מוסתר
נוראפינפרין הוא מולקולה במוח שמעצב בשקט כיצד אנחנו מתעוררים, מתמקדים, בונים זיכרונות ומגיבים ללחץ. עד לאחרונה, מדענים יכלו רק להציץ בפעולתו באמצעות כלים איטיים או לא מדויקים. המאמר הזה מציג זוג סימנים זוהרים חדשים שמאפשרים לחוקרים לצפות בזרימה של נוראפינפרין במוח החי, בזמן אמת ובפרטים עדינים. התקדמות זו עשויה להעמיק את הבנתנו של שינה, חרדה, למידה ומחלות ניווניות.
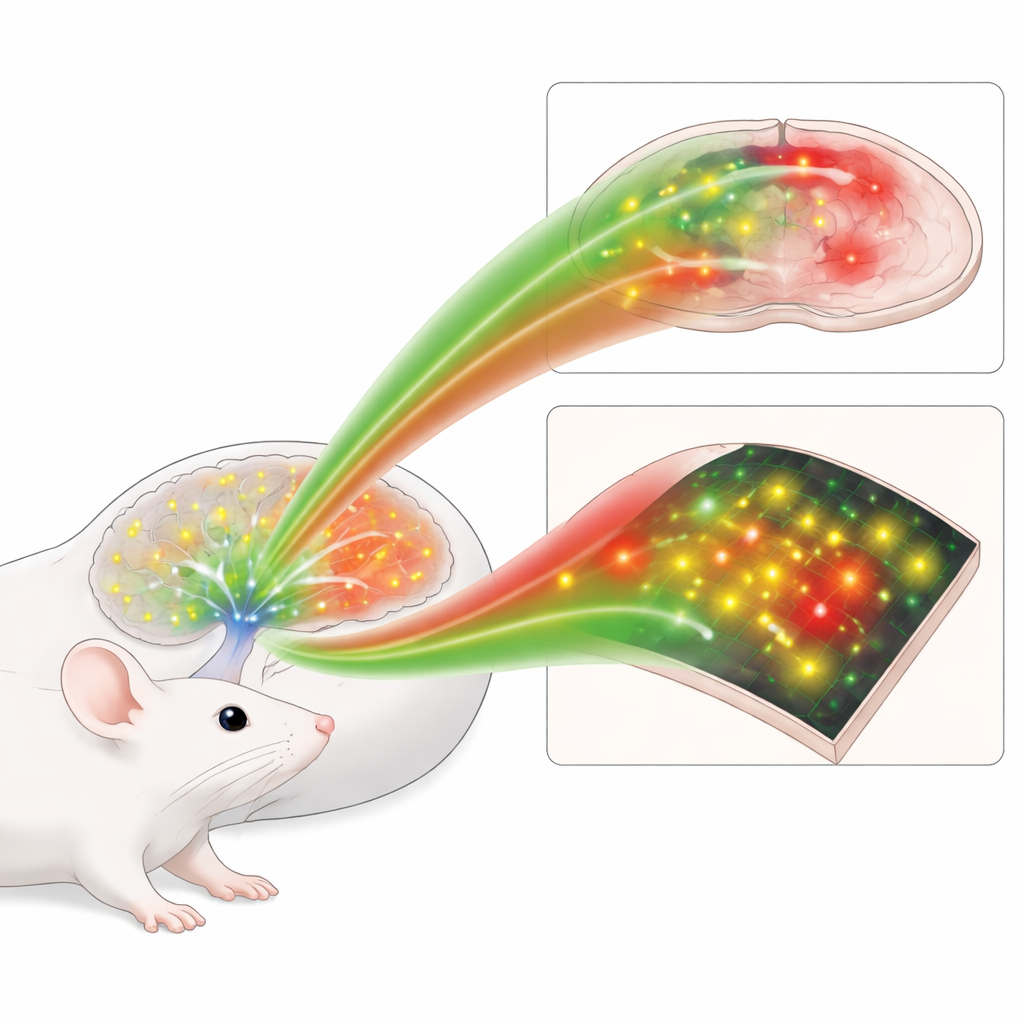
מדוע מעקב אחרי האות הזה היה כל כך קשה
נוראפינפרין משוחרר על ידי קבוצה קטנה של תאי גזע מוח שנשלחים סיבים ברחבי המוח, ומשנים את אופן הפעולה של מעגלים במקום פשוט להדליקם או לכבותם. שיטות מדידה קלאסיות, כגון זיהוי כימי קטן או תאים מושתלים שמגיבים לנוראפינפרין, מטשטשות אירועים לאורך שניות רבות או אינן מבחינות בבהירות בין מולקולה זו לחומרים קרובים. אסטרטגיה חדשה יותר משתמשת בקולטנים משונעים על פני התא שמבהירים כאשר הם נקשרים לנוראפינפרין, ומאפשרת קריאת אור. אבל הגרסאות מהדור הראשון היו יחסית עמומות, במיוחד בתחום האור האדום, ולא היו גמישות מספיק לניסויים שדרשו שילוב רב-צבעי.
בניית "כלבי שמירה" ירוקים ואדומים ברורים יותר
המחברים פיתחו חיישנים משופרים בירוק ובאדום, שנקראים nLightG2 ו-nLightR2, על ידי שילוב חלקים מחיישני דופמין ונוראפינפרין קודמים ובחינה שיטתית של עשרות מוטציות. השינויים האלה הפכו את החיישנים לבהירים הרבה יותר בנוכחות נוראפינפרין, בלי לשנות משמעותית את זוהר הרקע שלהם. בתרביות תאים, הכלים החדשים הראו תגובות גדולות יותר בכמה מונים לנוראפינפרין לעומת גרסאות קודמות, הגיבו בתוך עשרות מילישניות וחזרו למצב ההתחלתי בפחות משנייה. הם כמעט ולא הגיבו לחומרים מוחיים אחרים, כגון דופמין, ולא הפעילו את מסלולי האיתות הפנימיים של התאים — בדיקה בטיחותית חשובה שמבטיחה שהם צופים ולא משתתפים.
הוכחת העוצמה שלהם ברקמת מוח
בהמשך, הצוות הכניס את החיישנים לפרוסות מוח של עכבר והשתמש במיקרוסקופיית פוטון כפול, היכולה לראות לעומק הרקמה, כדי להשוות בין העיצובים הישנים והחדשים. כאשר נוראפינפרין נשפך על הרקמה או כאשר סיבים מקומיים הוערו חשמלית לשחרר אותו באופן טבעי, nLightG2 ו-nLightR2 יצרו הבזקי אור גדולים ונוחים לזיהוי הרבה יותר מאשר חיישנים קודמים. הכלים הירוק והאדום היו מהירים בדומה זה לזה, מה שאומר שבחירת הצבע כבר לא דורשת פשרה במהירות. הרגישות הגבוהה יותר אפשרה למאפיין היכן נוראפינפרין התפשט במרחב, במקום רק לדעת שהוא שוחרר אי שם בשדה הראייה.
צפייה במצבי מוח, פחד וניווט בפעולה
ההבטחה האמיתית של הכלים האלה נגלית בבעלי חיים חיים. באמצעות סיבים אופטיים דקיקים מאוד, המחברים שילבו את החיישן האדום של נוראפינפרין עם חיישן סידן ירוק המדווח על ירי תאי עצב. במרכז השינה של המוח ראו שפרצי פעילות בתאים המייצרים נוראפינפרין במהלך שינה עמוקה הובילו במקביל לעליות ברמות נוראפינפרין המקומיות, אירוע אחרי אירוע. באמיגדלה, אזור מוחי חשוב לרגש, החיישן הירוק של נוראפינפרין גילף כי צליל חסר-הרגלה החל לעורר עלייה מתמשכת בנוראפינפרין ברגע שהוא הוצמד לזעזוע קל, מה שמשקף חיזוק של זיכרונות פחד. בהיפוקמפוס, שעוזר למיפוי מרחב, החיישן האדום צולם יחד עם חיישן סידן של אסטרוציטים ירוקים בזמן שהעכברים רצו במסדרון וירטואלי תמורת תגמולי מים. שם פעילות אסטרוציטים בקרבת אתר הפרס הייתה מקושרת היטב לגלי נוראפינפרין מקומיים, רמז לדיאלוג בין הכימיקל הזה לתאי תמיכה במהלך חוויות מתגמלות.
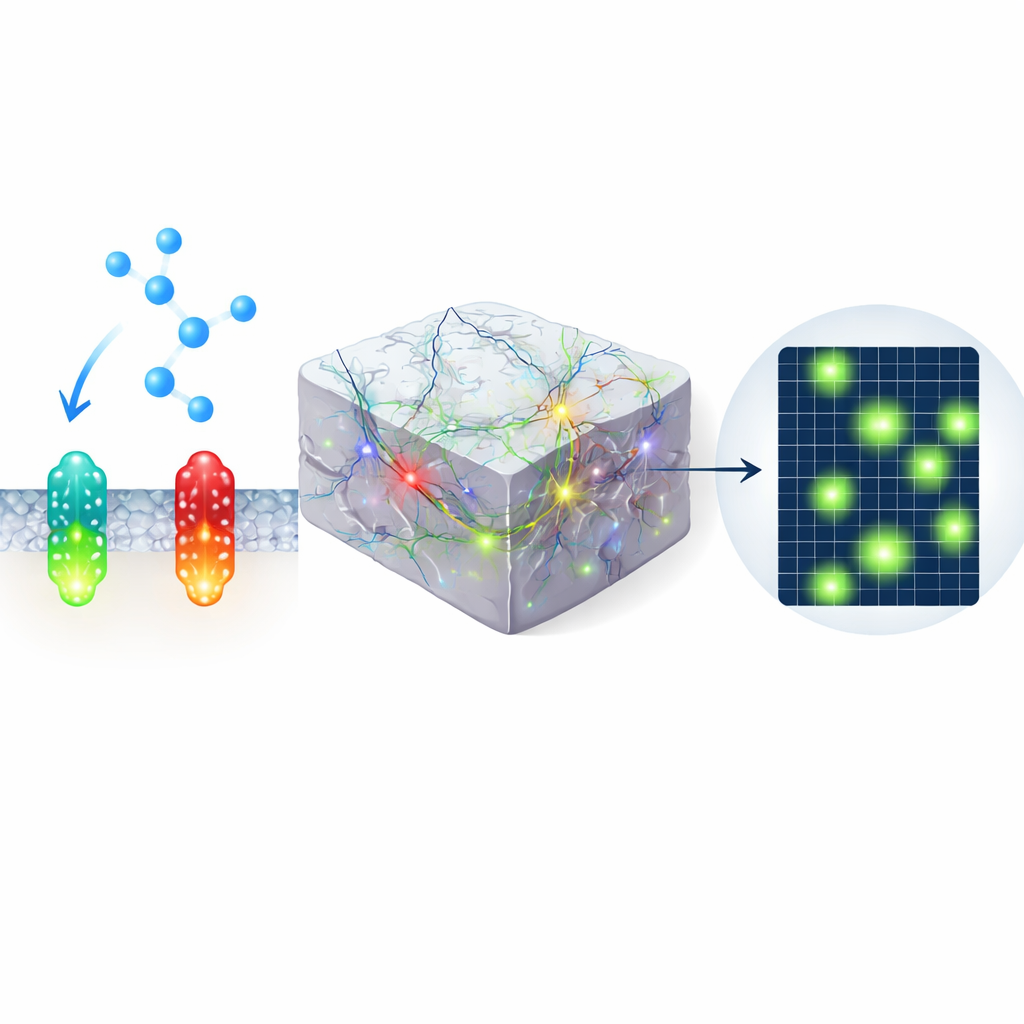
גילוי כיסי פעילות זעירים בקורטקס הראייה
בניסוי נוסף, המחברים הבעבירו את החיישן הירוק בקורטקס הראייה של עכברים ערים וצילמו אותו במיקרוסקופיית פוטון כפול בזמן שהבעלי חיים צפו בגירויים מתקרבים ועברו בין מנוחה לריצה. במקום שטף חלק של אות, הם מצאו חתיכות קצרות ומקומיות מאוד של פלואורסценציה מוגברת — מיקרודומיינים — מפוזרות בשדה הראייה. חלק מהמיקרודומיינים הגיבו בחיבה לאיום הוויזואלי, אחרים לתנועה, ורבים נדלקו ספונטנית. דפוסים אלה היו כמעט בלתי נראים בשימוש בחיישן ירוק ישן או בשליטת מוטציה שאינה קושרת, מה שמדגיש את הרגישות המשופרת של nLightG2 ומרמז שנוראפינפרין מעצב את פעילות המוח באופן הרבה יותר מדויק ודק ממה שחשבו עד כה.
מה משמעות הדבר למחקר מוח
ביחד, תוצאות אלה מראות ש-nLightG2 ו-nLightR2 מהווים ערכה חזקה לצפייה בנוראפינפרין במוח החי, בקנה מידה הנע ממיקרודומיינים בודדים ועד מצבים התנהגותיים שלמים. מאחר שהם קיימים בצבעים מובחנים וניתנים לשילוב עם מדווחים פלואורסצנטיים אחרים, מדענים יכולים כעת לעקוב אחרי נוראפינפרין לצד איתותים חשמליים או סידן בתאי סוגים ספציפיים, במהלך שינה, למידה או לחץ. היכולת לראות מתי והיכן המוודולטור הנוירוכימי הזה פועל עשויה בסופו של דבר להבהיר כיצד הוא תומך בקשב ובזיכרון בריאים, וכיצד הפגיעה בו תורמת למצבים כגון חרדה, דיכאון ומחלות ניווניות.
ציטוט: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
מילות מפתח: נוראפינפרין, נוירו-מודולציה, חיישנים המקודדים גנטית, הדמייה בפוטון כפול, שינה ולמידה