Clear Sky Science · he
בריחה אנטיגנית מולטי‑מודלית מאמצעי גיוס תאי T המכוונים ל‑GPRC5D במיאלומה נרקבת
כשסרטן עוקף אימונותרפיה מדויקת
תרופות אימונולוגיות עוצמתיות משנות את הטיפול במיאלומה נרקבת, סרטן דם שעדיין אינו נרפא ברוב המקרים. טיפולים אלה מפנים את תאי ה‑T של הגוף לזהות ולחסל תאי גידול המסומנים בדגלים ספציפיים על פני השטח. דגל מבטיח אחד הוא מולקולה הנקראת GPRC5D. אך, כמצופה בטיפולים ממוקדים רבים, הגידולים יכולים להתפתח ולהתחמק מהטיפול. המחקר הזה מפרט באופן יוצא דופן כיצד תאי המיאלומה משנים או מסתירים את דגל ה‑GPRC5D כדי להימנע מתרופות חזקות המושכות תאי T.
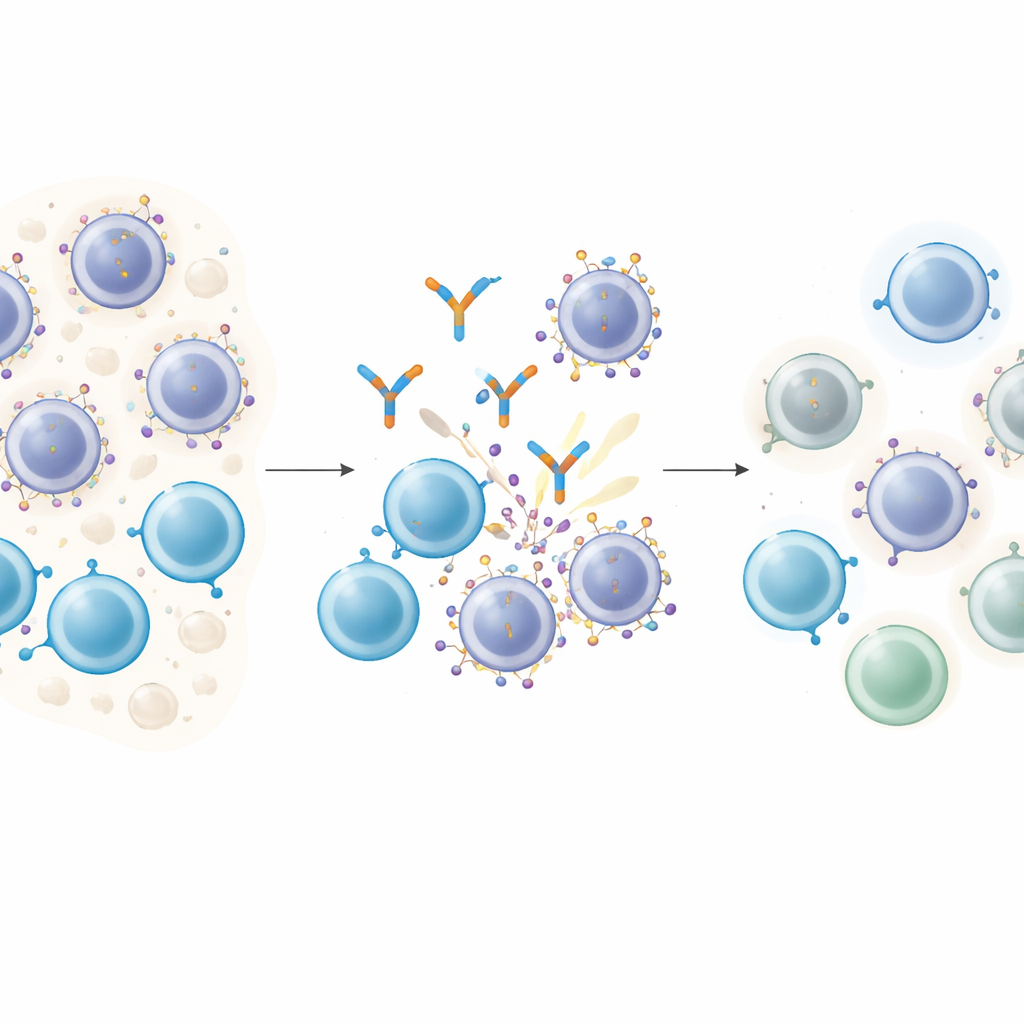
איך תרופות חכמות נצמדות לתאי הסרטן
נוגדנים המושכים תאי T פועלים כמו מצאני זוגות מולקולריים: קצה אחד תופס תא T, הקצה השני מתחבר למולקולה המטרה על תא הסרטני, ומקרב ביניהם במגע ישיר כדי שה‑T יוכל להרוג את המטרה. במיאלומה נרקבת, GPRC5D מהווה יעד אפקטיבי מכיוון שהוא רעיל על תאי פלזמה ממאירים אך נדיר ברקמות רגילות. מטופלים שקיבלו תרופה המכוונת ל‑GPRC5D בשם טלקואטמב (talquetamab) חווים לרוב רמיסיות עמוקות. עם זאת, כמעט כולם חווים בסופו של דבר החמרה, והשאלה הקריטית היא האם תאי הסרטן משנים את המטרה שעליה התרופות תלויות?
מעקב בזמן אמת אחרי אבולוציית הגידול
החוקרים עקבו אחר 21 חולים עם מיאלומה קשה שקיבלו טלקואטמב. הם אספו דגימות מועבר העצם לפני הטיפול בחלק מהמטופלים ואז שוב כאשר הסרטן חזר, ושילבו שכבות של ניתוח DNA, RNA וכרומטין כדי לבדוק את תאי הגידול. מבט מפורט מאוד זה חשף שבכ‑שני שלישים מהחולים שחזרו, הסרטן שינה את GPRC5D בצורה שהחלישה או חסמה את השפעת התרופה. באופן מרשים, כמה תת‑שכפולים עמידים — ענפים גנטיים מובחנים של הגידול — שגשגו לעיתים קרובות באותו אדם, והראו שאבולוציה לעבר בריחה יכולה לנוע במסלולים מרובים במקביל.
שלוש דרכים עיקריות בהן הגידולים מסתירים את המטרה
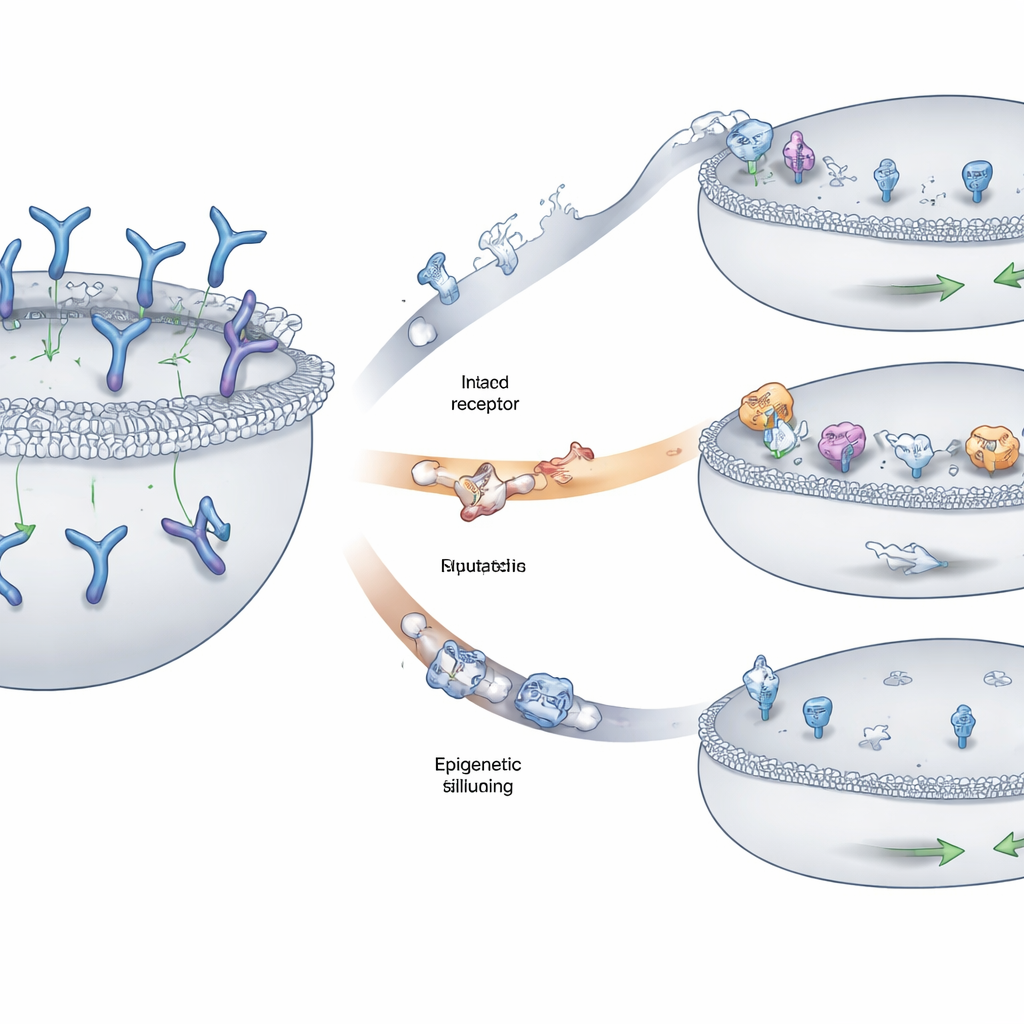
הצוות זיהה שלוש דפוסים חוזרים שבהם תאי מיאלומה נמנעו מזיהוי. אצל חלק מהמטופלים, חלקי הכרומוזום שנושאים את גן GPRC5D נמחקו בשני העותקים, ומחקו את הדגל לחלוטין מפני התא. באחרים, שינויים קטנים — החלפות אות בודדת ב‑DNA או הוספות ומחיקות זעירות — עיוותו אזורים מרכזיים של חלבון GPRC5D. רבים מהשינויים הללו הפריעו לחלקים של החלבון הדרושים לנסיעה תקינה מהחלק הפנימי של התא לממברנה החיצונית, וגרמו לכך ש‑GPRC5D נלכד במקטע פנימי במקום להיות מוצג שם שהתרופה תוכל לזהותו. מסלול שלישי כלל השתקה אפיגנטית: ה‑DNA המקיף את GPRC5D אורז באופן הדוק וסומן כימית כך שהגן נקרא בקושי, אף על פי שהרצף הבסיסי נותר ברובו שלם. תאי גידול המשתמשים באסטרטגיה זו ייצרו מעט או בכלל לא ייצרו GPRC5D.
כשהדגל קיים אך המפתח כבר לא מתאימה
לא כל דרכי הבריחה הסירו את GPRC5D מממברנת התא. במקרים מסוימים החלבון נראה תקין בבדיקות מעבדה סטנדרטיות אך כבר לא התאימה לתרופה כמו מפתח במנעול. הצוות שיחזר מוטציות ספציפיות המופקות מחולים בקווי תאים במעבדה ובדק עד כמה נוגדנים שונים המכוונים ל‑GPRC5D יכולים להיקשר ולהרוג תאים אלה. מוטציה אחת שינתה בעדינות את המקום המדויק שבו טלקואטמב אוחז בקולטן, ובלמה באופן חד את יכולת התרופה להיקשר ולהפעיל מוות תאי, אף על פי שהקולטן עדיין נראה בצביעה שגרתית. למרבה העניין, תרופה מכוונת אחרת ל‑GPRC5D, המחזיקה את הקולטן בשני אתרים, נשארה יעילה נגד כמה מהמוטנטים הללו, מה שמבליט כיצד עיצוב התרופה — למשל שימוש בקשירה מרובת ערך או מולטיאפיטופית — יכול להשפיע על הישרדות השכפולים העמידים.
מעבר למטרה: מגבלות נוספות להתקפת המערכת החיסונית
בעוד שרוב ההחמרות הראו צורה כלשהי של אובדן או שינוי ב‑GPRC5D, מיעוט מהמטופלים חזרו ללא שינויים ברורים במטרה עצמה. במקרים אלה הבעיה נראתה קשורה לתאי ה‑T: הם היו בעלי כושר פחות ונמוכי יכולת להרוג תאים סרטניים בבדיקות מעבדה, דבר המצביע על כך החשיפה הארוכה והמתמשכת לטיפול המושך עלולה לעייף את המערכת החיסונית. המחקר גם גילה כי תת‑סוג גנטי מסוים של מיאלומה (שכולל החלפת כרומוזומים בשם t(11;14)) שומר באופן טבעי על גן GPRC5D במצב כרומטין יותר "סגור", עם ביטוי בסיסי נמוך יותר. זה מעלה את האפשרות שחלק מהחולים עשויים להיות מועדים לתגובות חלשות מכיוון שהגידולים שלהם מתחילים עם רמות מדוכאות של דגל המטרה.
מה משמעות הממצאים למטופלים ולטיפולים עתידיים
עבור מטופלים ורופאים, עבודה זו מסבירה מדוע אפילו טיפולים חזקים המכוונים ל‑GPRC5D אינם עדיין ריפוי: תאי מיאלומה יכולים למחוק, לערבל, להסיט או להשתיק את הדגל שעליו התרופות נשענות, והם עושים זאת לעתים בכמה דרכים בו‑זמנית. הממצאים מצביעים על כך שמעקב אחרי DNA של הגידול, ולא רק מדידת רמות חלבון, יהיה חשוב לגילוי מוטציות בריחה מתפתחות שבדיקות שגרתיות עלולות לפספס. הם גם מכוונים לאסטרטגיות דור הבא — כגון תרופות המחברות ל‑GPRC5D ביתר חוזק במספר אתרים, קומבינציות הפוגעות ביותר ממטרה אחת בו‑זמנית, או סוכנים הפותחים מחדש גנים מושתקים — כדי להקדים את אבולוציית הגידול. במהות, המחקר ממפה את דרכי הבריחה שבהן משתמשת המיאלומה כדי שעיצובים טיפוליים עתידיים יוכלו לחסום אותן ולשמור על יעילות טיפולי תאי ה‑T לאורך זמן רב יותר.
ציטוט: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
מילות מפתח: מיאלומה נרקבת, גיוסי תאי T, GPRC5D, בריחת אנטיגן, אימונותרפיה לסרטן