Clear Sky Science · he
לינאוונקיברט ופמברוליזומאב בגידולים מוצקים מתקדמים עמידים לחסימת צירי חיסון: ניסוי שלב 1
מדוע סרטנים עקשניים חשובים לכולנו
תרופות אימונותרפיות שמביאות ל"הסרת הבלמים" מהמערכת החיסונית שינו את אופן הטיפול בהרבה סוגי סרטן, אך ברוב החולים או שמעולם לא זכו לתועלת משמעותית או שבסופו של דבר הגידולים שלהם חזרו לגדול. המחקר בוחן נוגדן חדש בשם לינאוונקיברט, שנועד לנטרל מגן חזק שהגידולים משתמשים בו כדי להתחבא מפני מתקפת מערכת החיסון, ומשלב אותו עם אימונותרפיה קיימת, פמברוליזומאב. התוצאות מציעות הצצה מוקדמת לכך שגם בחולים שסרטנם כבר חדל להגיב לתרופות חסימת צירים, ייתכן שניתן לשחזר שליטה חיסונית תוך שמירה על פרופיל תופעות לוואי סביר.
מגן נסתר סביב הגידולים
תרופות אימונותרפיות מודרניות רבות פועלות על ידי חסימת מולקולות "ציר" כמו PD‑1, שמגבילות את תאי T. כאשר הבלמים האלה מוסרים, התאים החיסוניים יכולים לתקוף את הסרטן בעוצמה רבה יותר. אך הגידולים לעיתים מתאימים את עצמם על‑ידי בניית שכונה עוינת סביבם שמונעת כניסת תאי T רוצחים או מחלישה אותם לאחר הגעתם. אדריכל מרכזי של בועה מגן זו הוא חלבון אותות הנקרא TGFβ1, המיוצר הן על‑ידי תאי הסרטן והן על‑ידי תאים תומכים בסביבה. ניסיונות מוקדמים לחסום את כל משפחת ה‑TGFβ הראו הבטחה אך נתקלנו בבעיות לב ודימום משמעותיות, מאחר שחברים אחרים במשפחה חשובים לרקמות בריאות. לינאוונקיברט תוכנן לנווט בין הסלע והמקום הסלעי על‑ידי ניטרול סלקטיבית של הצורה הלטנטית, הלא פעילה של TGFβ1 לפני שהיא מופעלת, תוך השארת מולקולות קרובות שהגוף זקוק להן ללא פגיעה.
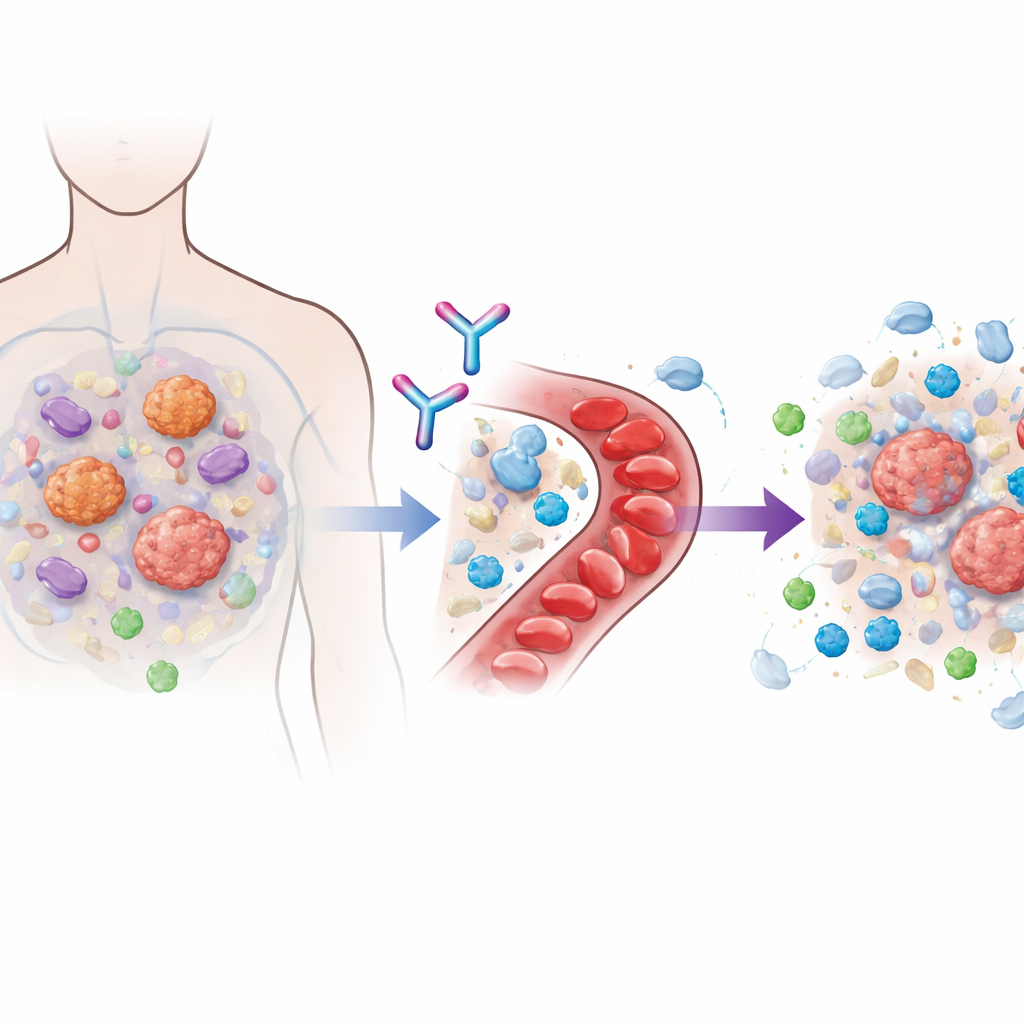
עיצוב ניסוי זהיר ראשון בבני אדם
ניסוי DRAGON היה מחקר רב‑מרכזי שלב 1 שנערך ב‑22 בתי חולים בארצות הברית ובקוריאה הדרומית. הוא גייס 112 מבוגרים עם גידולים מוצקים מתקדמים, שלכולם היו אופציות טיפול מוגבלות. בחלק הראשון של המחקר ניתנה לינאוונקיברט לבד במנות שעולות בהדרגה לקבוצות קטנות של חולים, או בשילוב עם תרופת PD‑1 קודמת שלהם. גישה צעד‑אחר‑צעד זו שימשה למיפוי בטיחות, פרמקוקינפטיקה ופרמקודינמיקה ובחירת מנה להמשך בדיקה נרחבת. בחלק השני, 78 חולים שסרטניהם כבר עמידו לפחות לשורת טיפול אחת מבוססת PD‑1 קיבלו מנה קבועה של לינאוונקיברט יחד עם פמברוליזומאב. חולים אלה סבלו מסוגי סרטן קשים לטיפול, כולל סרטן כליה בהיר תאי, מלנומה, סרטן ראש וצוואר, סרטן השתן (שלפוחית) וסרטן ריאה, ורובם עברו מספר טיפולים קודמים.
בטיחות ראשונה: מה קרה לחולים
המטרה העיקרית של ניסוי זה בשלב מוקדם הייתה בטיחות, ולינאוונקיברט הציג נתונים מעודדים בהיבט זה. בכל רמות המנה לא הושגה מנה מקסימלית מוסבלת, ולא נצפו תופעות לוואי קובעות מנה או מקרי מוות שיוחסו לתרופה. כאשר לינאוונקיברט שותף עם פמברוליזומאב במנת שלב 2, כשלושה רבעים מהחולים חוו תופעת לוואי כלשהי שקשורה לטיפול, בדומה למה שמתקבל לעיתים קרובות עם אימונותרפיה לבד. פריחות וגרד היו הבעיות הנוספות השכיחות ביותר, ומספר קטן של חולים פיתחו דלקות עור או ריאות חמורות יותר. באופן חשוב, לא תועד תגובת יתר חיסונית מסוכנת מסוג תסמונת שחרור ציטוקינים, אשר יכולה להתרחש עם חלק מהנוגדנים, ודפוס הבטיחות הכללי דמה ברובו לפרופיל של פמברוליזומאב לבדו.
רמזים לכך שניתן להחזיר את פעילות המערכת החיסונית
אף שזה לא היה ניסוי רחב ומכריע ביעילות, מספר סימנים הציעו כי חסימת TGFβ1 עשויה לסייע בהחזרת תגובות לחסימת PD‑1. בשלב ההרחבה, השילוב לינאוונקיברט–פמברוליזומאב הקטין גידולים מדידים בחלק ניכר מהחולים שבעבר הפסיקו להרוויח מתרופות PD‑1. שיעורי תגובה מאומתים היו 20% בסרטן כליה בהיר תאי, 18.2% במלנומה, וכמעט מעל 9% בסרטן ראש וצוואר ובסרטן השופכה, כאשר מטופל אחד עם סרטן כליה הגיע להיעלמות מלאה של המחלה הנראית לעין. תגובות רבות אלו נמשכו חודשים רבים, והחולים שהגיבו בדרך כלל נשארו על השילוב תקופה ארוכה יותר מאשר על הטיפול הקודם ב‑PD‑1. ביופסיות שנלקחו לפני ואחרי הטיפול סיפקו הסבר ביולוגי: הגידולים הראו חדירה מוגברת של תאי CD8 "הרוצחים", רמות גבוהות יותר של תאים מופעלים, פחות תאי רגולציה מדכאים ותאים מיואימיים, ומעבר כללי לסביבה דלקתית יותר המוכנה לתקיפה.
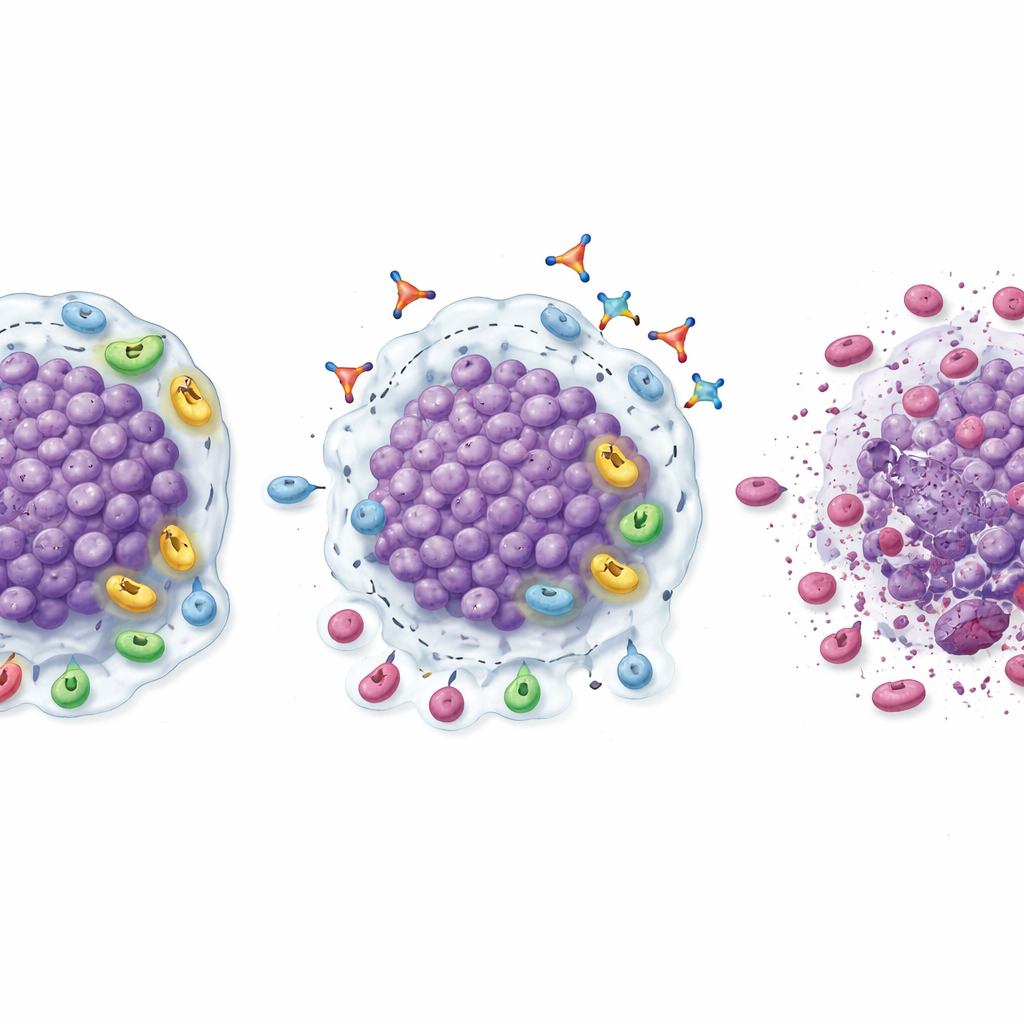
איתור מי עלול להרוויח הכי הרבה
החוקרים גם בדקו אילו חולים עשויים להיות מועמדים לתגובה. בסרטן כליה בהיר תאי, גידולים שכבר הכילו ברמה בסיסית תאי CD8 רבים—אך היו גם עשירים בתאי רגולציה וביטאו רמות גבוהות של TGFβ1—היו יותר בני ברית להקטנה על הטיפול המשולב. בקרב חולים אלה, שיעורי תגובה והישרדות ללא התקדמות היו גבוהים משמעותית מהקבוצה הרחבה יותר של סרטן הכליה. דגם זה מציע "נקודת מתיקות": גידולים שבהם יש חיילים חיסוניים רבים אך הם מונעים על‑ידי דיכוי מונע‑TGFβ1 עשויים להיות מועמדים אידיאליים ללינאוונקיברט יחד עם חסימת PD‑1. אם יאומת במחקרים גדולים יותר, בדיקות פשוטות של רקמות לסמנים אלה יכולות לסייע לרופאים לבחור חולים הסבירים להפיק תועלת.
מה משמעות העבודה הזאת להמשך
לאנשים המתמודדים עם סרטן מתקדם שכבר עמד בעמידות לאימונותרפיה, האפשרות לשקם את כוחה של מערכת החיסון שלהם מבלי להוסיף רעילות קשה היא מושכת. ניסוי ראשון זה בבני אדם מספק ראיות מוקדמות שנטרול סלקטיבי של מגן TGFβ1 באמצעות לינאוונקיברט ניתן לבצע בבטחה ועשוי להשיב שליטה משמעותית על הגידול כאשר הוא משולב עם מעכב PD‑1, במיוחד בחלק מסוגי סרטן הכליה. בעוד שהמחקר היה קטן ואינו אקראי, רשומת הבטיחות שלו, התוצאות הביולוגיות והתגובות הארוכות יחד בונות טיעון חזק לניסויים מתקדמים יותר שלב 2. אם מחקרים עתידיים יאשרו את הממצאים, גישה זו עשויה להרחיב את מעגל החולים שיכולים להרוויח מאימונותרפיה ולהפוך חלק מהסרטן העקשני כיום לגידול שניתן שוב לפגוע בו באמצעות ההגנות הטבעיות של הגוף.
ציטוט: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
מילות מפתח: אימונותרפיה של סרטן, עיכוב TGFβ1, התנגדות לחסימת צירי חיסון, סרטן כליה בהיר תאי, מיקרו‑סביבת הגידול