Clear Sky Science · he
נוף דלקתי מובן של תאי החיסון במחזור הדם
מדוע דלקת בדם חשובה עבורך
הדלקת נמצאת בלב של מחלות רבות, מדלקת מפרקים ואסטמה ועד COVID-19 וסרטן. עם זאת, הרופאים עדיין נאבקים בקריאת אותות הדלקת של הגוף בצורה שמסבירה באופן ברור מה משתבש ואיזה טיפול יהיה היעיל ביותר. המחקר הזה בונה "מפה" ענקית של תאי חיסון הנעים במחזור הדם ומראה כיצד תאים אלה עשויים לשמש כסמנים ביולוגיים חיים וקל להתאמה שיכולים לסווג מגוון רחב של מחלות דלקתיות.
בניית מפה ענקית של תאי חיסון
כדי למפות נוף זה, החוקרים ניתחו יותר מ‑6.5 מיליון תאי חיסון שנלקחו מדמם של 1,047 אנשים. המתנדבים כללו 19 מצבים, בין היתר מחלות אוטואימוניות כגון לזומוס ודלקת מפרקים שגרונית, מחלות ריאות כרוניות כמו אסטמה ו‑COPD, זיהומים כגון COVID-19 ו‑HIV, ומספר סוגי סרטן, לצד תורמים בריאים. באמצעות ריצוף RNA תא‑יחיד הם מדדו אילו גנים דלוקים בכל תא בנפרד, ואז השתמשו בשיטות סטטיסטיות מתקדמות כדי לתקן הבדלים טכניים בין המחקרים ולקבץ תאים ל‑64 מצבי תא ייחודיים. "אטלס הדלקת" הזה כוללת גם שחקנים מוכרים — כגון תאי T, תאי B ומונוציטים — וגם תת‑סוגים מיוחדים שמשתנים עם המחלה.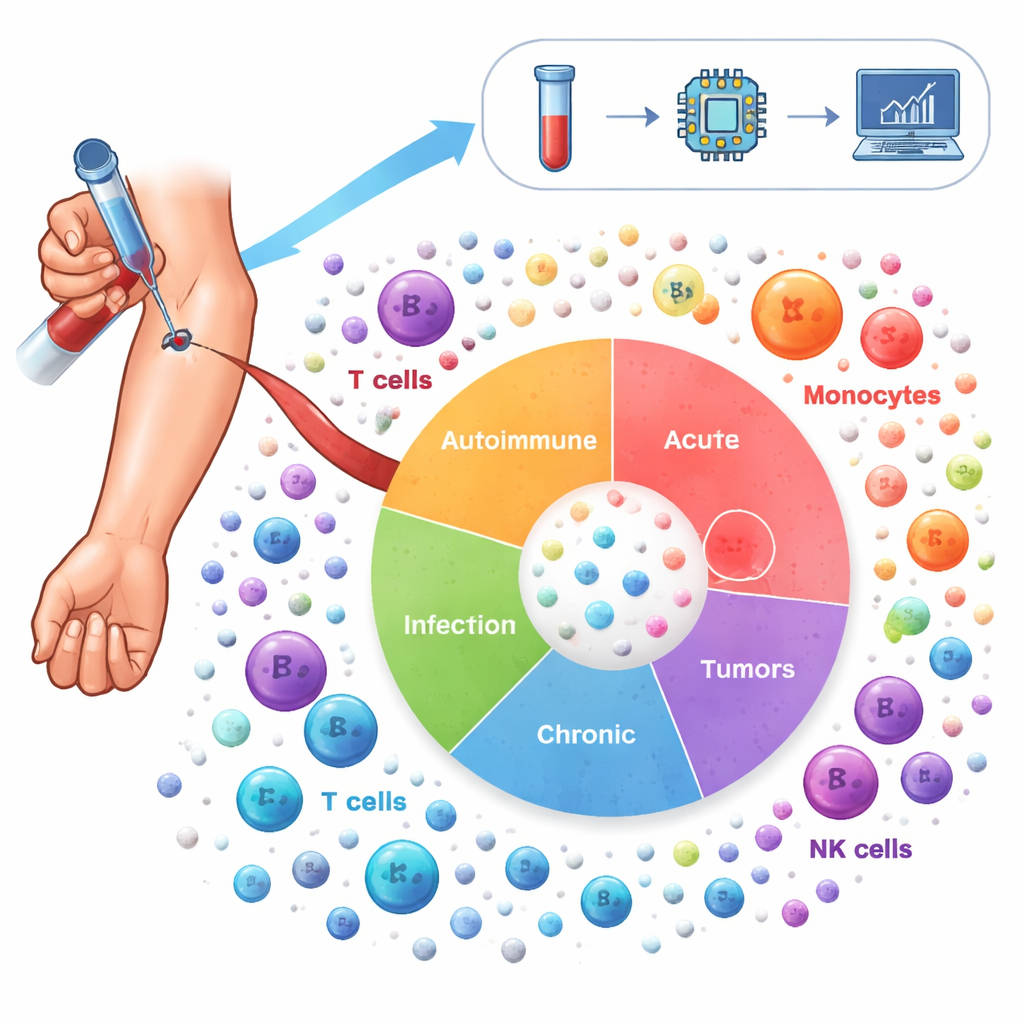
קריאת חתימות הדלקת של הגוף
הצוות התמקד לאחר מכן בגנים ששולטים כיצד תאי החיסון מפעילים את עצמם, נעים בגוף, מציגים אנטיגנים ומגבירים תגובות מול מולקולות איתות כמו אינטרפרונים וגורם נמק גידולים. הם קיבצו גנים אלה ל‑21 "חתימות" ביולוגיות ושיפרו אותן עבור כל סוג תא מרכזי. על ידי השוואת חולים לתורמים בריאים הם יכלו לראות אילו חתימות מוגברות או מדוכאות במחלות שונות. לדוגמה, מחלות דלקתיות חיסוניות רבות הראו פעילות מוגברת של מולקולות הדבקה ומכונות הצגת אנטיגן, בעוד תגובות אינטרפרון היו מדוכאות ברוב סוגי התאים אך מוגברות בכמה תאי T מסוג CD8. זיהומים ויראליים כמו שפעת ו‑COVID‑19 הגבירו תוכניות מונעות אינטרפרון, בעוד זיהומים כרוניים כמו HIV והפטיטיס B החלישו אותן.
התמקדות בגנים מרכזיים ובמפסקים בקרה
מכיוון שחתימות רחבות מסתירות עדיין פרטים חשובים, החוקרים התעמקו לגנים בודדים ולמוסדריהם. בתאי CD8 שאינם נאיביים הם מצאו ששני גנים, FGFBP2 ו‑GZMB, פעילים במיוחד בתתי־סוגים ספציפיים של זיכרון אפקטורי, במיוחד במחלת קוליטיס כיבית. גנים אלה קושרו לנזק במשטחי אפיתל, והאות החזק שלהם בדם מרמז שתאים תוקפניים אלה כבר מוכנים לפני שהם מגיעים לרקמות. ניתוח נפרד של רשתות ויסות גנטי הדגיש שני גורמי שעתוק, STAT1 ו‑SP1, כבודדים מרכזיים בתוכניות המופעלות על‑ידי אינטרפרון. דפוסי הפעילות שלהם השתנו בין מחלות וסוגי תאים — למשל, התנהגות מנוגדת במונוציטים מול תאי CD8 בלקות ולניסים ושינויים בין שלבי התלקחות וללא התלקחות — ומרמזים כיצד אותם מסלולים יכולים להיות מגינים בהקשר אחד ומזיקים בהקשר אחר.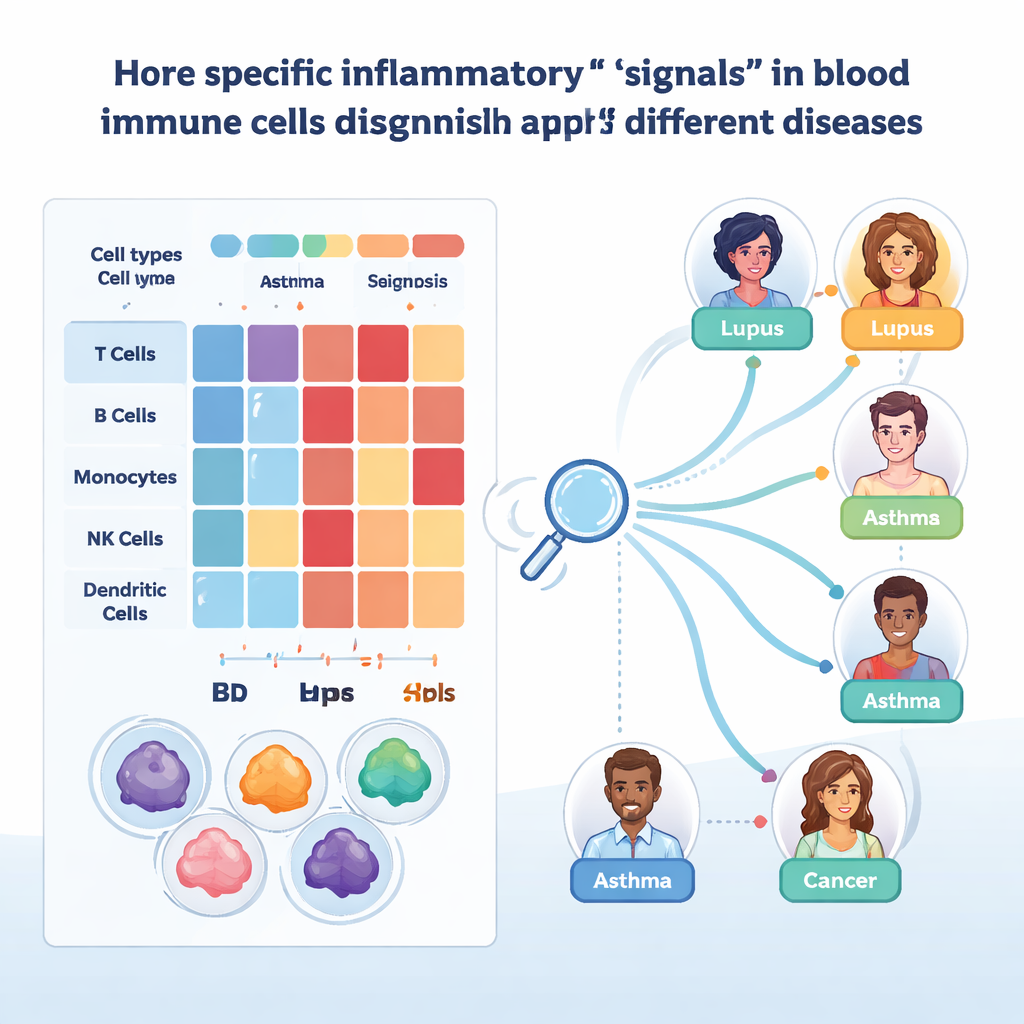
אימון מכונות לזיהוי מחלה מתוך תאי הדם
כדי להפוך את האטלס לכלי מעשי, הצוות השתמש בלמידת מכונה מובנת. הם אילפו מודלים של עצי החלטה משודרגים (gradient‑boosted) בנפרד לכל סוג תא עיקרי, וביקשו מהאלגוריתמים לתייג תאים בודדים לפי המחלה המתאימה על סמך ביטוי הגנים שלהם. מודלים אלה הגיעו לדיוק גבוה כאשר נבחנו על מדגמים שהוחזקו מחוץ לאימון, במיוחד לאחר תיקון להבדלים טכניים. בעזרת SHAP, שיטה שמסבירה אילו גנים מניעים כל החלטה, החוקרים יכלו לזהות סמנים מועמדים. דוגמה אחת היא CYBA במונוציטים, שרמותיו סייעו להבחין בין מחלות עור כגון פסוריאזיס לדלקת מעי בקרוהן ובקוליטיס כיבית. דוגמה נוספת היא IFITM1 בכמה תאי T ותאי לימפוייד קדומים, המבדילה אסטמה מ‑COPD ומרמזת על דפוסים שונים של הגנה אנטי‑ויראלית כרונית.
לעבר קומפאס אבחוני מבוסס דם
לבסוף, המחברים בדקו האם ניתן לסווג מטופלים שלמים — לא רק תאים בודדים — מתוך פרופילים חיסוניים במחזור הדם שלהם. הם הקרינו כל נתון של תא לחלל "הטמעה" מצומצם, חישבו ממוצעים של הטמעות אלה לפי סוג תא לכל מטופל, ואילפו מסווגים לחזות מחלה. כאשר מטופלים חדשים דמו לאלה שבנתוני האימון, הביצועים היו מצוינים. אך כאשר המדגמים הגיעו ממחקרים עצמאיים לחלוטין המשמשים בשיטות מעבדה שונות, הדיוק ירד באופן חד, מה שמצביע על רגישות כלים אלה לשונות טכנית. מאגר נתונים "מרוכז" מבוקר יותר, שנוצר במרכז אחד עם כימיה של ריצוף אחידה, השיב חלק גדול מהביצועים, מה שמצביע על הצורך בפרוטוקולים סטנדרטיים או במערכי אימון מאוד גדולים ומגוונים.
מה המשמעות של זה לאבחון וטיפול בעתיד
להסבר רפואי כללי, המסר המרכזי הוא שתאי החיסון במחזור הדם נושאים טביעת אצבע עשירה של אופן הדלקת בגופך. בקריאת טביעות אצבע אלה תא אחר תא, עבודת מחקר זו מראה שניתן להבחין בין מחלות רבות, לגלות גנים שעשויים להניע תסמינים ספציפיים ולהתחיל לבנות בדיקות דם אוניברסליות שיסווגו מחלות דלקתיות. המחקר עדיין אינו מבחן קליני מוכן לשימוש — הבדלים טכניים בין מחקרים מגבילים עדיין את האמינות — אך הוא מניח את היסודות לכלי "ביופסיה נוזלית" עתידיים שיכולים לסייע לרופאים לזהות את האבחנה והטיפול המתאימים מוקדם יותר, באמצעות משיכת דם פשוטה.
ציטוט: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
מילות מפתח: דלקת, תאי חיסון, ריצוף RNA תא-יחיד, סמנים ביולוגיים, למידת מכונה