Clear Sky Science · he
התועלת הקלינית במציאות של פרופיל גנומי מקיף בגידולים מוצקים מתקדמים
מדוע קריאת בדיקות DNA יכולה לשנות את הטיפול בסרטן
רופאים נעזרים יותר ויותר בבדיקות DNA עוצמתיות כדי לסרוק גידולים עבור מאות שינויים גנטיים בבת אחת, בתקווה להתאים לכל מטופל תרופה שמכוונת במדויק את הסרטן שלו. עם זאת, מחוץ לניסויים קליניים לא תמיד היה ברור עד כמה אסטרטגיה זו מאריכה בפועל את חיי החולים. מחקר זה בוחן יותר מ-54,000 אנשים עם סרטן מתקדם ביפן ומעלה שאלה פשוטה אך חשובה: כאשר אנו מבצעים פרופיל גנומי מקיף של הגידול, כמה תועלת ממשית מקבלים החולים בפועל?
מסתכלים מתחת למכסה של אלפי גידולים
החוקרים השתמשו במאגר נתונים ארצי שמתעד גם מידע גנטי וגם מידע קליני עבור מטופלים שעברו פרופיל גנומי מקיף (CGP) כחלק מהטיפול השגרתי. כל המטופלים סבלו מגידולים מוצקים מתקדמים וסיימו ברובם טיפולים סטנדרטיים. באמצעות בדיקה אחת שממפה 324 גנים קשורים לסרטן, הצוות תיעד אילו מוטציות היו קיימות וכמה חזקות הראיות לכך שכל מוטציה ניתנת למיקוד על ידי תרופה קיימת או טיפול נתמך היטב. הם קיבצו ממצאים מהרמות המבוססות ביותר (רמת ראיות A) ועד אלה הנתמכים רק בעבודה מעבדתית מוקדמת (רמה E) או ללא קישור קיים לטיפול.
התאמות גנטיות והישרדות: מי יוצא נשכר?
בכל הסוגים של סרטן, כמעט שלושה רבעים מהחולים נמצאו עם לפחות שינוי גנטי אחד שהמומחים מחשיבים כ"ניתן לפעולה" – משהו שעשוי לכוון את הטיפול. אלה שלגידוליהם היו סמנים ברמת הראיות החזקה ביותר (רמה A) נטו, בממוצע, לחיות יותר מאשר חולים שלגידוליהם היו רק סמנים חלשים יותר או ללא סמנים כלל. למשל, אנשים עם ממצאי רמה A הקשורים לתרופות שאושרו כבר חוו הישרדות חציונית של בערך 16 חודשים לאחר הבדיקה, לעומת כ-12 חודשים לחולים שממצאיהם היו פחות אינפורמטיביים. דפוס זה התקיים בכמה סרטרים, כולל ריאות, דרכי מרה ורחם, מה שמרמז כי מציאת יעד בעל אמינות גבוהה יכולה לתרגם לתוצאות טובות יותר גם בפרקטיקה היומיומית. 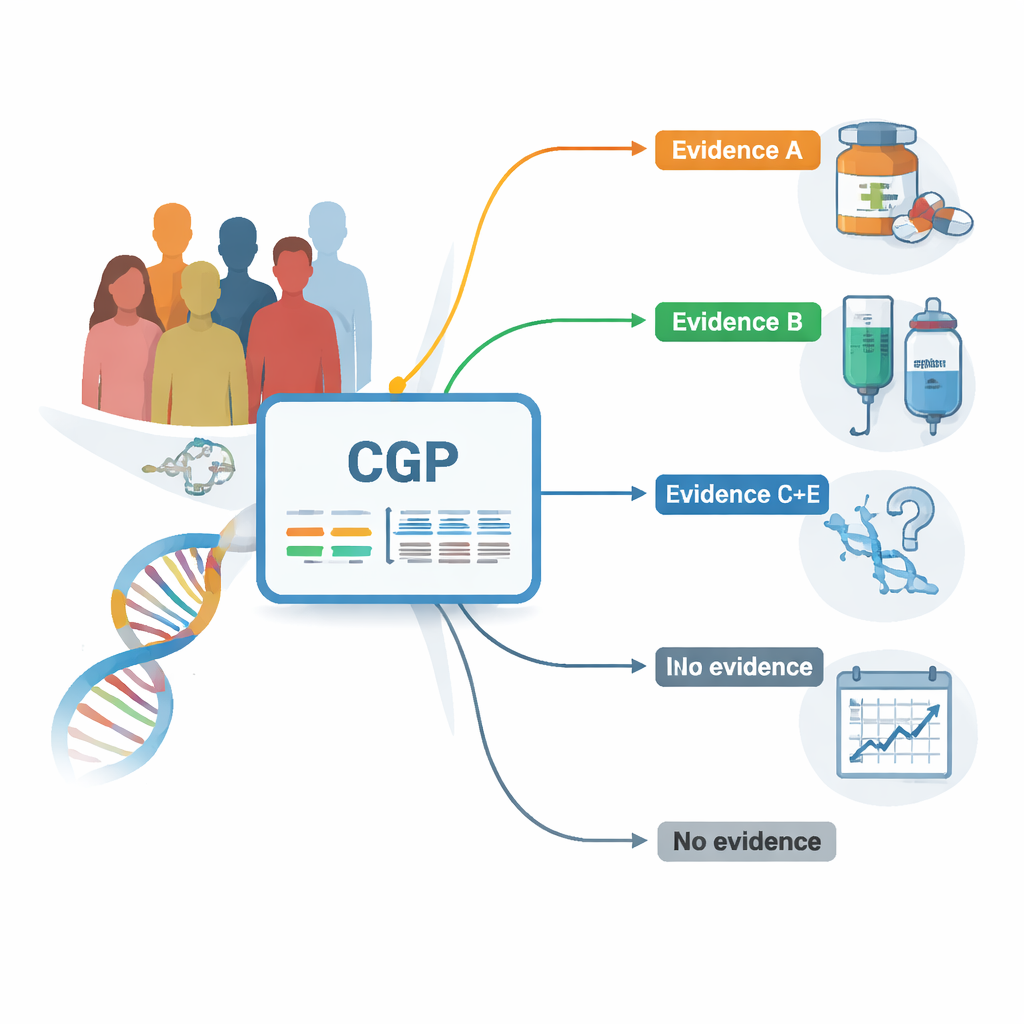
ממורטט מבטיח לתרופה בפועל
עם זאת, קיום יעד טוב בגידול וקבלת תרופה מתאימה התגלו כשתיים שונות לגמרי. רק כ-8% מכלל החולים המשיכו לקבל טיפול שהונחה בצורה ברורה על ידי תוצאות ה-CGP שלהם — או תרופה מדויקת מאושרת או טיפול ניסיוני בניסוי קליני או שימוש מחוץ לתווית. מחסומים כללו גיל מבוגר, מצב בריאותי כללי ירוד, והעובדה הפשוטה שאין תמיד ניסויים קליניים מתאימים או תרופות זמינות לכל מוטציה. החלק של החולים שזכו לתועלת עלה עם הזמן כשעוד תרופות מדויקות אושרו, אך היו הבדלים גדולים בין סוגי הסרטן: יותר מאשר אחד מכל חמישה חולים עם סרטן בלוטת התריס או ריאות קיבל טיפולים מונחי-CGP, בעוד שהשיעור נשאר מתחת ל-2% בסרטן הלבלב והכבד.
כשמידה אחת לא מתאימה לכולם
המחקר התרכז גם בסמנים "חוצי-גידולים" (tumor-agnostic), שלכאורה אמורים לפעול במספר סוגי סרטן. דוגמה מרכזית היא עומס המוטציות הגידולי (TMB), ספירה של כמה שינויים ב-DNA יש בגידול. חולים עם TMB גבוה מאוד — במיוחד 20 מוטציות או יותר למיליון אותיות DNA — נטו להגיב טוב יותר ולחיות זמן רב יותר לאחר טיפול באימונותרפיה המבוססת על פנברוליזומאב (pembrolizumab), ללא תלות בסמן אחר בשם חוסר יציבות מיקרו-לווינית (MSI). עם זאת, היו יוצאים מן הכלל בולטים. בסרטן עור נדיר המכונה מחלת פאגט אקסטראממארית, גם גידולים עם TMB גבוה התנגדו לפמברוליזומאב והחולים חוו תוצאות גרועות יותר, מה שמזהיר שמאסקר "אוניברסלי" עלול להיכשל בהקשרים ספציפיים. הצוות גם הראה שלא כל פיוזיות ה-DNA הכוללות את גני NTRK מגיבות באופן שווה לתרופות חוסמות TRK, וכי כמה חולים שבדיקות ישנות ומוגבלות יותר פספסו מוטציות מפתח עדיין הרוויחו כאשר ה-CGP זיהה אותן מאוחר יותר. 
מה המשמעות לחולים ולרופאים
לאנשים עם סרטן מתקדם, מחקר זה מציע הן תקווה והן ריאליזם. CGP מסייע בבירור חלוקה לקבוצות עם סיכויים טובים או גרועים יותר ויכול לחשוף אפשרויות טיפול עוצמתיות, במיוחד בגידולים מסוימים ובמקרים של סרטן עשיר במוטציות. יחד עם זאת, רוב החולים שהיו להם ממצאים "ניתנים לפעולה" עדיין אינם מקבלים תרופה מותאמת, בשל מגבלות באישורי תרופות, גישה לניסויים ומצב בריאותי. המסר הוא שבדיקת DNA רחבה היא כלי חשוב — אך התועלת האמיתית שלה תלויה בזמינות התרופות, הניסויים ומערכות הטיפול הנכונות כדי לפעול על בסיס ממצא הבדיקה.
ציטוט: Saito, Y., Horie, S., Kogure, Y. et al. Real-world clinical utility of comprehensive genomic profiling in advanced solid tumors. Nat Med 32, 690–701 (2026). https://doi.org/10.1038/s41591-025-04086-8
מילות מפתח: אונקולוגיה מדויקת, פרופיל גנומי, עומס מוטציות גידוליות, טיפול ממוקד, אימונותרפיה