Clear Sky Science · he
תבוננות מרחבית של איתות TGFβ בפיברובלסטים כמקור לעמידות לטיפול בדלקת פרקים שגרונית
למה כאב מפרקים עיקש חשוב
רבים מהאנשים עם דלקת פרקים שגרונית נוטלים תרופות מודרניות המרגיעות את המערכת החיסונית, אך מפרקיהם נשארים כואבים ונוקשים. המחקר הזה שואל מדוע חלק מהמטופלים לא משתפרים גם כאשר נראה שהדלקת במפרק דועכת. באמצעות בחינה מדוקדקת של המקום והאופן שבו תאים תומכים מסוימים במפרק מדליקים תוכניות ייצור צלקת, החוקרים חושפים צורת נזק נסתרת שעשויה להסביר את הכאב המתמשך ולהצביע על אסטרטגיות טיפול חדשות.
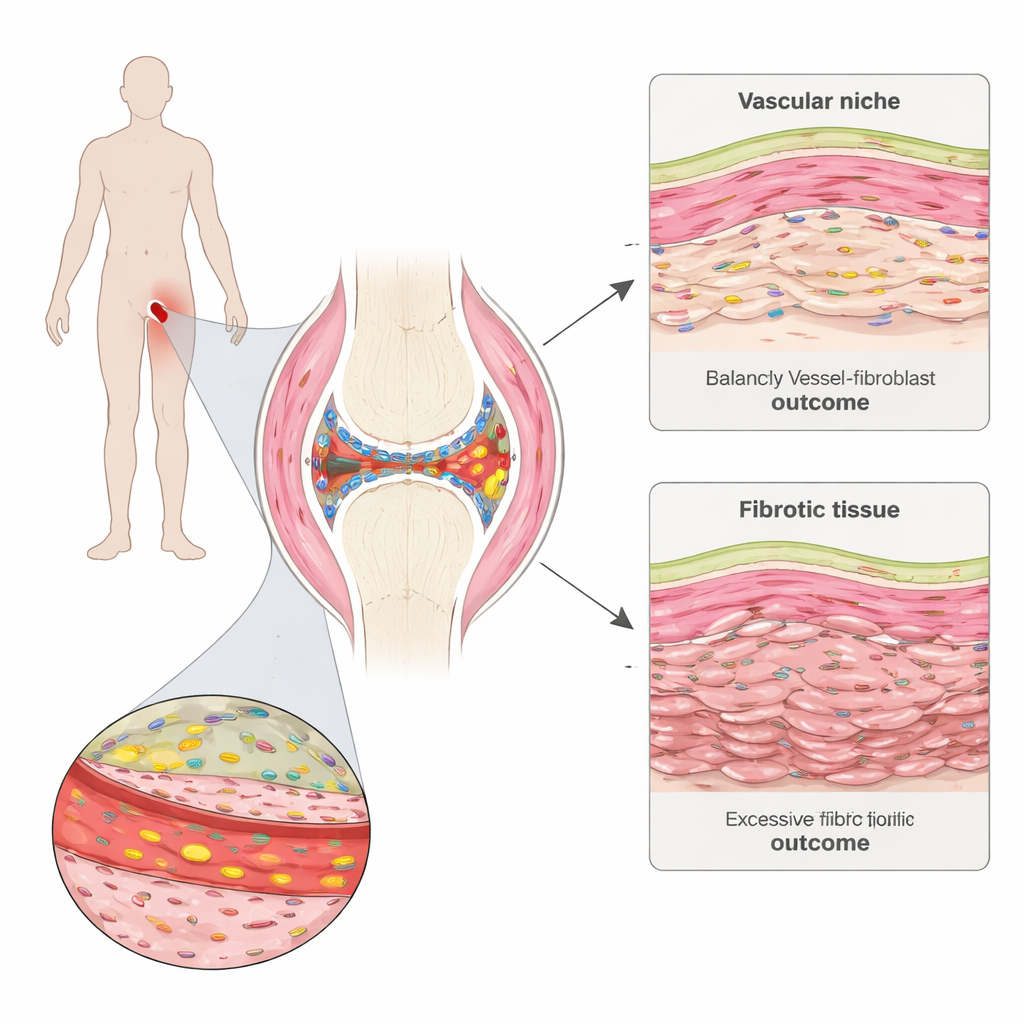
מבט מקרוב לתוך המפרק הכואב
דלקת פרקים שגרונית תוקפת את הסינוביה, רקמה דקה שמצפה ומשמן את המפרקים. הצוות אסף ביופסיות סינוביאליות זעירות מאנשים עם מחלה מוקדמת לפני תחילת הטיפול ושוב לאחר שישה חודשים. באמצעות מיפוי גנים מרחבי מתקדם הם יכלו לראות אילו גנים פעילים במאות־אלפי תאים אינדיבידואליים תוך שמירה על מיקום התאים ברקמה. הם זיהו "שכונות" מובחנות בסינוביה, כולל אשכולות של תאים חיסוניים, אזורים עשירים בשומן, המעטפת הדקה הפנימית ואזורי כלי דם מרופדים בתאים מבניים הנקראים פיברובלסטים.
תאי ייצור צלקת ועמידות לטיפול
בהשוואה בין מטופלים שהשיגו רמיסיה לאלה שלא, החוקרים מצאו דפוס בולט: עוד לפני הטיפול, למטופלים שלא היכו ברמיסיה היו כבר אותות חזקים יותר של יצירת צלקת רקמתית, או פיברוזיס. תוכנית פיברובלסטית מסוימת, המסומנת על ידי ייצור גבוה של חלבון מטריקס חוץ‑תאי בשם COMP, הייתה מורחבת אצל מטופלים אלה. פיברובלסטים עשירים ב‑COMP שיתפו תכונות עם תאי צלקת הנראים בפיברוזיס ריאתי ועורי והיו מקושרים במיוחד לתגובה גרועה לטיפול. עם הזמן, אזורים שדומיינו על ידי תאים אלה נטו להפוך לדחוסים בסיבים חיבוריים יחסית דלים בתאים, מה שמרמז שהם משאירים מאחורי מטריצה קשיחה שיכולה להתקיים גם לאחר שהדלקת שקטה.
כלי דם כמוליכים נחבאים
הפיברובלסטים הפיברוגניים לא היו מפוזרים באקראי. הם הצטברו סביב כלי דם, ויצרו אזורי פרי‑ווסקולר שכבתיים. השכבה הפנימית, הדבוקת לקיר הכלי, הביעה גנים שונים משכבת החוץ. הצוות הראה שתאים המרפדים את כלי הדם שולחים אותות נוטץ׳ לפיברובלסטים הסמוכים, אשר בתורם מעצבים את אופן התגובה של פיברובלסטים למשפחת אותות המעודדות צלקת הידועה כ‑TGF‑בטא. בקרבת הכלי, איתות נוטץ׳ דוחף את הפיברובלסטים לייצר TGF‑בטא אך במקביל מוריד את מספר קולטני ה‑TGF‑בטא על פני השטח שלהם, וכך שומר על הרגישות שלהם בבדיקה. רחוק יותר, שם השפעת נוטץ׳ דועכת, לפיברובלסטים יש יותר קולטנים והם הופכים לרגישים מאוד, ומתפתחים לתאי COMP‑עשירים שמניעים פיברוזיס.
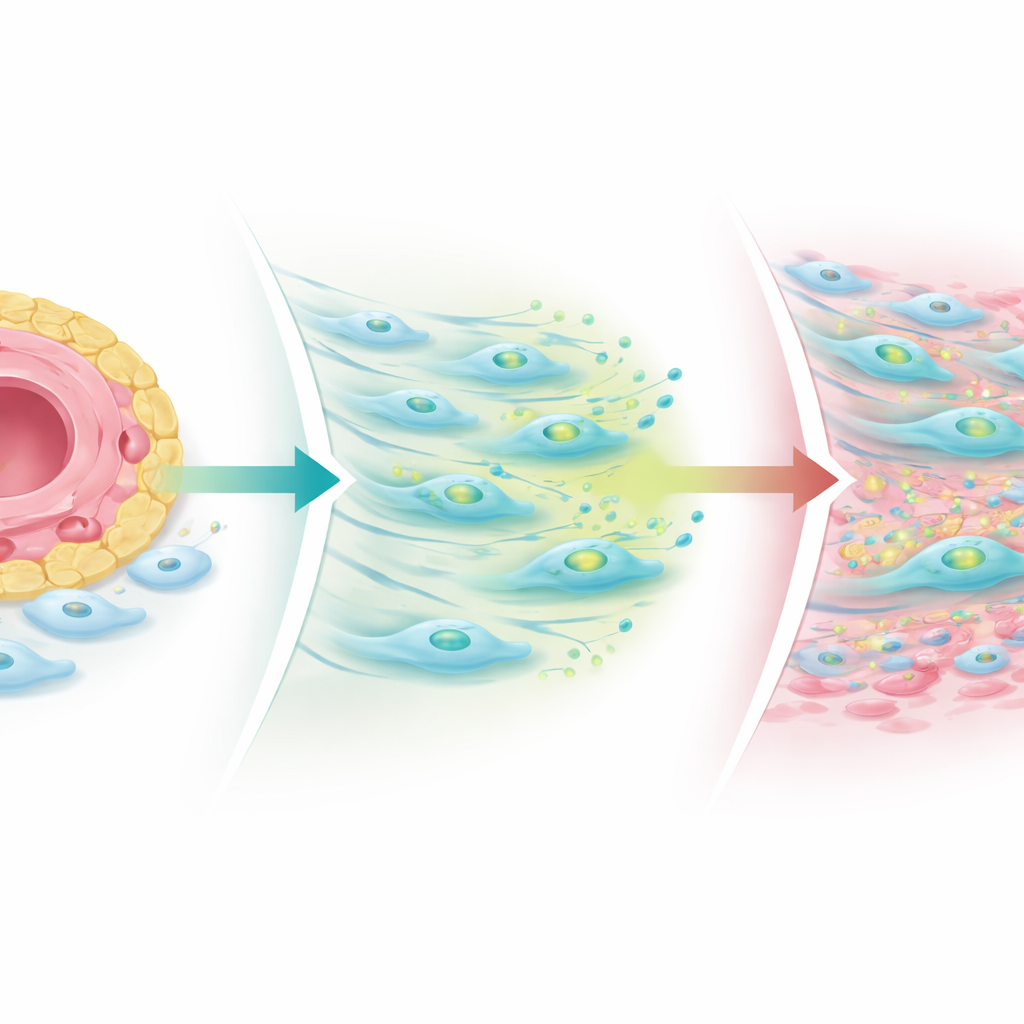
מה קורה כשהאיזון נשבר
החוקרים בנו מודלים מפרקיים מפושטים במשטחי מעבדה ואורגנואידים תלת־ממדיים המיוצרים מרקמת מטופלים כדי לבחון את המנגנון הזה. כאשר חיזקו את אותות נוטץ׳ מתאי האנדותל, הפיברובלסטים הגדילו את ייצור ה‑TGF‑בטא אך הורידו את רמות הקולטנים, מה שמגביל את היווצרות הצלקת. כאשר חסמו את נוטץ׳ או הפריעו לדפוס היציב שלו, הפיברובלסטים השיבו קולטני TGF‑בטא—ובייחוד קו‑קולטן שנקרא TGF‑בטא רצפטור III— ותאי פיברוזה חיוביים ל‑COMP התרחבו הרחק מכלי הדם. בביופסיות מטופלים שנלקחו לאחר הטיפול, אשכולות תאים חיסוניים הצטמצמו כמעט אצל כולם, אך נישות פיברוגניות, ובמיוחד אזורים עשירים ב‑COMP, לעתים קרובות גדלו, במיוחד אצל אלה שכאב המפרק שלהם נמשך. הדבר מרמז שתרופות אנטי‑דלקתיות סטנדרטיות יכולות לכבות את "האש" החיסונית בעוד שהן משאירות או אפילו חושפות תהליך ייצור צלקת ששומר על נוקשות וכאב במפרקים.
דרכים חדשות להרגיע מפרקים עקשניים
לבסוף, הצוות בחן האם שיבוש מעגל פיברוגני זה יכול להיות שימושי מבחינה טיפולית. באורגנואידים שמקורם בחולים, תרופות המעכבות את נוטץ׳ או חוסמות איתות TGF‑בטא הפחיתו את ייצור ה‑COMP, חלבונים קשורים לצלקת וקולגנים מרכזיים, ושינו מחדש פעילות גנטית באזורים פרו‑וסקולריים. לצופה הכללי, המסר הוא שלא כל נזק בדלקת פרקים שגרונית נובע מדלקת נראית: חלקו "תכנותי" בתוך תאי התמיכה של המפרק וכלי הדם. על ידי מיקוד בשיח נוטץ׳–TGF‑בטא שמווסת את אופן הנחת הרקמה הצלקתית על‑ידי הפיברובלסטים, טיפולים עתידיים עשויים למנוע או להפוך צורה פיברוטית עקשנית של המחלה העמידה לתרופות הממוקדות במערכת החיסון של היום.
ציטוט: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
מילות מפתח: דלקת פרקים שגרונית, פיברוזיס, פיברובלסטים, אותות TGF‑בטא, מסלול נוטץ׳