Clear Sky Science · he
אתר אלוסטרי יחיד מאחד הפעלה, וויסות ועיכוב ב-TRPM5
איך שומר־שער זעיר אחד מעצב טעם וחילוף חומרים
האוכל שאנו נהנים ממנו ואופן שבו גופנו מעבד סוכר תלויים בחלבונים מיקרוסקופיים שממלאים תפקיד של “שומר‑שער” בתאים שלנו. אחד מהשומרים האלה, תעלה הנקראת TRPM5, מסייעת בחישה של טעמי מתוק, מר ומסו-אומי ועוזרת ללבלב לשחרר אינסולין. המחקר הזה מגלה כיצד כיס קטן יחיד ב‑TRPM5 יכול לפעול ככפתור בקרה ראשי: להפעיל את התעלה, לכוונן את הרגישות שלה ואפילו לכבות אותה — תובנות שהן בעלות פוטנציאל להנחות טיפולים עתידיים בסוכרת, השמנה והפרעות מעיים.
תעלה בצומת שבין טעם וסוכר בדם
TRPM5 ממוקמת בממברנות של תאי טעם בלשון, בתאים המפרישים הורמונים במעיים ובתאים המפרישים אינסולין בלבלב. כשהרמות של סידן בתוך התאים עולות, TRPM5 נפתחת ומאפשרת לזרום יונים בעלי מטען חיובי, מה שמשנה לזמן קצר את המתח החשמלי של התא. בטעמי הטעם, האות החשמלי הזה מעביר למוח מידע שיש על הלשון חומר מתוק, מר או אוממי. בלבלב זה מסייע לכוונן פולסים של אינסולין אחרי ארוחה. בני אדם ובעלי חיים עם תפקוד TRPM5 לקוי מראים קשיים בהפרשת אינסולין ושליטה על רמות הסוכר בדם, מה שמרמז שתרופות המכוונות ל‑TRPM5 עשויות אי‑פעם לסייע בטיפול בהפרעות מטבוליות. עם זאת, עד לא מזמן החוקרים לא החזיקו בכלים מדויקים להדליק או לכבות את התעלה.
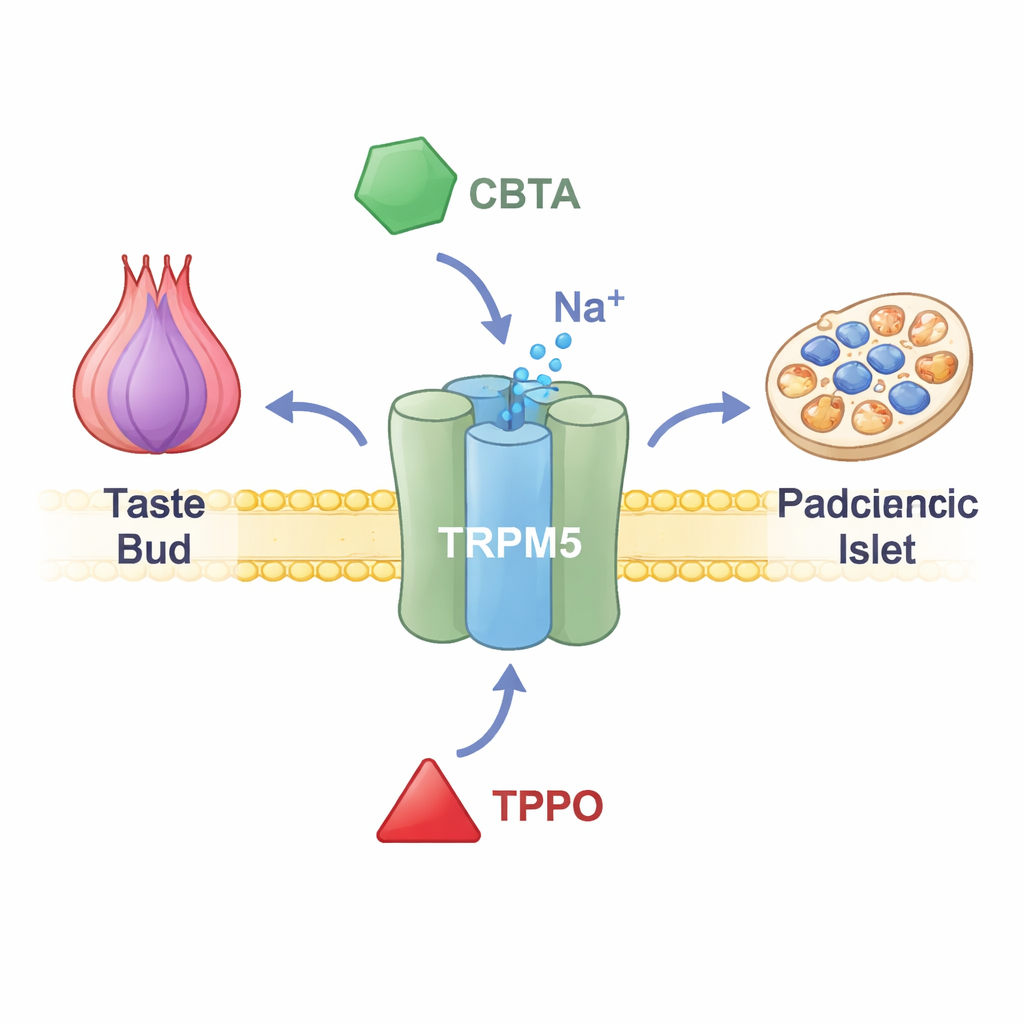
מפתח כימי חדש שמאיץ את התעלה
החוקרים התרכזו בעצם סינתטי הנקרא CBTA, שהיה ידוע קודם לכן כממריץ של TRPM5 אך לא הובן לעומק. באמצעות הקלטות חשמליות בתאים מהונדסים שמייצרים TRPM5 הם הראו כי CBTA מסוגל לפתוח את התעלה גם כשרמות הסידן כמעט חסרות, מה שמוכיח שהוא פועל כמפעיל אמיתי ולא רק כחומר המגביר את השפעת הסידן. כשיש כמויות זעירות של סידן — רמות שבדרך כלל משאירות את TRPM5 שקטה — CBTA וסידן פועלים ביחד ויוצרים זרמים גדולים בהרבה מאשר כל אחד מהם לבדו. משמעות הדבר היא ש‑CBTA עושה את TRPM5 רגיש במיוחד, כך שרמות סידן בקרבת מנוחה פתאום מספיקות כדי להפוך את התעלה לפתוחה לרווחה.
כיס בקרה נסתר שנחשף ב‑Cryo‑EM
כדי לראות כיצד זה פועל ברזולוציה אטומית, הצוות השתמש במיקרוסקופיה אלקטרונית קפואה (cryo‑EM) כדי ללכוד תמונות תלת‑ממדיות של TRPM5 בתנאים שונים. הם גילו כי CBTA מקובץ לתוך חלל שלא תואר קודם בחלק העליון של אזור חישה וולטאג’ בתעלה, ממש מעל לאזור שבו הסידן בדרך כלל נקשר. חלל זה, שנוצר על ידי אשכול חומצות אמינו, משמש כאתר עגינה מדויק. כאשר המדענים שינו חומצות אמינו מרכזיות שמרפדות את הכיס, CBTA כבר לא היה מסוגל להפעיל את TRPM5, אף על פי שסידן עדיין עבד — מה שמאשר שהנישה הקטנה הזאת חיונית לפעולת התרופה. באופן בולט, קשירת CBTA משנה בעדינות חלקים סמוכים של החלבון באופן שמקל על הסידן לתפוס את מקומו הרגיל, ובכך מסבירה את הסינרגיה הדרמטית שנמדדה בהקלטות החשמליות.
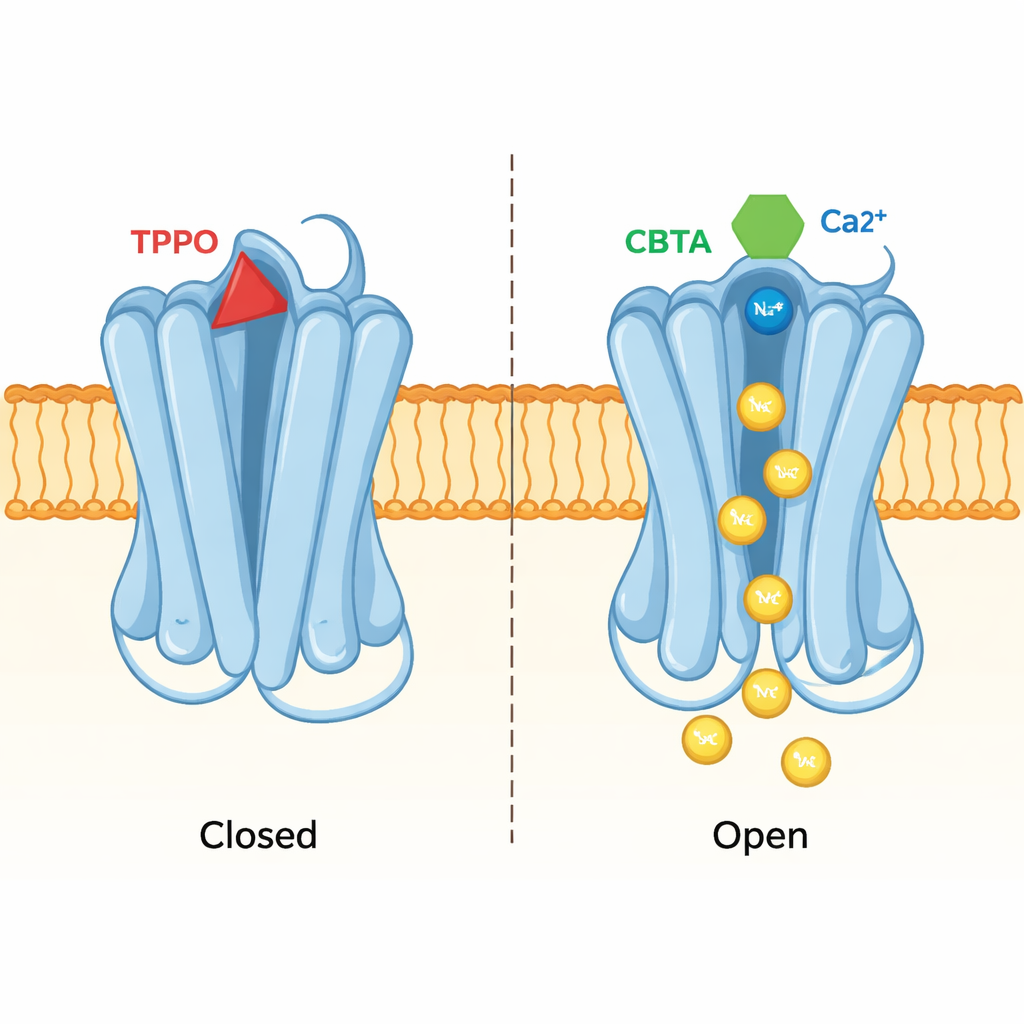
כיס אחד, שתי תוצאות מנוגדות
גישה מבנית דומה גילתה כיצד מעכב בשם TPPO משתמש באותו כיס בדיוק כדי לייצר את ההשפעה ההפוכה. כאשר TPPO נקשר, שני אתרי הסידן ב‑TRPM5 נשארים מאוכלסים, אך הפור המרכזי של התעלה נשאר לחוץ ולא מעביר יונים. השוואה בין המבנים הקשורים ל‑TPPO ול‑CBTA הראתה שהצורות השונות שלהם דוחפות מקטעי חלבון סמוכים בכיוונים מנוגדים. CBTA מעודד תנועות שמתפשטות אל הפור ופותחות אותו; TPPO, במקום זאת, מופרע את ההתקשרות בין הכיס לפור ושומר על השער סגור. במהותו, הכיס הזה יכול לפעול כמאיץ או כבלם, בהתאם למולקולה שממלאת אותו.
שינוי כבלי התקשורת הפנימיים של התעלה
המחקר גם מראה שהכיס הזה יכול לקחת על עצמו תפקידים שבדרך כלל מטופלים על‑ידי אתר קשירת סידן נפרד בתוך התא. בתעלות מוטנטיות שבהן אתר הסידן הפנימי הרגיל מנוטרל, סידן לבדו לא הצליח לפתוח את TRPM5. עם זאת, CBTA עדיין הפעלה את המוטנטים האלה ושינתה אלמנט מבני מרכזי הקושר בין החלקים הפנימיים והחיצוניים של התעלה. במוטנטים אחרים שמפרקים את הקשר בין קשירת הסידן לפתיחת הפור, הוספת CBTA השיבה את ההתנהגות לנורמה. תוצאות אלה מראות שהאתר החדש שזוהה יכול להפנות או לתקן תקשורת בין דומיינים שונים בתעלה, ופועל כמרכז גמיש לאיתות בטווח ארוך בתוך החלבון.
מדוע זה חשוב לתרופות עתידיות
ללא מומחיות מיוחדת, המסר המרכזי הוא שהחוקרים מצאו כיס יחיד רגיש לתרופות ב‑TRPM5, שיכול לשלב בין הפעלה, כוונון וכיבוי. פעיל קטן כמו CBTA יכול לחקות סידן ולהגביר מאוד את רגישות התעלה, בעוד שמולקולה אחרת, TPPO, יכולה לנעול את אותה תעלה בסגירה — כל זאת על‑ידי עגינה באותו מקום. תמונה מאוחדת זו של אופן השליטה ב‑TRPM5 פותחת פתח לעיצוב מולקולות מותאמות שיגדילו או ירגיעו את פעילותה ברקמות ספציפיות, עם יישומים פוטנציאליים שמטווחים משיפור טיפולים מבוססי טעם ותרופות לתנועת מעיים ועד פיתוח אסטרטגיות חדשות לניהול רמות סוכר ומחלות מטבוליות.
ציטוט: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
מילות מפתח: תעלת TRPM5, תפיסת טעם, הפרשת אינסולין, פתיחת וסגירת תעלות יוניות, וויסות אלוסטרי