Clear Sky Science · he
עיכוב CDK4/6 מקטין את ההתרחבות בעקבות כימותרפיה של המטופל עם מוטציות ב‑TP53
מדוע חשוב להגן על הדם בזמן טיפול בסרטן
כימותרפיה נגד סרטן יכולה להציל חיים, אך היא גם פוגעת בעצם המח שבה מיוצרים תאי דם חדשים. אצל חלק מהאנשים הנזק הזה מעודד במקרה תאי גזע של דם נדירים שיש להם מוטציות קיימות להתפשט ולשלוט, דבר שעשוי להוביל מאוחר יותר לסוגי סרטן דם אגרסיביים. המחקר בוחן שאלה תקווה: האם אפשר להשתמש בתרופה חולפת ככפתור "השהייה" על תאי גזע של דם כדי להגן עליהם בזמן כימותרפיה, ולהאט את עלייתם של הקלונים המוטנטים המסוכנים מבלי להחליש את הטיפול בגידול עצמו?
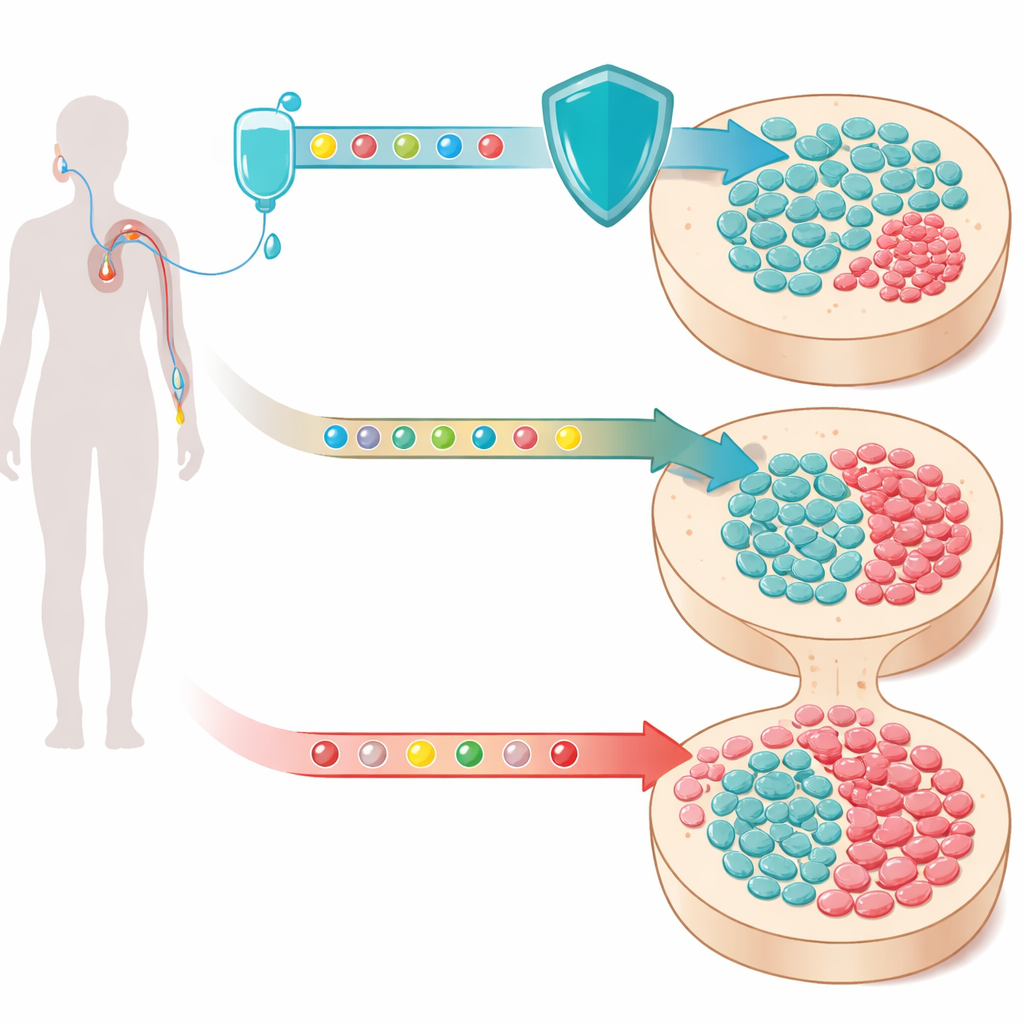
קלונים נסתרים בדם
ככל שאנו מתבגרים, תאי הגזע המייצרים דם צוברים בהדרגה שינויים ב‑DNA. רוב התאים המתקלקלים נשארים בלתי מזיקים, אך מעטים מהם זוכים ליתרון גידולי ומתחילים ליצור קלונים קטנים—כיסים של תאים בעלי התאמה גנטית—הנמצאים במחזור הדם. תופעה זו, שנקראת המטופויאזה קלונלית, נפוצה למדי במבוגרים. כאשר הגן הפגוע הוא TP53 או גנים אחרים המעורבים בתגובה לנזק ב‑DNA, הקלונים הללו מדאיגים במיוחד: הם שורדים מצבי לחץ שפוגעים בתאים נורמליים ומקושרים באופן הדוק לנאופלזיות מילואידיות הקשורות לטיפול, קבוצה של סרטןי דם שלעיתים קרובות קטלניים שעשויים להופיע שנים אחרי כימותרפיה.
להשהות את תאי הגזע במהלך כימותרפיה
החוקרים התמקדו בתרופות החוסמות CDK4/6, מנועי מפתח שדוחפים תאים להתחלק. אחת התרופות הללו, טרילאציקליב, מאושרת כבר להקטין ספירות דם נמוכות אצל אנשים המקבלים טיפולים מסוימים בסרטן ריאה. מתן קצר לפני כימותרפיה דוחף את תאי הגזע והפרוגניטורים במח העצם למצב מנוחה. הצוות הניח שאם גם התאים הבריאים וגם התאים המוטנטים ב‑TP53 יהיו פחות פעילים כשהכימותרפיה תגיע, המוטנטים יאבדו חלק ניכר מיתרון ההישרדות הרגיל שלהם, מפני שפחות תאים—נורמליים או מוטנטים—יהיו ברגע חלוקה כשתרופות שמשבשות DNA יהיו בשיא הרעילות שלהן.
עדויות ממחקרים קליניים ומודלים חייתיים
כדי לבחון את הרעיון אצל מטופלים אמיתיים, הקבוצה ניתחה דגימות דם מארבעה ניסויים קליניים אקראיים על מטופלים שקיבלו כימותרפיה לסרטן ריאה מסוג תאים קטנים, סרטן קולון גרורתי וסרטן שד משולש שלילי. בכל ניסוי, המטופלים חולקו אקראית לקבל טיפול כימותרפי סטנדרטי יחד עם טרילאציקליב או פלצבו. בעזרת רצף DNA עמוק במיוחד של תאי דם בתחילת הטיפול ולאחר מספר מחזורים, המדענים עקבו איך קלונים מוטנטים ידועים השתנו בגודלם לאורך זמן. בכל הניסויים, קלונים הנושאים מוטציות בתגובת נזק ל‑DNA—בפרט TP53 ו‑PPM1D—התרחבו במהלך הכימותרפיה, אך הם גדלו באופן משמעותי יותר לאט באנשים שקיבלו טרילאציקליב. בממוצע, קצב הגדילה של הקלונים המסוכנים הללו קטן בכ‑שליש בערך, בעוד שמוטציות שגרתיות הקשורות לגיל בגנים אחרים הושפעו במידה מועטה.
התבוננות מעמיקה במנגנון ההגנה
מכיוון שהמעקב אחר המטופלים עדיין קצר יחסי, הצוות פנה למודלים בעכברים כדי לחשוף איך חסימת CDK4/6 מעצבת את מח העצם במהלך הטיפול. הם יצרו עכברים שמערכת הדם שלהם הכילה חלק קטן של תאי גזע מוטנטים ב‑Trp53, המדמה המטופויאזה קלונלית אנושית. כשהעכברים קיבלו כימותרפיה מבוססת פלטינה לבדה, התאים המוטנטים עקפו במהירות את השכנים הבריאים הן בדם והן במח. אך כאשר נתנו טרילאציקליב—או מעכב CDK4/6 אחר, פלבציקליב—קצר לפני כל מנה של כימותרפיה, השתלטות המוטנטים נחסמה כמעט לחלוטין. רצף RNA בתא בודד הראה כי עיכוב CDK4/6 דחף תאי גזע ופרוגניטורים למצב יותר שקט ופחות מפצלתי, הפחית תוכנית גנים של "עמידות גזע" שמטיבה עם תאים מוטנטים ארוכי־חיים, הסיט את ההתפתחות הרחק מקוונות מיילואידיות וכיוון אותה לקוונות לימפואידיות, והפעיל באופן סלקטיבי מסלולי מוות תאי בתאי גזע מוטנטים ב‑Trp53 תוך שמירה על התאים הנורמליים.
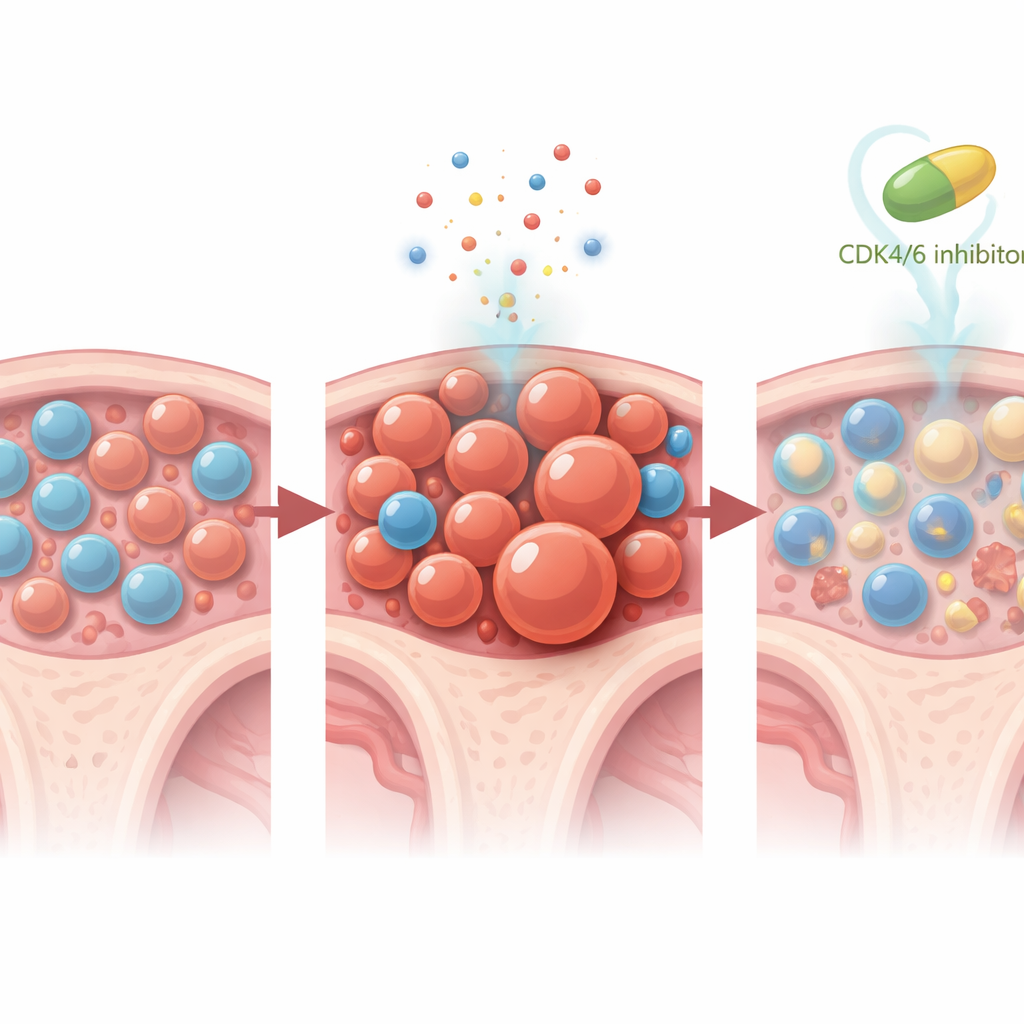
השפעה מתמשכת וכיוונים עתידיים
ניסוי בולט בעכברים הצביע על כך שגם קורס קצר של עיכוב CDK4/6 יכול להשאיר אפקטים מתמשכים: שתי שבועות של טרילאציקליב שניתנו סביב תקופת הכימותרפיה מנעו את התרחבות קלוני‑Trp53 למשך לפחות שישה שבועות אחרי שסיום כל הטיפול. חשוב לציין שספירויות הדם ובריאות כללית של המח נותרו מקובלות, מה שמעיד שהאסטרטגיה ההגנתית לא הייתה פשוטו כמשמעו ויתור על סוג אחד של רעילות בתמורה לאחר. אף על פי שאף אחד מהמטופלים בניסויים לא פיתח סרטן דם במהלך המעקב המוגבל, נוכחותם והגדילה המאטה של קלונים זעירים מאוד עם מוטציות ב‑TP53 תומכות ברעיון שזו צעד מוקדם שניתן לשנותו בדרך להיווצרות לוקמיה הקשורה לטיפול.
מה המשמעות עבור חולי סרטן
עבור מטופלים שכבר נושאים קלונים מסוכנים של תאי דם, החשש היה שהקבלת הכימותרפיה הדרושה לשליטה בגידול המוצק עשויה גם לשתול את הזרעים ללוקמיה עתידית שלעיתים קרובות אינה ניתנת לטיפול. עבודה זו מציעה הוכחת רעיון כי מעכבים של CDK4/6 המנוהלים בתזמון מדוד יכולים להחליש את יתרון הגידול של הקלונים המסוכנים הללו על‑ידי מקלט קצר של מח העצם בזמן הכימותרפיה. למרות שיש צורך בניסויים קליניים ארוכים וגדולים יותר כדי להוכיח שגישה זו אכן מקטינה את התחלואה בלוקמיות הקשורות טיפול, היא מצביעה על עתיד שבו ניתן לטפל בגידול הראשוני בעוצמה ובו‑זמנית להגן על המערכת המייצרת דם מפגיעה גנטית ארוכת טווח.
ציטוט: Chan, I.C.C., Zhang, P., Pan, X. et al. CDK4/6 inhibition mitigates chemotherapy-induced expansion of TP53-mutant clonal hematopoiesis. Nat Genet 58, 582–592 (2026). https://doi.org/10.1038/s41588-026-02526-w
מילות מפתח: המטופויאזה קלונלית, מוטציות TP53, תופעות לוואי של כימותרפיה, מעכבי CDK4/6, לוקמיה הקשורה לטיפול