Clear Sky Science · he
RNA גליקו במורכבות עם הסולפט של ההפארן מווסתת איתות VEGF-A
איך תאים מכוונים בדיוק את אותות כלי הדם של הגוף
כלי דם אינם צומחים פשוט בכל מקום שבו מופיעים אותות גדילה — הם חייבים להיות מבוקרים בדיוק כדי להזין רקמות מבלי להזין גידולים או לגרום לעיוורון. המאמר הזה חושף "בלם" בלתי צפוי על אות מרכזי המניע צמיחת כלי דם בשם VEGF‑A. המחברים מראים כי קטעי RNA קטנים, המקושטים על פני התא בשותפות עם סוכרים וחלבונים, יכולים להחליש את המסר של VEGF‑A, ומשנים את האופן שבו אנו חושבים על השפה שהתאים משתמשים בה על פני השטח שלהם.
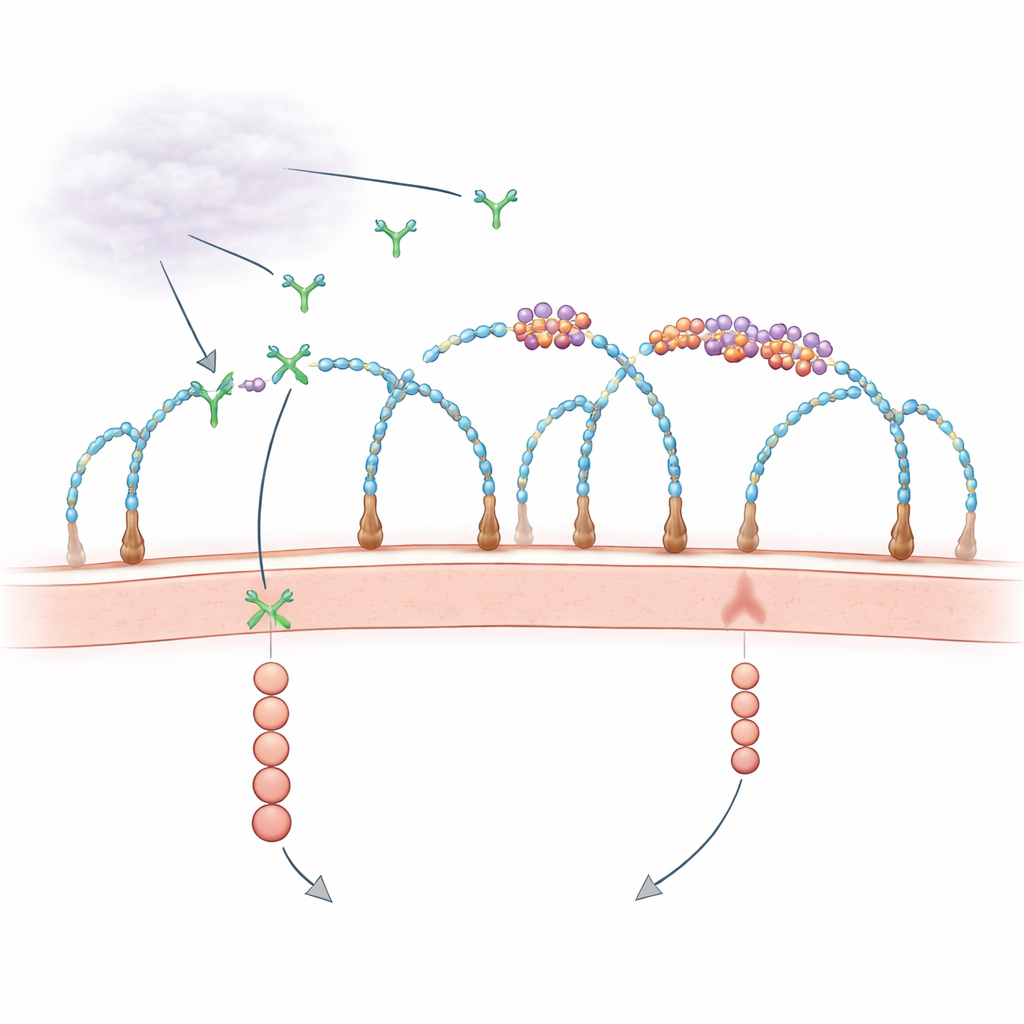
תפקיד מפתיע ל‑RNA על פני התא
עשרות שנים ביולוגים ידעו כי מעטפת התא החיצונית, עשירה בחלבונים מקושטים בסוכרים הנקראים פרוטאוגליקנים של הפארן‑סולפט, מסייעת ללכוד גורמי גדילה ולהציגם לקולטנים. במקביל, תצפיות מפוזרות רמזו כי קטעי RNA מחוץ לתאים עשויים להשפיע על צמיחת כלי דם, אך השחקנים והמנגנונים היו לא ברורים. עבודות אחרונות גילו כי חלק מ‑RNA הקטנים מקושרים כימית לסוכרים מורכבים כדי ליצור "גליקוRNA", וכי חלבוני קשר‑RNA מסוימים מופיעים גם הם על פני התא, מתאגדים יחד עם RNA אלה. המחקר החדש שואל שאלה ממוקדת: האם האיים הקטנים האלה של RNA–חלבון בממברנה אכן שולטים באופן שבו אותות גדילה כמו VEGF‑A מתקבלים?
בניית איים מקובצים של RNA–חלבון בעזרת שרשרות סוכר
באמצעות מסכים של קריספר‑נוקאאוט ברמת הגנום ומיקרוסקופיה ברזולוציה גבוהה, החוקרים גילו כי שרשראות סוכר ספציפיות — הפארן‑סולפט עם דפוסי סולפורילציה מסוימים — הן סקפולדות חיוניות להרכבת צברים אלה של RNA‑חלבון, אותם הם מכנים ריבונוקלאופרוטאינים על פני התא (csRNPs). כאשר הורדו אנזימים מרכזיים שבונים או מסולפים את ההפארן‑סולפט, הצברים של גליקוRNA ושותפיהם החלבוניים נעלמו מפני התא, אף על פי שה‑RNA והחלבונים עדיין היו נוכחים בתוך התאים. אנזימים הקוצצים את שרשראות ההפארן‑סולפט מהמשטח או חוסמי סולפורילציה כימיים הביאו לאותו אפקט. ממצאים אלה מראים כי שרשראות הפארן‑סולפט שלמות ומסולפות כראוי מארגנות את ה‑csRNPs לאיים ננו‑קלים בממברנה.
צברים של RNA פועלים כבלמים על אות חזק לצמיחת כלי דם
הצוות פנה אז לתאי אנדותל אנושיים, המחפים כלי דם ומגיבים ל‑VEGF‑A. הם גילו שגם תאים אלה מציגים צברים של csRNP מעוגנים להפארן‑סולפט. טיפול בתאים חיים ב‑RNases, אנזימים המפרקים RNA, הסיר את מרכיב ה‑RNA מבלי להפריע לשרשראות הסוכר הבסיסיות. בתנאים אלה, הצורה הנפוצה ביותר של VEGF‑A הקושרת הפארן (VEGF‑A165) גרמה להפעלה חזקה הרבה יותר של מסלול איתות ERK במורד הזרם, בעוד צורה קצרה יותר החסרה את זנב הקישור להפארן (VEGF‑A121) לא הושפעה. יותר מולקולות VEGF‑A165 התקשרו לפני התא לאחר הסרת ה‑RNA, אך רמות הקולטן נשארו זהות. במכשירים מיקרופלואידיים תלת‑ממדיים, תאי אנדותל שטופלו ב‑RNase גדלו לעומק ג'לים של קולגן בצורה מרובה והיוו מבנים דמויי‑צינור בצורה עזה יותר, מה שמציין כי השמדת RNA משטחי משחררת התנהגות פרו‑אנגיוגנית.
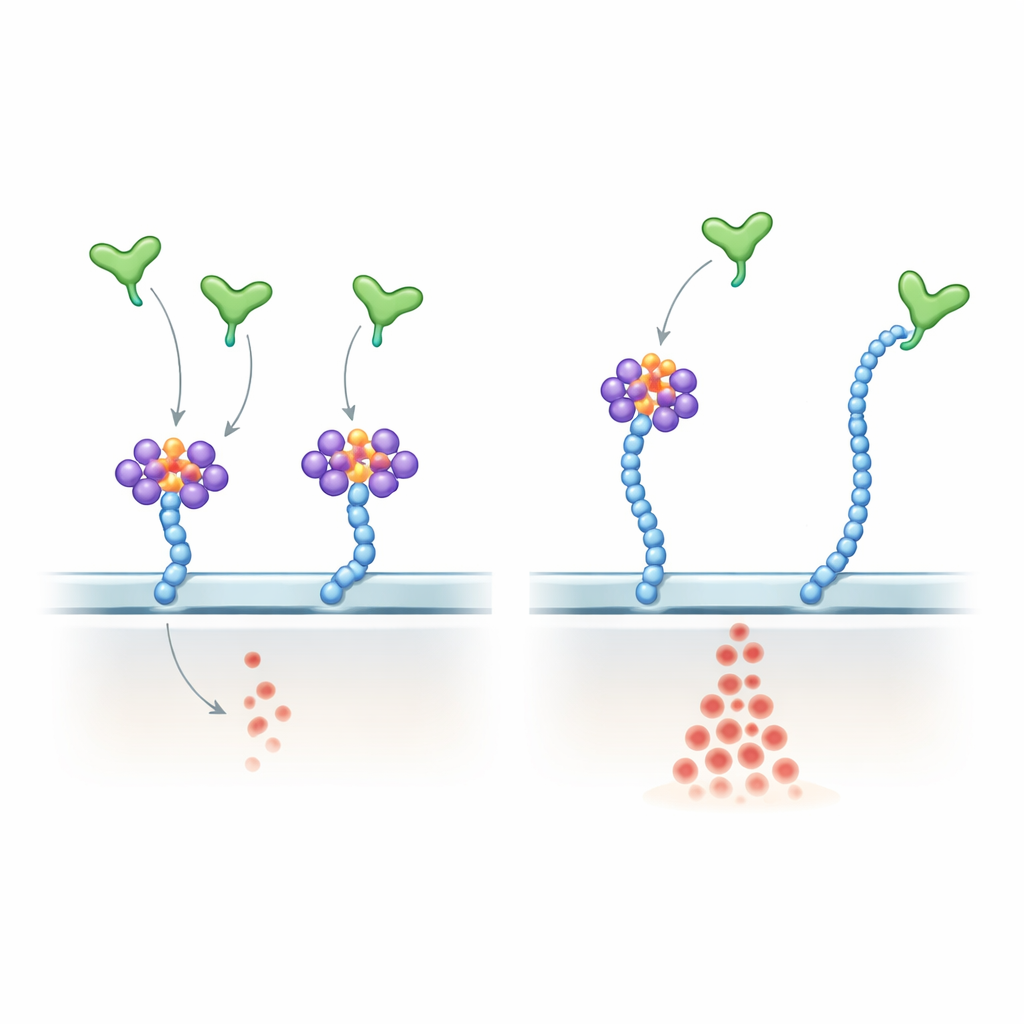
פירוק האופן שבו VEGF‑A מבחין בין RNA לסוכר
כדי לבדוק את המנגנון, המחברים הראו כי VEGF‑A165 נקשר ישירות ל־RNAים קטנים נבחרים, כולל רבים מגליקוRNA הידועים, דרך האזור האלקטרו‑חיובי בקצה ה‑C שלו — אותו אזור שקושר גם הפארן‑סולפט. הם הנדסו גרסה עדינה של VEGF‑A165 שבה שיירי ארגינין מרכזיים בזנב זה הוחלפו בליזינים. מוטנט זה שמר על המטען החיובי הכולל שלו ועדיין קיבל בידו שרשראות הפארן‑סולפט, אך הוא קושר גליקוRNA בצורה חלשה והפך לשאינו רגיש ברובו לטיפול ב‑RNase. בתאי אנדותל, המוטנט יצר הפעלה חזקה ועמידה יותר של ERK מאשר VEGF‑A165 הרגיל, המדמה באופן הדוק את אפקט הסרת ה‑RNA מפני התא. בעכברים חיים, הזרקת המוטנט לעין גרמה לצמיחת כלי דם רטינלית רבה יותר מאשר החלבון הרגיל. בעוברים של דג הזברה, ביטוי יתר של הגרסה המוטנטית של Vegfa הפריע לתבנית כלי הדם הנורמלית והגדיל את מספר תאי האנדותל.
ממנגנון בסיסי למשמעויות רחבות יותר
לבסוף, המחברים הראו כי חיבור זנב הקישור להפארן של VEGF‑A לחלבון איתות לא קשור, Wnt3a, יכול להסיט את פעילות ה‑Wnt: חיבור הזנב הרגיל הקטין שינויים התפתחותיים מונעי‑Wnt, בעוד חיבור הזנב העמיד‑RNA הגביר אותם. יחד, ניסויים אלה תומכים במודל שבו צברי csRNP, המעוגנים על ידי הפארן‑סולפט מסולף בצורה ספציפית, קושרים את VEGF‑A וגורמים קרובים כדי לרכך את פעילותם. כאשר מרכיב ה‑RNA מוסר או כאשר גורמי הגדילה מאבדים את יכולתם לחוש RNA, האיזון נוטה לעבר איתות חזק יותר ופיתוח צינורות כלי דם משתנה במגוון מינים.
מדוע זה חשוב עבור בריאות ותרופות עתידיות
ללא‑מומחה, המסר המרכזי הוא שתאים משתמשים לא רק בחלבונים ובסוכרים, אלא גם ב‑RNAים קטנים המוצגים על פני השטח כדי למתן אותות גדילה רבי‑עוצמה כמו VEGF‑A. צברים אלה של RNA–חלבון העוגנים בסוכרים פועלים כבלמים מתכווננים על יצירת כלי דם, ועוזרים להבטיח שכלי דם חדשים יצמחו איפה ומתי שצריך. הפרת האיזון הזה — על‑ידי פירוק RNA משטחי התא או שינוי תכונות קשירת‑RNA של גורמי גדילה — יכולה להעצים או לסטות את צמיחת הכלי־דם. הבנת שכבת הבקרה שנחשפה זו עשויה לפתוח דלתות לטיפולים המכוונים לכוונון מדויק יותר של אנגיוגנזה בהקשר של סרטן, מחלות עיניים, ריפוי פצעים ורפואה רגנרטיבית על‑ידי פגיעה ב‑RNA משטחי התא, בסקפולדות הסוכר שלהן או באזורים החושיים‑RNA של גורמי הגדילה.
ציטוט: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
מילות מפתח: אנגיוגנזה, גורם גדילה של תאים אנדותליאליים כלי דם, הפארן סולפט, RNA על פני התא, גליקוRNA