Clear Sky Science · he
מגן מטבולי התלוי בפוליאמינים מווסת ספלייסינג אלטרנטיבי
כיצד מולקולות זעירות עוזרות לתאים לקרוא את הגנים שלהם
בתוך כל תא, אותו תסריט DNA יכול להיקרא בדרכים רבות, מה שמאפשר למספר מוגבל של גנים לייצר מגוון עצום של חלבונים. גמישות זו תלויה בתהליך שנקרא ספלייסינג אלטרנטיבי, שמערך את הודעות ה‑RNA לפני שהן מומרות לחלבונים. מאמר זה מגלה שמולקולות קטנות בעלות מטען חיובי הנקראות פוליאמינים מובילות בצורה שקטה את שלב העריכה הזה, ופועלות כסוג של מגן שמסייע לתאים להחליט אילו גרסאות RNA לייצר. מאחר שהספלייסינג האלטרנטיבי קריטי בסרטן, בתפקוד המוח ובתאי גזע, גילוי השכבה הנסתרת הזו של בקרה נושא השלכות רחבות על בריאות ומחלה.
עוזרים קטנים טעוני מטען בכל תא
פוליאמינים הם מולקולות זעירות וגמישות הנושאות מספר מטענים חיוביים. תאים מייצרים אותן מתוך רכיבי מזון בסיסיים, וכבר זמן רב הם ידועים כסייעים לצמיחה ולשרידות, במיוחד בתאים מתחלקים במהירות כמו גידולים. המחברים שאלו האם פוליאמינים משמשים גם כאותות, ולא רק כדלק. על ידי חסימה חלקית של ייצור פוליאמינים בתאי סרטן ערמונית ובבני עכבר, הם מדדו כיצד חלבונים ו‑RNA משתנים לאורך זמן. הם מצאו שלפני שרמת הפוליאמינים הכוללת צונחת בחדות, מתרחשת גל חזק של שינויים בפוספורילציה של חלבונים—תגים כימיים שמדליקים או מכבים מתגים חלבוניים—ובמיוחד ברכיבים של מכונת עריכת ה‑RNA התאית, הספלייסוזום.
חיבור מחדש של עורך ה‑RNA התאי
בהתמקדות ב‑RNA, הקבוצה השתמשה בריצוף מעמיק כדי לעקוב אחרי ספלייסינג אלטרנטיבי כאשר סינתזת הפוליאמינים הועמדה. מאות מקטעי RNA אותרו כמעוקפים או כלולים בצורה שונה, בתאי סרטן, בסוגי תאים נורמליים וברקמות עכבר. שינויים אלה לא היו פשוט תוצאה משנית של האטת חלוקת התאים או של תהליך אחר התלוי בפוליאמינים שנקרא היפוסינציה. במקום זאת, כאשר החוקרים סיפקו לתאים פוליאמינים חיצוניים, רבות מההיסטות בספלייסינג חזרו לעבר הנורמליות. גם תרופות וגם כלי גנטיים שהורידו פוליאמינים יצרו דפוסי ספלייסינג דומים, והורדה נוספת של פוליאמינים באמצעות שילוב תרופות הגבירה את השינויים, מה שאישר שהאפקט מקושר בקשר הדוק לזמינות פוליאמינים.
מטרה נסתרת: מודול ה‑SF3 בספלייסינג
כדי לזהות היכן במנגנון הספלייסינג פועלים הפוליאמינים, המחברים השוו את חתימת הספלייסינג שנגרמה מהפחתת פוליאמינים עם מפה רחבה שנוצרה על ידי דממת יותר מ‑300 גורמי ספלייסינג ידועים באופן פרטני. ההתאמה הקרובה ביותר הצביעה על חלק ספציפי בספלייסוזום הקרוי תת‑המורכב SF3, שעוזר לזהות אותות מרכזיים ב‑RNA. ניתוח חישובי של נתוני קשירת חלבון–RNA ציבוריים תמך בקשר זה: RNAים שספייסינג שלהם הופר על ידי אובדן פוליאמינים היו בעלי סבירות גבוהה יותר להיקשר לחלבוני SF3. כאשר הצוות שיתק חלקית רכיבים של SF3 באופן גנטי או באמצעות תרופה, השפעות הספלייסינג של דלדול הפוליאמינים נמחקו ברובן, מה שמראה שפעילות SF3 שלמה נדרשת לנתיב הבקרה החדש הזה. 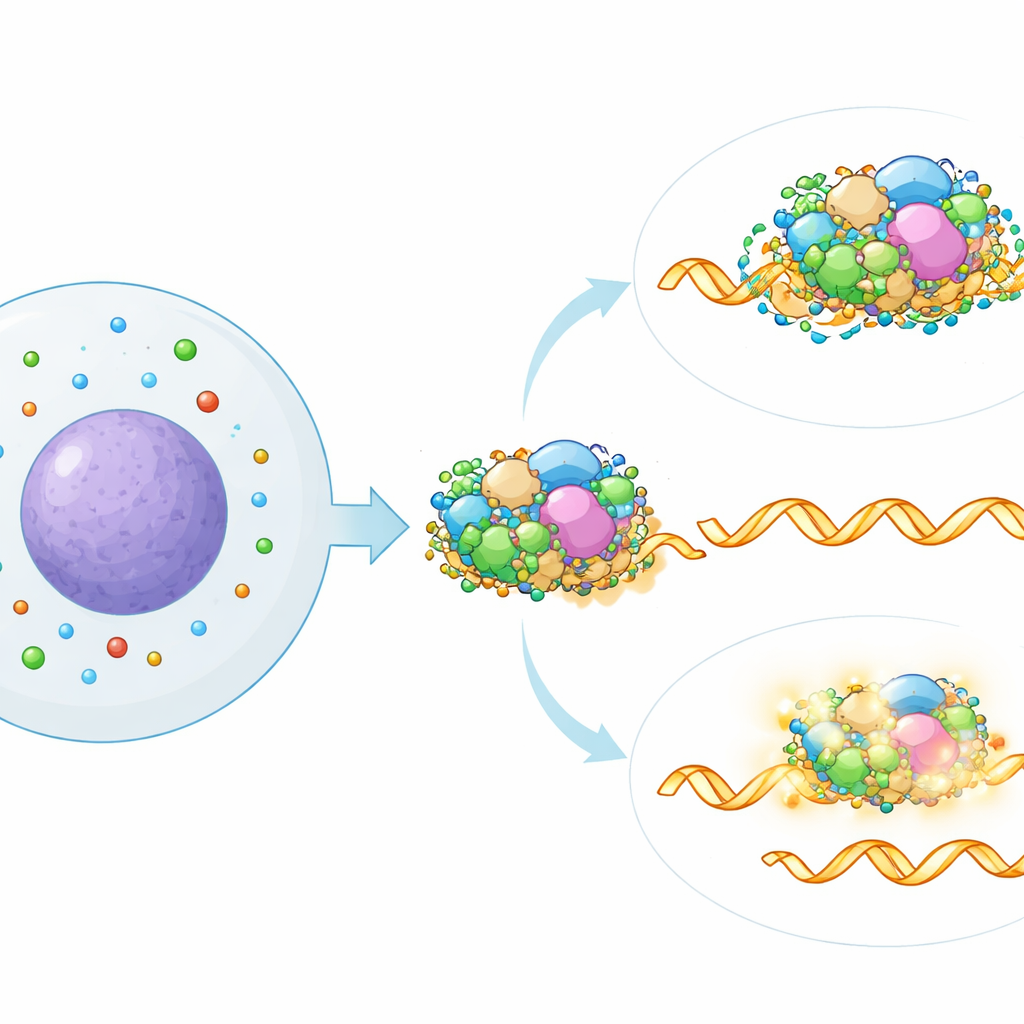
מיגון מטבולי: כיצד פוליאמינים חוסמים תיוג חלבונים
בהעמקה, החוקרים הבחינו שהאתרי הפוספורילציה שנפגעו בחוזקה ביותר על חלבוני SF3 נקבצו בתוך רצפים קצרים העשירים בחומצות אמינו בעלות מטען שלילי. דגמי מולקולות וניסויים במגנוט גרעיני הראו שהפוליאמינים שולשים לתוך כיסים חומציים אלה, יוצרים מספר מגעים אלקטרוסטטיים ומכסים באופן חלקי שרשראות סרין סמוכות שבהן בדרך כלל מוספים קבוצות פוספט. ה"חיבוק" הפיזי הזה מקטין את הנגישות של אתרים אלה לקינאזות חלבון—האנזימים שמצמידים פוספטים. בניסויים מבחנה, הוספת פוליאמינים חסמה ישירות קינאז בשם CK1 מלפוספוריל חלבוני SF3. בתאים, עיכוב CK1 וקרובו CK2 הקטין את שינויים הספלייסינג שנגרמו מאובדן פוליאמינים, ובבעלי‑חיים מיוחדים שבהם חלבון SF3A3 הונדס כך שנעדרו שלושה אתרי פוספורילציה מרכזיים, הם הפכו לפחות רגישים לשינויים בספלייסינג התלויים בפוליאמינים. 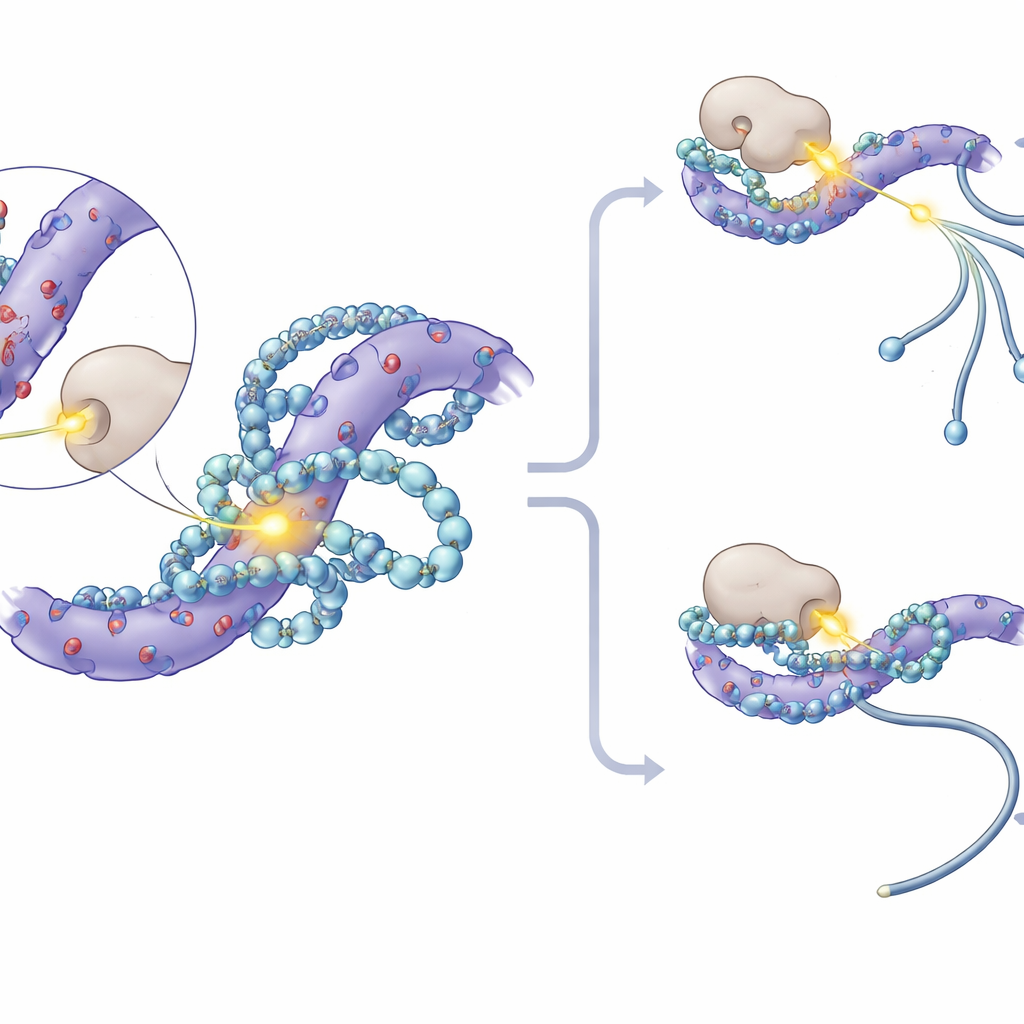
מולקולה מעוצבת שמפרידה בין התפקידים
המחקר גם מציג תרופה דמוית‑פוליאמין, BENSpm, שהיא טעונה חיובית בעוצמה רבה יותר אך בו‑זמנית מכבה את ייצור הפוליאמינים התאי. BENSpm נקשרה בחוזקה לכיסים החומציים של SF3 וחסמה את פעולת הקינאז, בדומה לפוליאמינים טבעיים, אך לא הצילה את גדילת התאים כאשר פוליאמינים אמיתיים היו נדירים. זאת אפשרה למחברים להבחין בין תפקידי הפוליאמינים הקלאסיים (תמיכה בצמיחה ובמטבוליזם) ובין תפקיד ה'הגנה' החדש שהוגדר כאן. בתאי גזע עובריים של עכבר, דלדול פוליאמינים דחף תאים לאבד את סימן ה"סטמנס" Nanog ושינה את מרקם הספלייסינג שלהם. BENSpm החזירה גם את פרופיל הספלייסינג וגם את הבעת Nanog חרף שימור העיכוב בסינתזת הפוליאמינים הרגילה, מה שמרמז שמיגון מטבולי הוא דרישה מרכזית לשמירת זהות תאי הגזע.
מדוע גילוי זה חשוב
במובנים יום‑יומיים, עבודה זו מראה שפוליאמינים פועלים ככפפות מגן זעירות סביב חלקים רגישים של חלבוני ספלייסינג מרכזיים. כשהכפפות על הידיים, קינאזות אינן יכולות לתפוס ולתיוג את האתרים בקלות, ועיבוד ה‑RNA של התא נשמר במסלולו. כאשר רמות הפוליאמינים נמוכות, הכפפות יורדות, הפוספורילציה מתפרצת ודפוסי הספלייסינג משתנים, עם השלכות על תאי סרטן ותאי גזע כאחד. על‑ידי הגדרת מנגנון ה"מיגון המטבולי" הזה ובהצעת מולקולת כלי שמדמה אותו באופן סלקטיבי, המחקר פותח פתח לדרכים חדשות לכוונן את קריאת הגן מבלי לשנות את ה‑DNA עצמו, ועשוי להשריץ טיפולים עתידיים הממוקדים בספלייסינג בסרטן וברפואה רגנרטיבית.
ציטוט: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
מילות מפתח: פוליאמינים, ספלייסינג אלטרנטיבי, עיבוד RNA, איתות מטבולי, ויסות תאי גזע