Clear Sky Science · he
מסלולי הפעלה ספציפיים לליגנד קובעים אותות GPCR בתאים
איך קולטן אחד יכול להתנהג כמו הרבה מתגים
רבים מהתרופות של היום פועלות על משפחה ענקית של חלבונים על פני התא הנקראים קולטי חלבון G-קשורים, או GPCR. קולטים אלה משפיעים על קצב לב, מצב רוח, נשימה ועוד פונקציות רבות בגוף. במשך עשורים ראו בהם מתגים פשוטים של דלוק/כבוי: תרופה נקשרת, המתג מתהפך, ואות נכנס לתא. המאמר הזה מראה שהמציאות עשירה בהרבה. באמצעות סוג חדש של "מרגל" פלואורסצנטי שנבנה ישירות בתוך הקולטן, המחברים צופים, בתאים חיים, כיצד תרופות שונות דוחפות את אותו קולטן לאורך מסלולי הפעלה נבדלים — כמו בחירה בנתיבים שונים בעיר — כדי לייצר דפוסי איתות שונים. הבנת המסלולים הנסתרים הללו עשויה לעזור בעיצוב תרופות שמעניקות את התועלת המבוקשת תוך הימנעות מתופעות לוואי.
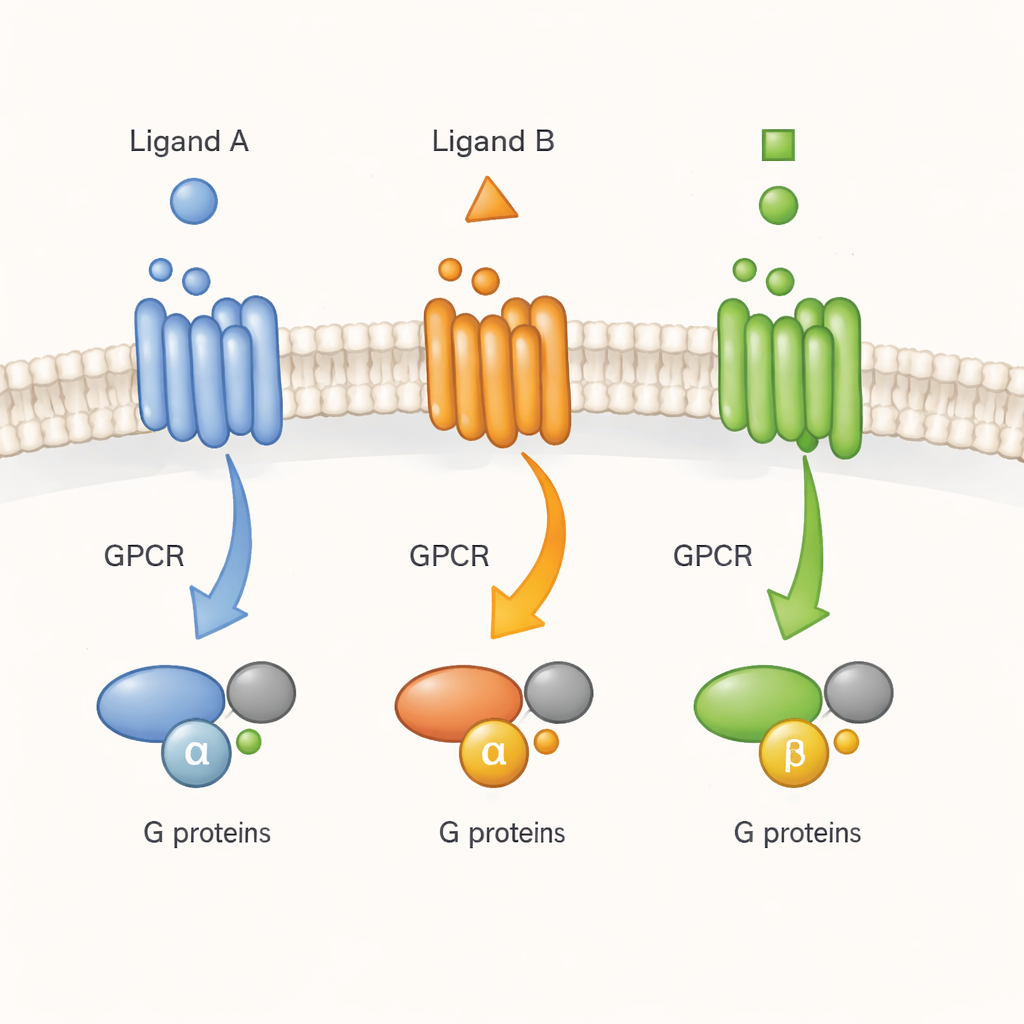
צפייה בפעמון הדלת של התא בזמן אמת
לעתים קרובות מתארים את ה-GPCRים כפעמוני דלת מולקולריים: מולקולה אות (ליגנד) מצלצלת מבחוץ, והקולטן מעביר את ההודעה לחלבוני G מבפנים. עבודות קודמות עם קולטים מזוקקים בתמיסות דטרגנט הציעו ש-GPCRים אינם פשוט עוברים מצורה לא פעילה אחת לצורה פעילה אחת. במקום זאת, הם מדגימים מגוון צורות שניתן לייצב במידה שונה על ידי תרופות. אולם לא היה ברור האם אותה מורכבות קיימת בסביבה הצפופה והדינמית של תא חי. כאן המחברים בוחנים קולטן מייצג, קולטן המוסריני M2 לאצטילכולין, רגולטור חשוב של פעילות הלב והעצב, ושואלים האם ליגנדים שונים דוחפים אותו לצורות פעילות מובחנות שחשובות לאיתות תאי אמיתי.
בניית דווחי אור זעירים על פני שטח הקולטן
כדי לעקוב אחרי תנועות הקולטן מבלי להפריע לתפקודו הרגיל, צוות החוקרים השתמש בהרחבת הקוד הגנטי, טכנולוגיה שמאפשרת להכניס חומצת אמינו מעוצבת במיקומים נבחרים על פני הקולטן החיצוניים. "עוגן" כימי זה ניתן ללחיצה (click) על צבע פלואורסצנטי קטן בתאים חיים. על ידי סריקה של 72 מיקומים ושמירת אלה שעדיין התנהגו כמו קולטים רגילים, הם בנו פאנל של שבע תבניות של קולטן M2, שכל אחת נושאת צבע יחיד במקום חיצוני-לולא שונה. כאשר הוחל המוליך הטבעי אצטילכולין, הבהירות של הצבע באתרי אלה עלתה או ירדה באופנים אופייניים, וחשפה כיצד כל חלק מפני שטח הקולטן זז כאשר האיתות החל. חשובה מכך, הקולטים המסומנים הללו עדיין יכלו להפעיל חלבוני G ולעבור קליטה פנימית נורמלית, מה שמראה שהדווחים היו נאמנים ולא מפריעים.
תרופות משאירות "טביעות אצבע קונפורמציונליות" מובחנות
החוקרים השוו לאחר מכן כמה תרופות שכולן מפעילות את קולטן M2 אך בעוצמות שונות: האצטילכולין של הגוף, אגוניסט סינתטי־על חזק בשם איפרוקסו, ושני אגוניסטים חלקיים חלשים יותר, ארקולין ופילוקרפין. כל תרופה ייצרה דפוס ייחודי של שינויים בפלואורסצנציה על פני שבעת אתרי הדווח — טביעת אצבע קונפורמציונלית. ברוב המיקומים, גודל התזוזה עקב בעוצמת ההפעלה של התרופה. בשני אתרים, לעומת זאת, הקשר היה הפוך: התרופות החלשות ייצרו את השינויים הגדולים ביותר, והתרופה החזקה כמעט ולא יצרה שינוי. התנהגות כזו אינה ניתנת להסבר על ידי מצב פעיל יחיד. במקום זאת היא מצביעה על כך שהקולטן עצמו, בתאים חיים, יכול לאמץ מספר צורות פעילות מובחנות, שחלקן מועדפות על ידי תרופות חזקות ואחרות על ידי חלשות.
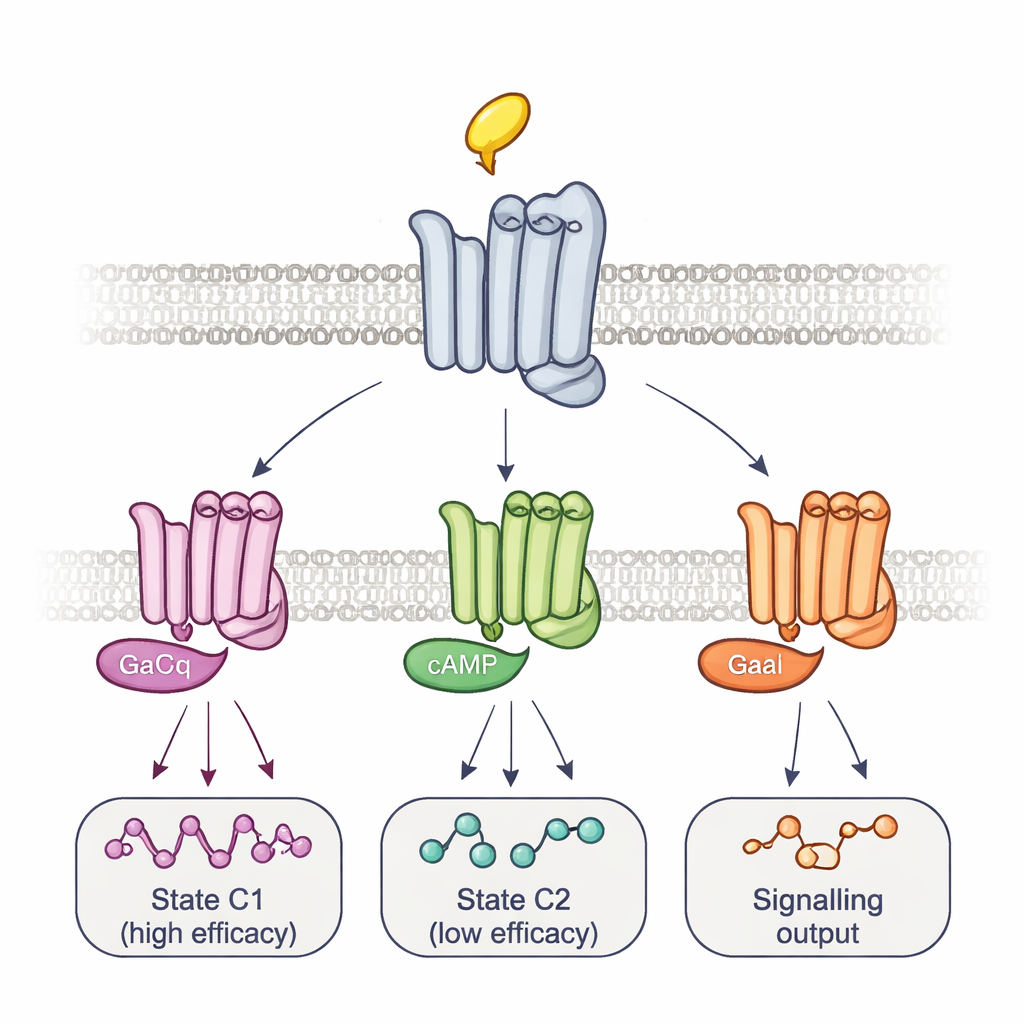
מורכבות של קומפלקסים ומסלולים מתוזמנים לאיתות
כדי לקשר צורות אלה לאיתות בפועל, הצוות שינה את חלבוני G עצמם. ביטוי יתר של חלבון G מוטנט היוצר קומפלקסים צפופים ובעלי חיים ארוכים עם קולטים מוחק באופן סלקטיבי את האות מכמה אתרי דווח תוך שהוא מחזק אחרים. דפוס זה, יחד עם תזמון השינויים בפלואורסצנציה, חשף לפחות שני קומפלקסי קולטן–חלבון G עיקריים: קומפלקס המתהווה במהירות ובעלי יעילות גבוהה, ואחד איטי יותר ובעל יעילות נמוכה. תרופות שונות הזיזו את המאזן בין הקומפלקסים הללו ואף השתמשו בצעדים ביניים שונים כדי להגיע לשם, ועקבו אחר מסלולי הפעלה ספציפיים לתרופה. באמצעות בדיקת ביולומיניסנציה נפרדת שמנטרת פאנל של 14 תת־סוגים של חלבוני G, המחברים הראו כי שיווי המשקל הללו מסייעים לקבוע לא רק עד כמה תרופה מפעילה איתות באופן כללי, אלא אילו חלבוני G בדיוק מופעלים. לדוגמה, ארקולין הפעיל באופן מועדף חלבוני Go מסוימים, בעוד שפילוקרפין העדיף בחוזקה את הקומפלקס בעל היעילות הנמוכה.
מדוע הדבר חשוב לתרופות טובות יותר
ללא מומחיות מיוחדת, המסר המרכזי הוא שקולטן יחיד אינו רק מתג אחד אלא אשכול של מתגים קשורים, כל אחד נגיש באמצעות מסלולים שונים וכל אחד מחובר לתוצאות מטה־זרם מעט שונות. המחקר הזה מספק תצפית ישירה על אותם מסלולים ומצבים בתאים שלמים, במקום במערכות מצומצמות בצינורות ניסוי. על ידי מיפוי כיצד תרופות מסוימות משיקות את הקולטן לעבר קומפלקסים ושותפי חלבון G מסוימים, החוקרים מקבלים תבנית לעיצוב תרופות "חכמות" — תרכובות שמניעות קולטנים למצבים שמייצרים אותות מועילים תוך הימנעות מאותות הקשורים לתופעות לוואי. אסטרטגיית החיישן הפלואורסצנטי שפיתחו כאן אמורה להיות ניתנת להתאמה לרבים מהקולטים האחרים, ופותחת חלון אל הכוריאוגרפיה בזמן אמת של פעולת תרופות בתאים חיים.
ציטוט: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
מילות מפתח: אותות GPCR, יעילות ליגנד, חלבוני G, חיישנים מבניים פלאורוסנטיים, גילוי תרופות