Clear Sky Science · he
פלסטיות תאי T המועדת על‑ידי המיקרוביוטה מאפשרת שליטה על הגידול באמצעות המערכת החיסונית
כיצד חיידקי מעי ידידותיים עשויים לסייע במלחמה בסרטן
אימונותרפיה של סרטן שינתה את הטיפול עבור מטופלים רבים, אך רק חלק מהם רואים את הגידולים שלהם מתכווצים ונמנעים מהישנות. המחקר שואל שאלה שנראית פשוטה אך יש לה השלכות רחבות: האם חיידקים ספציפיים במעי יכולים "לאמן" תאי חיסון באופן שמשפר את יעילות התרופות החוסמות נקודות בקרה, כגון טיפול נגד PD‑1? במעקב אחרי מסלול תאי החיסון מן המעי הדק אל הגידולים בעכברים, המחברים חושפים קישוריות ישירה וניתנת לבחינה בין מיקרואורגניזם יחיד במעי לבין שליטה מוצלחת בגידול.
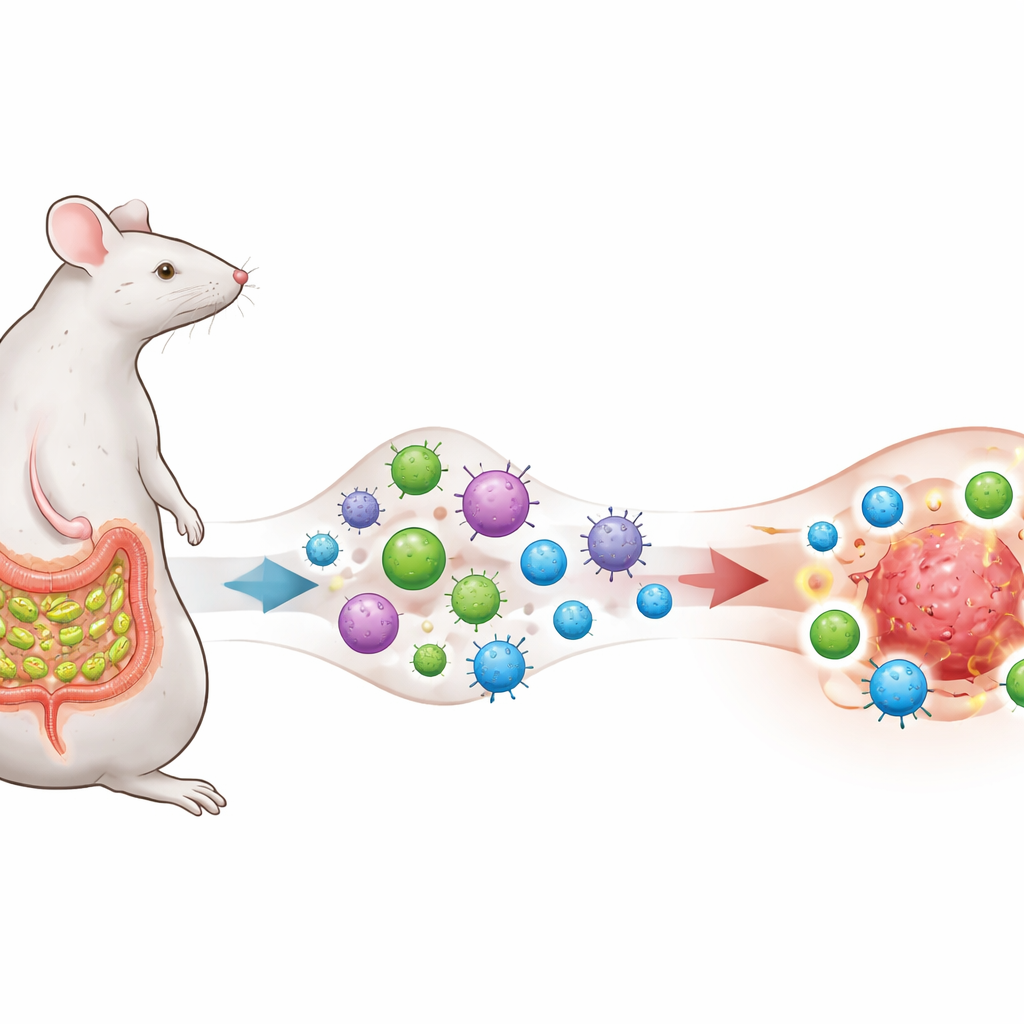
מיקרוב ש"מאמן" את המערכת החיסונית
החוקרים מתמקדים בחיידק מעי הנקרא segmented filamentous bacteria (SFB), הידוע בקיומו סמוך לציפוי המעי הדק בעכברים ובהפעלתו של תגובת תאי עזר מסוג Th17 חזקה שבאופן רגיל תורמת לשמירה על הומאוסטזיס. הם מהנדסים תאי גידול של מלנומה, ריאות ומעי גס כך שיציגו מקטע חלבון המוכר גם ל‑SFB, ובכך יוצרים "חפיפה אנטיגנית" מכוונת בין המיקרוב לגידולים. עכברים נשארים ללא SFB או מושתלים בהם SFB, וכולם מקבלים טיפול נגד PD‑1, נוגדן חוסם נקודות בקרה נפוץ שמטרתו לשחרר את הבלמים מתאי ה‑T.
תאים מאולפים במעי הופכים גידולים מקרים לקרירים ל"חמים" מדלקת
טיפול נגד PD‑1 לבדו, או נוכחות SFB לבדה, אינם מעכבים את גדילת הגידול משמעותית. אך כאשר לגידולים יש את האנטיגן הנגזר מ‑SFB והעכברים מושתלו ב‑SFB, טיפול נגד PD‑1 הופך לפתע ליעיל מאוד: הגידולים מתכווצים, הישרדות משתפרת, ובעלי החיים ששרדו דוחים אתגרים מחודשים של גידול ללא טיפול נוסף, מה שמעיד על זיכרון חיסוני ממושך. אצל עכברים מוצלחים אלה, הגידולים מלאים בתאי CD8 "הרוצחים" אגרסיביים שמייצרים אינטרפרון‑γ ומולקולות טוקסיות נוספות, בעוד שתאי T רגולטוריים מדכאים מהווים חלק קטן יותר מאוכלוסיית החיסון. בקיצור, המיקרו‑סביבה המקומית סביב הסרטן מתעצבנת מ"קרה" יחסית ובלתי תגובתית ל"חמה" ומודלקת.
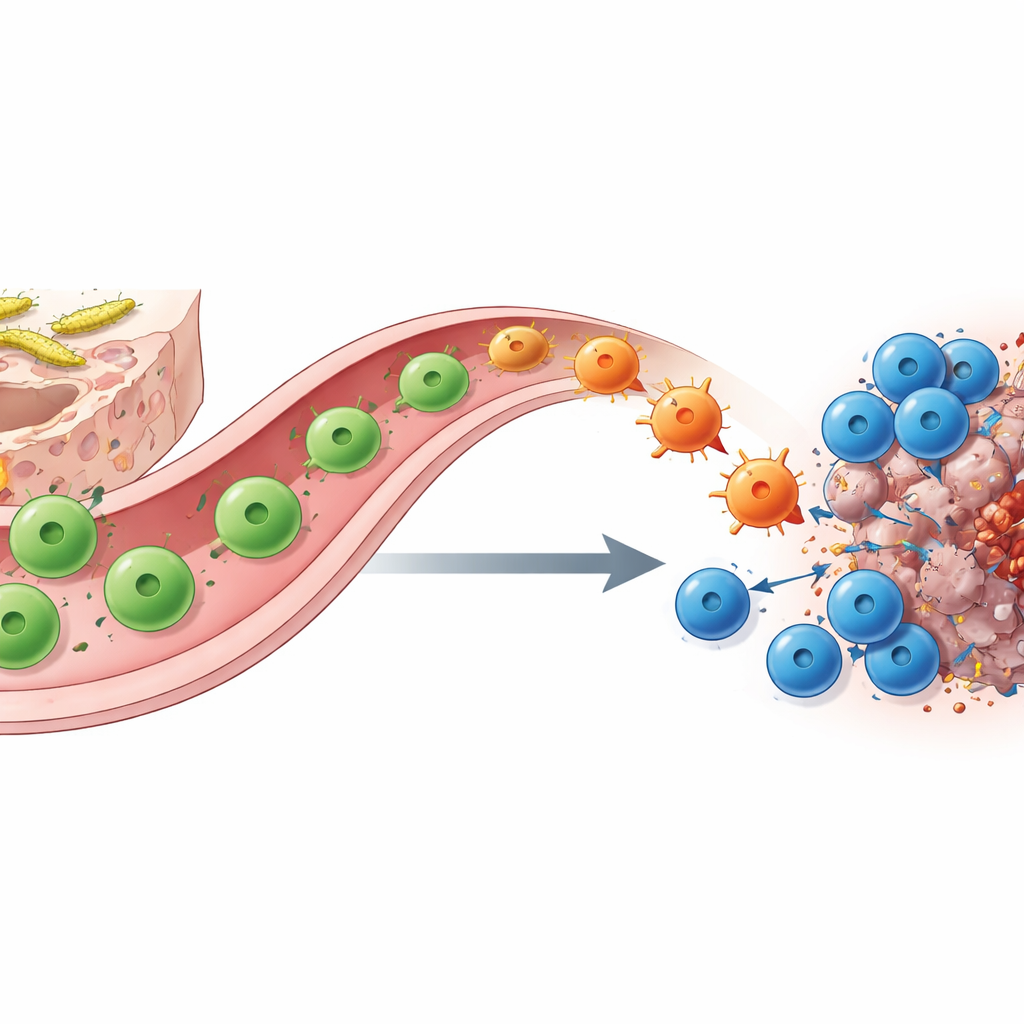
תאי עזר משתני צורה יוצרים גשר בין המעי לגידול
כיצד מושגת ההזזה הזו על‑ידי התיישבות SFB? באמצעות ברקוד מולקולרי, רצף חד‑תאי ומעקב גנטי חכם, המחברים מראים שהשחקנים המרכזיים הם תאי עזר CD4 הספציפיים ל‑SFB. במעי הדק תאים אלו מתחילים כתאי Th17 שתומכים בתפקוד המחסום ומייצרים בדרך כלל את המולקולה IL‑17A. כאשר הם נתקלים באנטיגן תואם בתוך גידול תחת חסימת נקודות בקרה, הם נודדים מהמעי אל אתר הסרטן ומ"משנים התמחות" לסט סוגי Th1‑דומים שמסלקים במקום זאת כמויות נרחבות של אינטרפרון‑γ ו‑TNF. תאי "לשעבר Th17" אלה משפרים הצגה אנטיגנית ומפרישים כימוקינים שמושכים ומעצימים תאי CD8 הרוצחים. הסרה של תאי עזר או רוצחים, או מחיקה גנטית של תאי שושלת IL‑17A שמשמשים כמקורות, מבטלת במידה רבה את תועלת טיפול נגד PD‑1, מה שממחיש את השותפות בין סוגי התאים האלו.
לא כל המיקרובים נותנים הוראות מועילות
כדי לבדוק האם כל חיידק מעי עם חפיפה אנטיגנית יספיק, הצוות חזר על הניסוי עם מיקרוב קבעי שונה, Helicobacter hepaticus. האורגניזם הזה גם מעורר תגובות תאי‑T חזקות אך בעיקר מרחיב תאים בסגנון רגולטורי שמרגיעים דלקת. כאשר הגידולים מתוכנתים להציג אנטיגן של H. hepaticus והעכברים מושתלים בחיידק זה, טיפול נגד PD‑1 אינו משפר את התוצאה. על אף שתאי עזר רבים הספציפיים ל‑H. hepaticus נודדים אל הגידול, הם שומרים על מאפיין רגולטורי ומייצרים מעט אינטרפרון‑γ, וכך אינם מצליחים להניע את תאי הרוצחים. הניגוד הזה מצביע על כך שאיכות ופלסטיות התכניות התאית שמעורר המיקרוב — ולא רק התאמת האנטיגן — קובעות האם המיקרוביוטה תסייע או תפגע באימונותרפיה של הסרטן.
מה המשמעות של זה לטיפול עתידי בסרטן
בסך הכל, העבודה מספקת הוכחה ישירה בחיות כי חיידק מעי מוגדר יכול לאמן מראש תאי עזר במעי, לשלוחם לגידולים החולקים אנטיגן ותחת חסימת נקודות בקרה לגרום להם לשנות תפקיד ולהפוך לתאים רבי עוצמה המתקיפים את הגידול. בהבהרת המעגל מהמעי אל הגידול, המחקר מרמז כי בעתיד ניתן יהיה להשתמש במיקרובים נבחרים או מהונדסים לצד אימונותרפיה כדי להפוך יותר גידולים של מטופלים ליעדים מנוצלים וטועים—בתנאי שהמיקרובים הללו יפעילו את סוג התגובה התאית הגמיש והפרו‑דלקתי הנכון במקום תגובה מרגיעה ורגולטורית.
ציטוט: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
מילות מפתח: מיקרוביוטת המעי, אימונותרפיה של סרטן, פלסטיות תאי T, חסימת נקודות בקרה, מיקרו‑סביבה של הגידול