Clear Sky Science · he
הלחץ שולט בהורשת ההטרוכרומטין באמצעות אוביקוויטילציה של היסטון H3
איך תאים זוכרים לחץ
התאים שלנו צריכים דרכים "לזכור" לחצים שעברו—כגון חום, מחסור בחומרי מזון או חשיפה לתרופות—כדי להגיב מהר יותר בפעם הבאה. מערכת זיכרון עוצמתית נשענת על הטרוכרומטין, דנ״א דחוס שמכבה גנים מסוימים למשך חלוקות תא רבות. המאמר בוחן כיצד תאים מכוונים בצורה פעילה את הזיכרון הזה בתגובה ללחץ, וחושף מרכז מולקולרי שמקשר בין אותות סביבתיים לשינויים ממושכים בפעילות הגנים. הבנת מערכת הבקרה הזו עשויה להסביר כיצד פטריות מפתחות עמידות לתרופות ואיך לחץ משנה את הנוף האפיגנטי בתאים שלנו.
מנעול על הגנום
ניתן לחשוב על הטרוכרומטין כמנעול מולקולרי על מקטעי דנ״א, ששומר על גנים סמוכים בשקט. המנעול הזה בנוי מתגים כימיים על חלבוני היסטון, במיוחד סימן הנקרא H3K9me3. לאחר הקמתו, הוא יכול להעתיק את עצמו בכל שכפול דנ״א, מה שמאפשר דפוסי דיכוי גנים לעבור בירושה ללא שינוי ברצף הדנ״א עצמו. עד כה, רוב המחקר הציע שהעתקה עצמית זו נשענת בעיקר על לולאת משוב "קורא–כותב": קומפלקס אנזימטי מזהה את סימני H3K9me3 הקיימים ומוסיף את אותו הסימן להיסטונים השכנים, ובכך מרחיב בהדרגה את התחום השקט. עם זאת, מודל זה לא הסביר במלואו כיצד תנאים סביבתיים מאיצים, מאטים או מנוים מחדש את התפשטות ההטרוכרומטין.
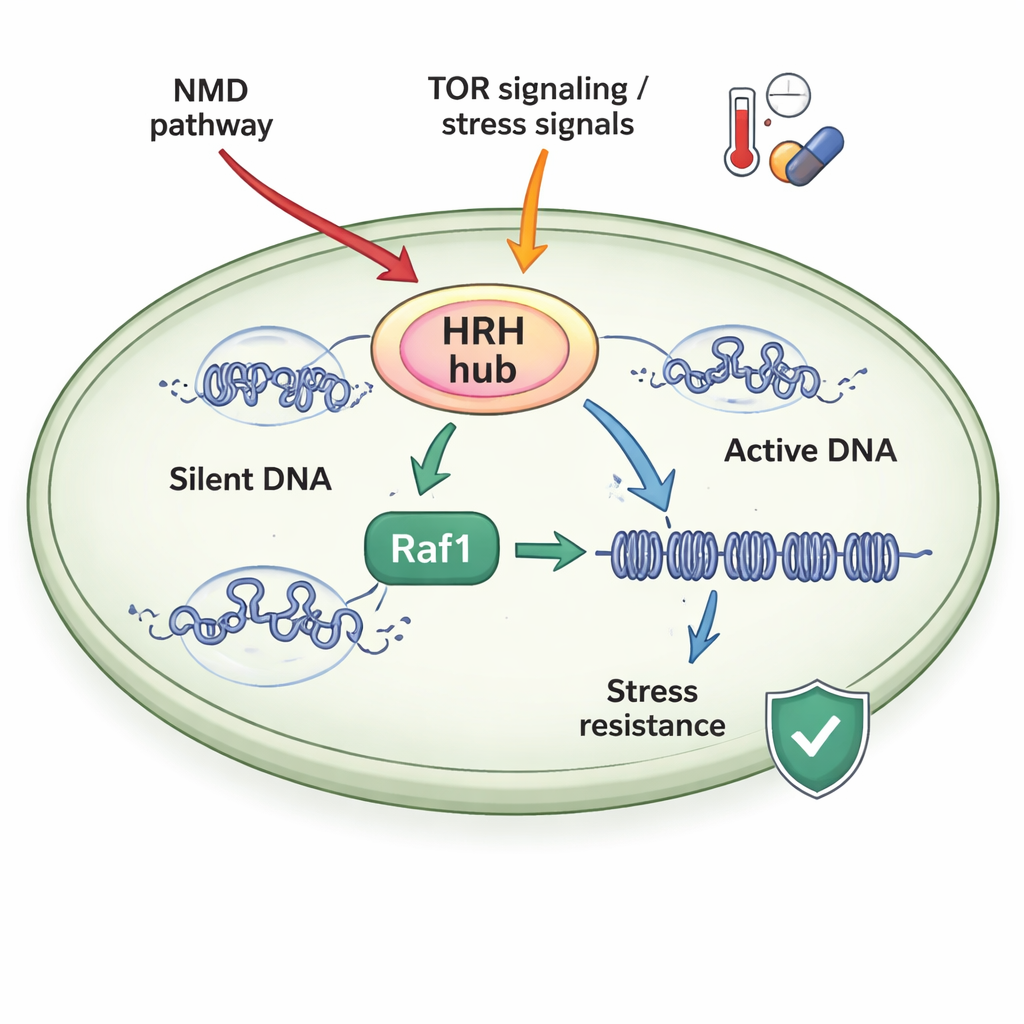
מרכז בקרה רגיש ללחץ
המחברים חקרו את שמרי הפיצול (fission yeast), אורגניזם מודל פשוט שמכונת הכרומטין שלו דומה מאוד לזו של אורגניזמים גבוהים יותר. הם התמקדותו בקומפלקס בשם ClrC, שמוסיף את סימן H3K9me3 ומצמיד חלבון קטן, יוביקוויטין, למיקום אחר בהיסטון H3 (H3K14ub). תת‑יחידה מרכזית של ClrC, Raf1, פועלת כ"שומר סף" מגביל: כאשר כמות Raf1 נמוכה, רוב האנזים העיקרי (Clr4) נשאר חופשי במקום להצטרף לקומפלקס על הכרומטין, ודומיינים שקטים אינם מצליחים להתפשט. כאשר Raf1 בשפע, יותר ClrC מורכב ונקשר בצורה יציבה ל‑DNA, מה שמאפשר לסימני H3K14ub ו‑H3K9me3 להתפרש לאורך הכרומוזומים ולחזק את דיכוי הגנים.
כיוונון עדין של המנעול באמצעות יוביקוויטין
על‑ידי מיפוי סימני הכרומטין ברחבי הגנום, הקבוצה הראתה כי H3K14ub מרוכז מאוד בכל מקום שהטרוכרומטין נוצר וכי סימן זה למעשה נעלם אם מסירים את Raf1. כאשר לתאים יש מוטציה החוסמת את שלב הוספת היוביקוויטין (בעוד H3K9me3 נשאר תקין בנקודת ההתחלה), דומיינים שקטים אינם יכולים להתפשט החוצה. במלים אחרות, H3K14ub אינה רק קישוט; היא דרושה לדחיפת חזית ההטרוכרומטין קדימה. ניסויים ביוכימיים ודמייתיים מסבירים מדוע: H3K14ub משפר באופן משמעותי את פעילות האנזים Clr4 ועוזר לשמור על הקומפלקס מחנה על הכרומטין, מה שמעלה את הצפיפות המקומית של H3K9me3 מעל הסף הנדרש להורשה יציבה. באופן מעניין, הגדלת רמות Raf1 יכולה לעקוף כמה גורמים אחרים שבדרך כלל נדרשים לשימור הדומיינים השקטים, מה שמדגיש כי אוביקוויטילציה מונעת‑Raf1 היא מנוף בקרה מרכזי.
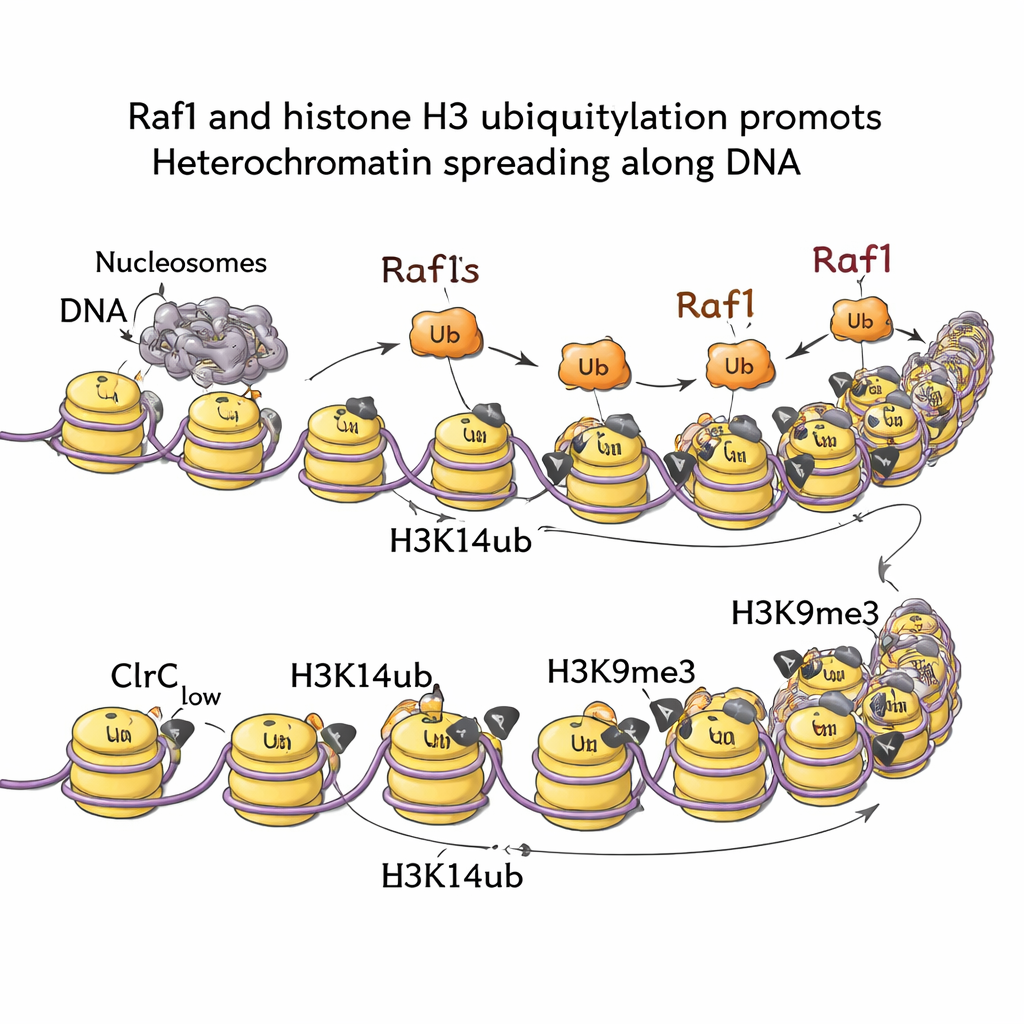
אותות מתהליכי פירוק RNA ונתיבי גדילה
תאים אינם משאירים את רמות Raf1 למקריות. המאמר מראה כי שתי מערכות עיקריות המגיבות ללחץ מזינות את מה שהמחברים מכנים מרכז רגולציה של הורשת הטרוכרומטין (HRH), שמרכזו Raf1. ראשית, מסלול פירוק ה‑nonsense‑mediated decay (NMD)—הידוע בהשמדת mRNA פגומים—מכוון את ה־mRNA המקודד ל‑Raf1, ומשאיר את רמות Raf1 נמוכות בתנאים רגילים. השבתת NMD מייצבת את ה‑RNA של Raf1, מעלה את כמות חלבון Raf1 ומשחזרת את התפשטות ההטרוכרומטין במוטנטים שאחרת אינם יכולים לשמר דומיינים שקטים. שנית, חיישן גדילה ולחץ שנקרא TORC2, הפועל דרך קינאז Gad8, מקדם את ביטוי Raf1. טמפרטורה גבוהה מכבה את המסלול הזה, מורידה את רמות Raf1, מחלישה את ההטרוכרומטין ומקשה על התאים לשמר מצבים שקטים אלא אם כן מעלים את Raf1 בניסוי.
לחץ, עמידות לתרופות והשלכות רחבות
המחברים אז מקשרים את המרכז המולקולרי הזה להתאמה בעולם האמיתי. חשיפת שמרים לקפאין, לחץ הידוע גם כמחליש את NMD במערכות אחרות, מעלה את רמות Raf1 ומשפר את התפשטות ההטרוכרומטין לאתרים חדשים, כולל גנים שאילומים שלהם מקנה עמידות לקפאין ותרופות אנטיפטרייתיות. באופן דומה, תאים שבהם Raf1 מוגבר מלאכותית הופכים לעמידים יותר לפלוקונאזול ולקלוטרימאזול, סוכנים אנטיפטרייתיים נפוצים. לעומת זאת, כאשר Raf1 מוקטן—בגלל חום או בשל אובדן איתות TORC2–Gad8—הטרוכרומטין נעשה בלתי יציב והזיכרון האפיגנטי דוהה, אלא אם כן Raf1 משוחזר. מאחר שחלבוני Raf1‑דמיים, קומפלקס ClrC וסימן H3K14ub קיימים גם בפטריות פתוגניות וביונקים, הממצאים מציעים שמרכז אפיגנטי חיישן־לחץ דומה עשוי לעצב עמידות לתרופות, התפתחות ומחלות במינים רבים.
למה זה חשוב
במונחים יומיומיים, עבודה זו מראה כי דיכוי גנים על‑ידי כרומטין אינו מנעול קשיח אלא מערכת חכמה ומתכווננת. תאים משתמשים במרכז מרכזי כדי לקרוא רמזים סביבתיים—שינויי טמפרטורה, מצב תזונתי, לחצים כימיים—ולכוון את Raf1 למעלה או למטה. זה בתורו קובע כמה מהגנום מכוסה בשקט מתמשך וכמה קל לתאים "לרפרוגרם" את עצמם ללא מוטציות בדנ"א. על ידי גילוי התפקיד המרכזי של אוביקוויטילציה של היסטון H3 ומינון Raf1 בתהליך זה, המחקר מספק שרטוט כיצד לחץ יכול לעצב במהירות את הנוף האפיגנטי—ומרמז על דרכים חדשות להשפיע על עמידות לתרופות בפטריות או על דיכוי גנים חריג במחלות אנושיות.
ציטוט: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
מילות מפתח: הטרוכרומטין, הורשה אפיגנטית, אוביקוויטינציה של היסטון, התאמה ללחץ, עמידות פטרייתית לתרופות