Clear Sky Science · he
ניתוח השוואתי של מערכי סריקה מוטציונית עמוקה בווירוסים אנטרו A ו-B מזהה היפרדות פונקציונלית ומטרות תרפויטיות
מדוע וירוסים זעירים עם RNA חשובים לנו
אנטרו־וירוסים הם קבוצה גדולה של וירוסים זעירים בעלי RNA שמסתובבים בשקט ברחבי העולם, בדרך כלל גורמים להתקררויות קלות או לזיהומי קיבה אך לפעמים מעוררים שיתוק, נזק לבב או מחלות קשות אחרות. יש לנו מעט חיסונים ועוד פחות תרופות שעובדות באופן רחב נגדם, בחלקו משום שהווירוסים הללו מתפתחים במהירות רבה. המחקר הזה שואל שאלה נראית פשוטה אך בעלת השלכות מעשיות משמעותיות: כאשר הווירוסים האלה עוברים מוטציות, אילו חלקים מהמכונות שלהם יכולים להשתנות בחופשיות, ואילו חלקים כה חיוניים שעבורם האבולוציה משמרת יציבות כמעט מוחלטת? התשובות מצביעות על אסטרטגיות חדשות לתכנון טיפולים שקשה לווירוס לעקוף.
קוראים את ספר ההוראות של הווירוס — מוטציה אחת בכל פעם
החוקרים התרכזו בשני אנטרו־וירוסים אנושיים שגורמים למחלות שונות מאוד: אנטרו־וירוס A71, שקשור למחלות נוירולוגיות קשות בילדים, וקוקסאקי B3, המקושר לדלקת לב ואפילו לסרטן הלבלב. באמצעות טכניקה שנקראת סריקה מוטציונית עמוקה הם יצרו ספריות ויראליות שבהן כמעט כל מיקום בחלבוני הווירוס שונה שיטתית. וירוסים מוטנטים אלה הורשו להדביק תאי תרבית, וריצוף מהיר שימש למדידת האופן שבו כל שינוי השפיע על גדילת הווירוס. על ידי השוואת כל מוטנט לווירוס המקורי, הצוות בנה מפת פירוט של האתרים בפרוטאום הווירלי הסולחים שינוי לעומת אלה שמאוד מוגבלים. 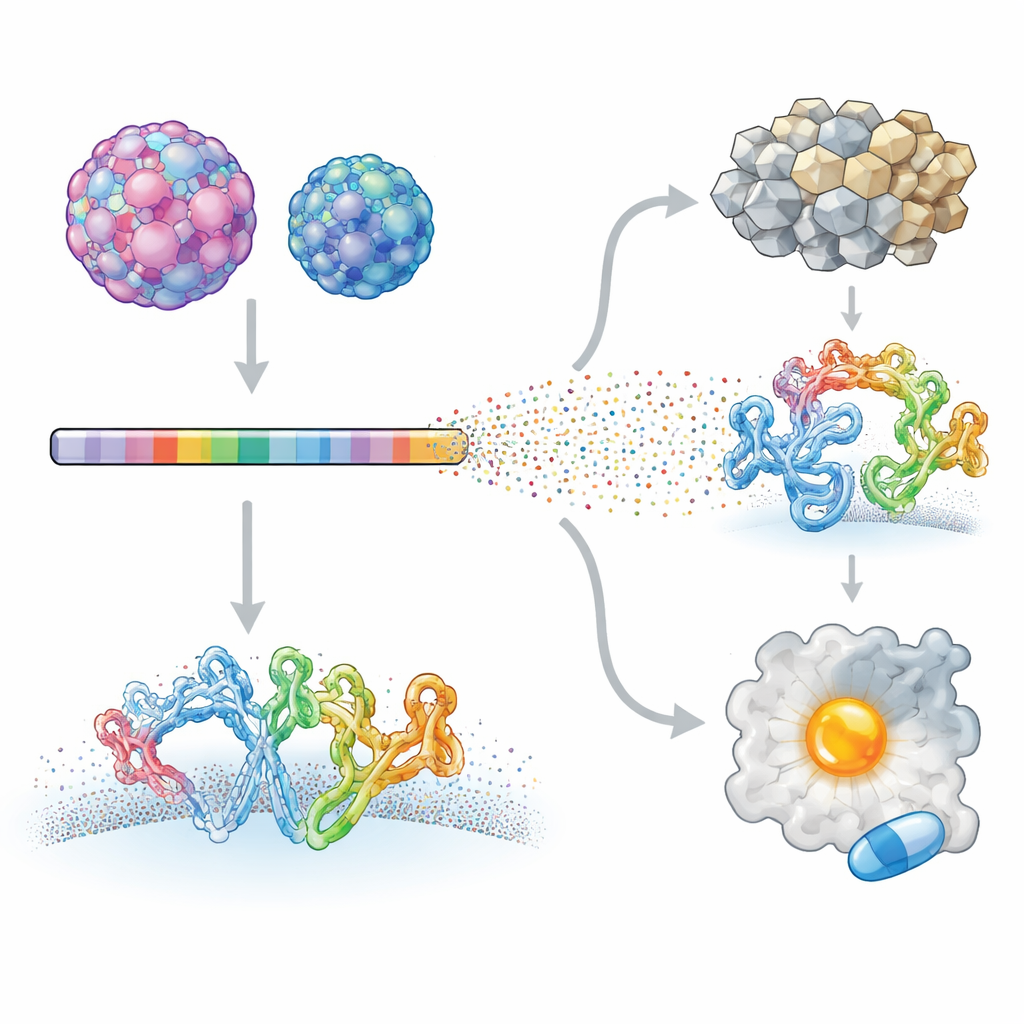
מגבלות קשות משותפות וגמישות ספציפית לכל וירוס
למרות ששתי הוירוסים חולקים רק כ־50% של רצפי חומצות אמינו, הם הראו דפוסי הגבלה כוללים דומים להפליא. ה״סוסים העובדים״ האנזימטיים הפנימיים שמעתיקים את הגנום, חותכים חלבונים ופורמים RNA היו רגישים מאוד למוטציות בשני הוירוסים. בדומה לכך, המשטחים החבויים שמחזיקים יחד את מעטפת החלבון, הקפסיד, הוכחו כקשים לשינוי ללא פגיעה בווירוס. לעומת זאת, אזורים הפונים החוצה ומתקשרים עם המאחסן היו יותר חופשיים להשתנות ולעתים קרובות שונים בצורה חדה בין שני המינים. ניתוח מבני הראה שאזורים שמורים ונטולי־סלחנות למוטציה מקבצים סביב אתרי פעילות וממשקי הרכבה, בעוד שאזורים שנוגעים בקולטנים של המאחסן, בממברנות או במולקולות חיסון היו מוקדי גמישות ספציפית למין.
איך הוירוסים פוגשים תאים ומתחמקים ממערכות ההגנה
הצוות התקרב אז ללחיצת היד המולקולרית בין הווירוס והמאחסן. אנטרו־וירוס A71 וקוקסאקי B3 משתמשים בקולטנים תאיים שונים כדי להיכנס, והמחקר מצא שמסלולי המגע המדויקים על פני שטח הקפסיד הם בין האזורים השונים ביותר מבחינת סלחנות למוטציות. שיירים שמאחזים בקולטן עבור וירוס אחד מוגבלים מאוד בוירוס הזה אך יחסית סלחניים בוירוס האחר, מה שמשקף כיצד כל אחד מהם כינה מחדש את פלטפורמת העגינה שלו. סטייה דומה הופיעה בחלבון קטן קשור לממברנה בשם 3A, המסייע לעצב מחדש ממברנות תאיות ולהשיג גורמי מאחסן לשכפול הגנום. מודלים הציעו ששני הוירוסים משתמשים בחלקי מגע שונים חלקית על גבי 3A כדי למשוך את אותו גורם מאחסן, GBF1, וייתכן שמחדירים חלבון זה לממברנות בעומקים שונים. הבדלים אלה מסבירים מדוע וירוסים קרובים יכולים להדביק רקמות שונות ולעורר דפוסי מחלה מובחנים.
מה האבולוציה במעבדה מפספסת — ומה היא מקבלת נכון
כדי להציב את ניסויי תרביות התאים שלהם בהקשר עולמי, המחברים השוו את מפות המוטציות שלהם לאלפי רצפי וירוס טבעיים מדגימות חולים. באופן כללי, אתרים שהיו גמישים במעבדה נטו גם להיות משתנים בטבע, במיוחד בהשוואות רחבות יותר ברמת המין. עם זאת, כשבדקו אילו חומצות אמino ספציפיות מועדפות בכל אתר, האבולוציה הטבעית ובחירת המעבדה הסכימו הכי קשות בתוך טיפוס וירוס יחיד. באופן בולט, אי־התאמות החמורות ביותר התרכזו על פני שטח הקפסיד החיצוני ועל אזורי מגע עם המאחסן בחלבונים הלא־מבניים 2A ו־3A — בדיוק היכן שתשובות חיסון וסביבות מאחסן מורכבות צפויות להשפיע יותר. ממצאים אלה מרמזים שסוריקה מוטציונית עמוקה לוכדת את המגבלות המכניות הבסיסיות של חלבוני הווירוס, בעוד שזיהומים אמיתיים מוסיפים לחצים נוספים מצד חסינות וטיפיזם רקמתי שקשה לשכפל במבחנה.
מציאת נקודת תורפה משותפת לתרופות עתידיות
לבסוף שאלו החוקרים האם המפות האלה יכולות להדגיש עקב אחילס משותף לפיתוח תרופות. בעזרת כלים חישוביים חיפשו בשני הוירוסים כיסים על פני חלבונים שיכולים, מבחינה עקרונית, לקשור מולקולות קטנות. לאחר מכן חפפו את נתוני המוטציות כדי לראות אילו כיסים בנויים משיירים שהווירוס אינו יכול לשנות בקלות מבלי לפגוע בעצמו. כיס אחד, הממוקם על הליקאזת 2C — מנוע בצורת טבעת המסייע לפרום את ה־RNA הווירלי — בלט. צורתו ושייריו המרכיבים שמורים מאוד בארבעה מיני אנטרו־וירוסים אנושיים עיקריים, הוא ממוקם הרחק מאתרי הפעילות המוכרים, ושינויים בו נדירים בטבע ופוגעים קשות בניסויים במעבדה. 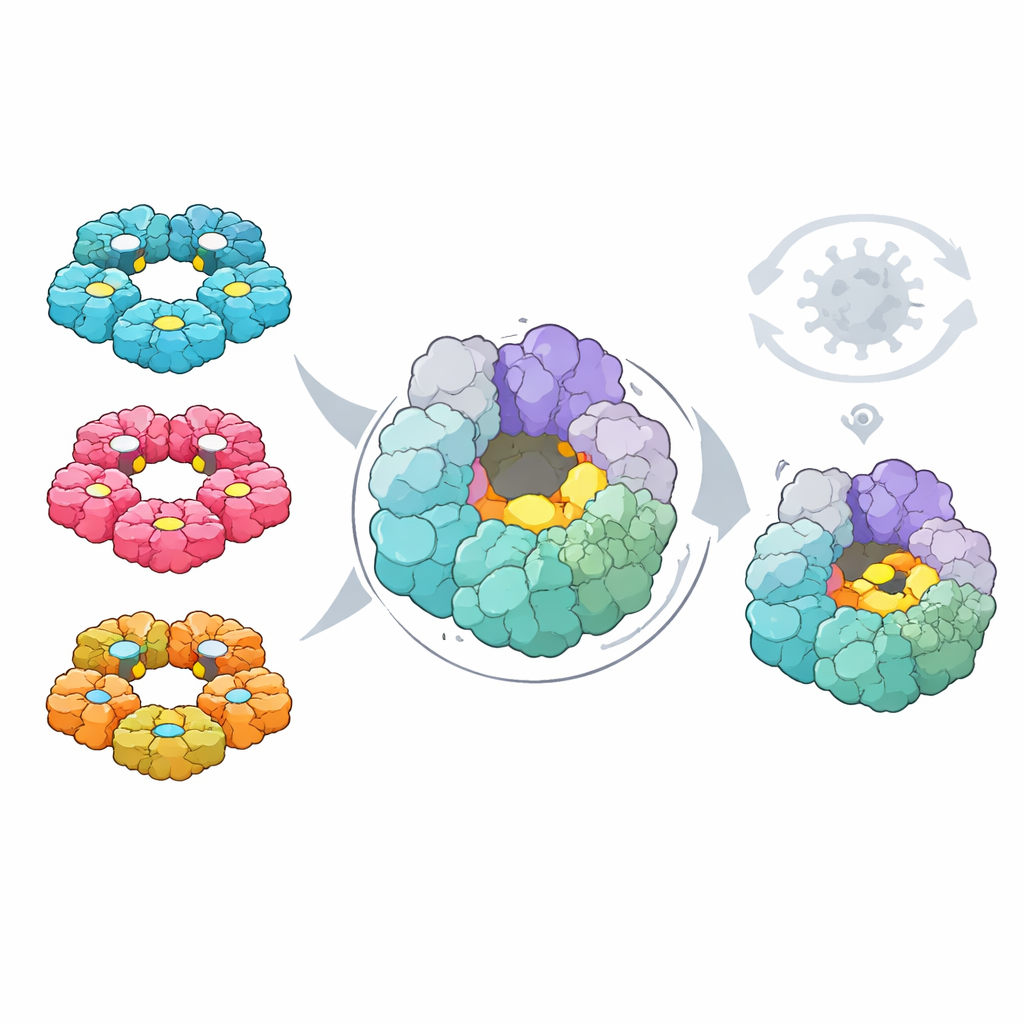
מה משמעות הדברים עבור טיפולים עתידיים
על־ידי חקירה שיטתית של איך כל שינוי אפשרי באות יחידה משפיע על שני אנטרו־וירוסים חשובים, המחקר הזה חושף חלוקה ברורה בין ליבת מכונה ויראלית משותפת וקפדנית לבין ממשקים גמישים ופרטניים המאחים עם המאחסן. הליבה המשמרת כוללת כיס חדש שהודגש על גבי הליקאזת 2C שנראה שקשה לווירוס למוטט מבלי לאבד כושר, מה שהופך אותו למטרה מושכת לאנטי־ויראליים רחבי־טווח עם מחסום גבוה להתנגדות. במקביל, המשטחים החיצוניים והאתרי המגע עם המאחסן שעוברים שינויים בקלות מסבירים מדוע וירוסים קרובים מתנהגים באופן שונה בגוף ומצביעים על האזורים שבהם חיסונים וטיפולים מבוססי חסינות יצטרכו להתמודד עם אבולוציה מהירה. יחד, ממצאים אלה מספקים מפת דרכים לתכנון טיפולים המנצלים את מגבלות האבולוציה של הווירוס.
ציטוט: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
מילות מפתח: אנטרו־וירוסים, אבולוציה ויראלית, סריקה מוטציונית עמוקה, מטרות אנטי־ויראליות, הליקאזת 2C