Clear Sky Science · he
מולקולות פקו-טבעיות מונומולריות ממריצות פירוק של IDO1 על‑ידי E3 הטבעי שלה KLHDC3
כיבוי אנזים התומך בסרטן
מערכת החיסון שלנו סורקת כל העת אחר תאים סרטניים, אך גידולים לעתים קרובות נלחמים בחזרה על‑ידי חטיפת הכימיה הפנימית של הגוף. שחקן מרכזי במאבק הזה הוא אנזים הנקרא IDO1, שעוזר לגידולים לנטרל תאי חיסון. מחקר זה מתאר מעמד חדש של מולקולות קטנות שעושות יותר מאשר לחסום את פעולת IDO1 — הן משכנעות את התאים להיפטר מהאנזים כולו. על‑ידי ניצול מכונת ההשלכת הפסולת הטבעית של התא, תרכובות אלה עשויות להחזיר את ההתקפות החיסוניות על הגידול בדרכים שעלולות לעלות על אלה של תרופות ישנות.
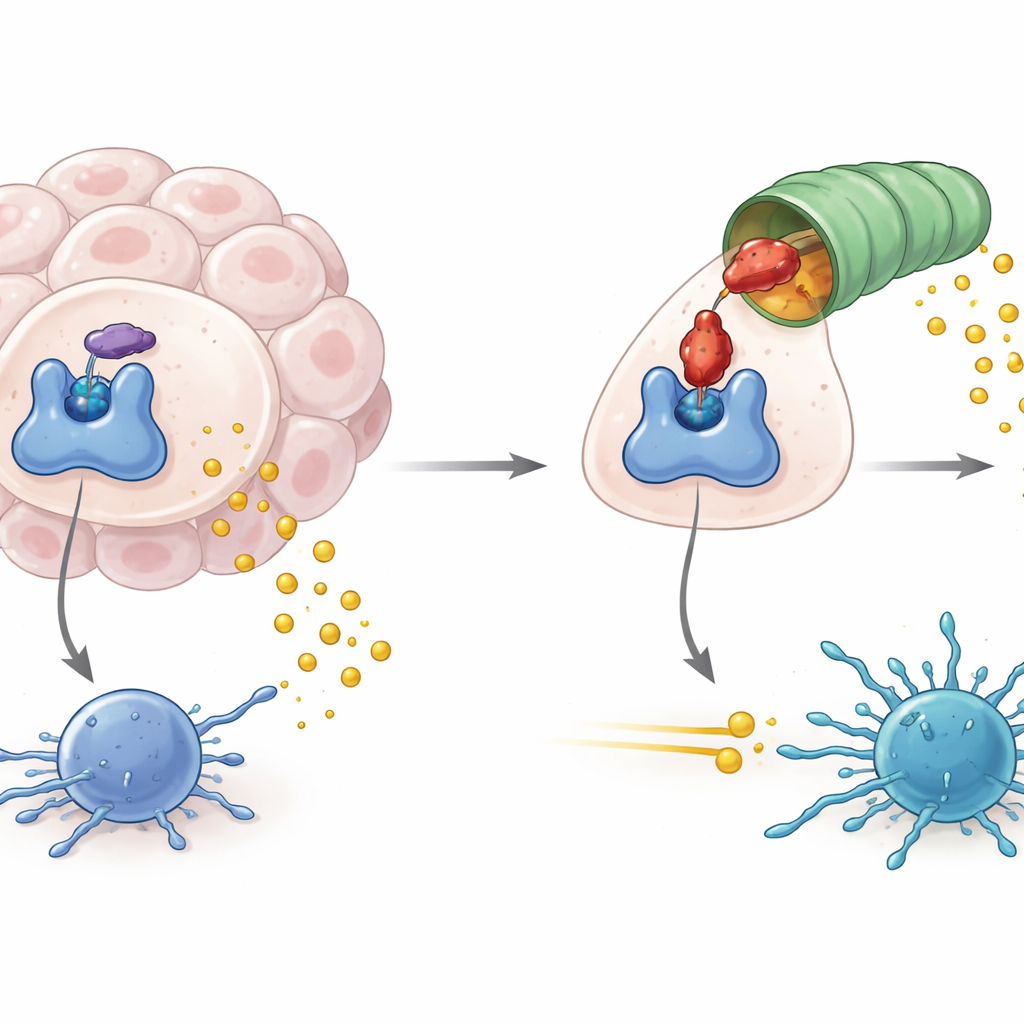
כיצד גידולים מנצלים שומר שער מטבולי
IDO1 יושב בנקודת הכניסה של נתיב מטבולי שמפרק את חומצת האמינו טריפטופן למוצר הנקרא קינורנין. כאשר IDO1 רב ופעיל, רמות הטריפטופן יורדות והקינורנין עולות, ויוצרות סביבה כימית שמדכאת את פעילות תאי החיסון, כולל תאי T הנלחמים בגידול. פעילות גבוהה של IDO1 נקשרה לא רק להחלשת החיסון נגד הגידול אלא גם ללימפומות מוּנעות־ויראלית ולכמה צורות של נוירודגנרציה. לכן מפתחי תרופות התמקדו בחסימת הפעילות האנזימטית של IDO1, בתקווה לנתק את האות המדכא ולשפר את הישימות של אימונותרפיות קיימות.
מדוע חוסמי אנזים פשוטים לא הספיקו
למרות תוצאות מבטיחות בבעלי חיים, נסיונות קליניים של מעכבי IDO1 מסורתיים היו מאכזבים. הסבר שעולה הוא ש‑IDO1 הוא יותר ממזרז פשוט. גם כאשר הפעולה הכימית שלו נחסמת, החלבון עצמו יכול לפעול כמרכז איתות שממשיך לקדם גדילה והפצה של הגידול. חלק מהמעכבים אפילו מייצבים את IDO1, ומשפרים את כמות החלבון בתאים. במילים אחרות, השבתת הפעולה הקטליטית לבדה עלולה להשאיר את תפקידיו הפרו‑גידוליים הלא־אנזימטיים בלתי נוגעים — או גרוע מזה, לחזקם.
עיצוב תרכובות שמפעילות השמדה עצמית
המחברים חיפשו בספרייה רחבה של מולקולות "פקו‑טבעיות" — תרכובות סינתטיות הבנויות מקטעים המושפעים ממוצרי טבע אך משולבות מחדש בדרכים חדשות. הם מצאו משפחת מולקולות, שכינו iDegs, שמקורה בבלוק בונה בצורת צמח בשם (−)-myrtanol. תרכובות אלה נקשרות לכיס הרגיל של IDO1 שמחזיק את הקופקטור המכיל ברזל, ההם. על‑ידי הזזה של ההם, iDegs גם מחלישות את יכולת IDO1 לייצר קינורנין ובמובן הקריטי, מעצבות מחדש חלק מקצה הזנב של החלבון. מבני קריסטל ברזולוציה גבוהה מראים שכאשר iDegs תופסים את אתר ההם, הם משחררים ומפרקים חלקית הליקס סופי (C‑terminal) שבדרך כלל מוחזק במצב קומפקטי ומוגן.
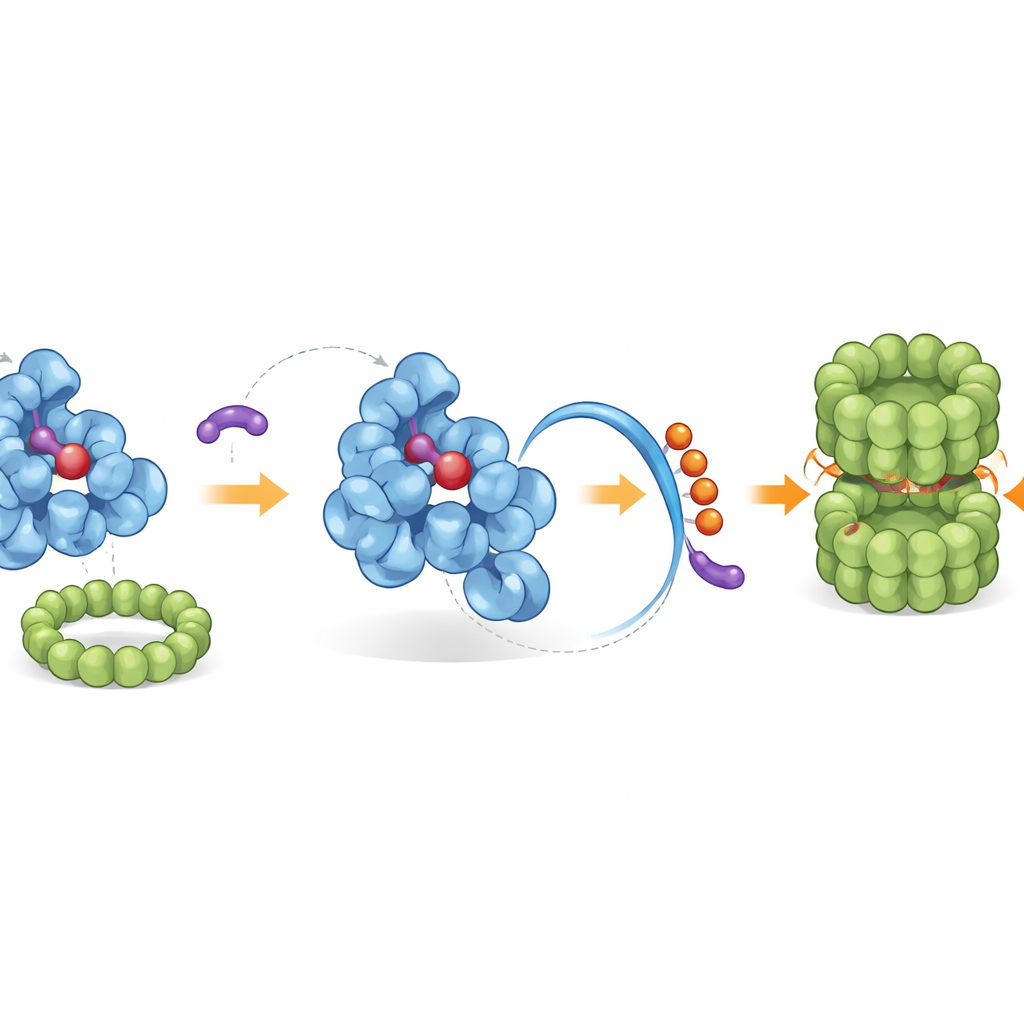
גיוס צוות הניקיון הטבעי של התא
הזנב שהשתנה מעלה "תג־סיום" מובנה שהמכונה להשלכת הפסולת של התא מזהה. באמצעות מסכי גנומים ושחזור ביוכימי, החוקרים זיהו קומפלקס ליגאז ספציפי, בשם CRL2–KLHDC3, שמצמיד באופן טבעי דגלי אוביקוויטין קטנים לזנב החשוף של IDO1, ומסמן אותו להשמדה על‑ידי הפרוטאוזום — הקוצץ המולקולרי של התא. בתנאים רגילים רק הצורה החסרת‑הם של IDO1 מתוייגת ביעילות כך, בעוד ש‑IDO1 קשור־ההם מוגן. iDegs מזיזים את האיזון הזה על‑ידי קשירה רק לצורת ה‑heme‑free, ומגברים את מסלול הפירוק הטבעי. חברים רבי עוצמה בסדרה לא רק חוסמים ייצור קינורנין אלא גם מגבירים את תיוג האוביקוויטין על IDO1 ומקטינים בצורה חדה את רמות החלבון במספר סוגי תאים סרטניים.
שינוי גורלו של IDO1 — והשפעות על התגובה החיסונית
התנהגות דו‑פעולתית זו נושאת השלכות פונקציונליות חשובות. במבחני הגירה עם תאי סרטן השחלות, מעכב IDO1 שנבדק קלינית והיה יציב את האנזים למעשה האיץ את תנועת התאים, בהתאמה לתפקידו הלא‑אנזימטי הפרו‑גידולי של IDO1. לעומת זאת, תרכובת iDeg האטה את ההגירה, בהתאמה גם לחסימת הפעולה האנזימטית וגם לאובדן החלבון עצמו. המחקר חושף אפוא דרך חדשה למניפולציה של IDO1: לא על‑ידי גרירה אל ליגאז זר ומלאכותי באמצעות מולקולה עבה ומתוכננת, אלא על‑ידי "הגברת" מסלול המיחזור הטבעי הקיים בתאים.
מה זה עשוי לה betekenen עבור טיפולים עתידיים בסרטן
ללא מומחים, המסר העיקרי הוא שאיכות — לא רק כמות — החסימה האנזימטית חשובה. המולקולות הקטנות החדשות האלה פועלות כמתגים מדויקים: הן נועלות את IDO1 בצורה פגיעה שהתא מוכן להרוס, וחותכות גם את תרומתו המטבולית וגם את תרומתו האותתית להישרדות הגידול. מאחר ש‑iDegs קומפקטיות, בעלות מאפייני תרופה ושיעבדות להסרת IDO1 על‑ידי הליגאז הטבעי של התא, הן עשויות להציע גישה עדינה ורחבת־שימוש יותר מתרופות "מפחיתות‑חלבון" מוקדמות. אם אסטרטגיות דומות יישומו על חלבונים בעייתיים אחרים, עבודה זו מרמזת על דור חדש של טיפולים שמעודדים תאים חולים לפרק בעצמם את נשקיהם המולקולריים.
ציטוט: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
מילות מפתח: IDO1, אימונותרפיה של סרטן, פירוק חלבון ממוקד, ליגאז אוביקוויטין, מדכאי מולקולות קטנות