Clear Sky Science · he
איזון ליגנדים ביוקומפטיבי בקואורדינציית מתכות מעבר מאפשר ארילציה עדינה של חלבונים בתוך תאים
להפוך מתכות לכלים עדינים בתא
הרבה תגובות כימיות עוצמתיות תלויות במתכות, אך כאשר מקרבים את אותן מתכות לתאים חיים בדרך כלל זה מביא בעיות: נזק, מתח ותמותת תאים. העבודה הזו מציגה כי עם "ידית" מולקולרית מתאימה סביב אטום ניקל, ניתן לבצע תגובה מתוחכמת בתוך תאים חיים ללא נזק משמעותי. הפריצת דרך הזו מאפשרת למדענים לסמן אלפי אתרים ספציפיים בחלבונים ואפילו לעקוב אחר הופעת פתוגנים שקשה לעקוב אחריהם, וכך לפתוח דרכים חדשות למיפוי מה באמת קורה בתוך תאים במצב בריאות ומחלות.
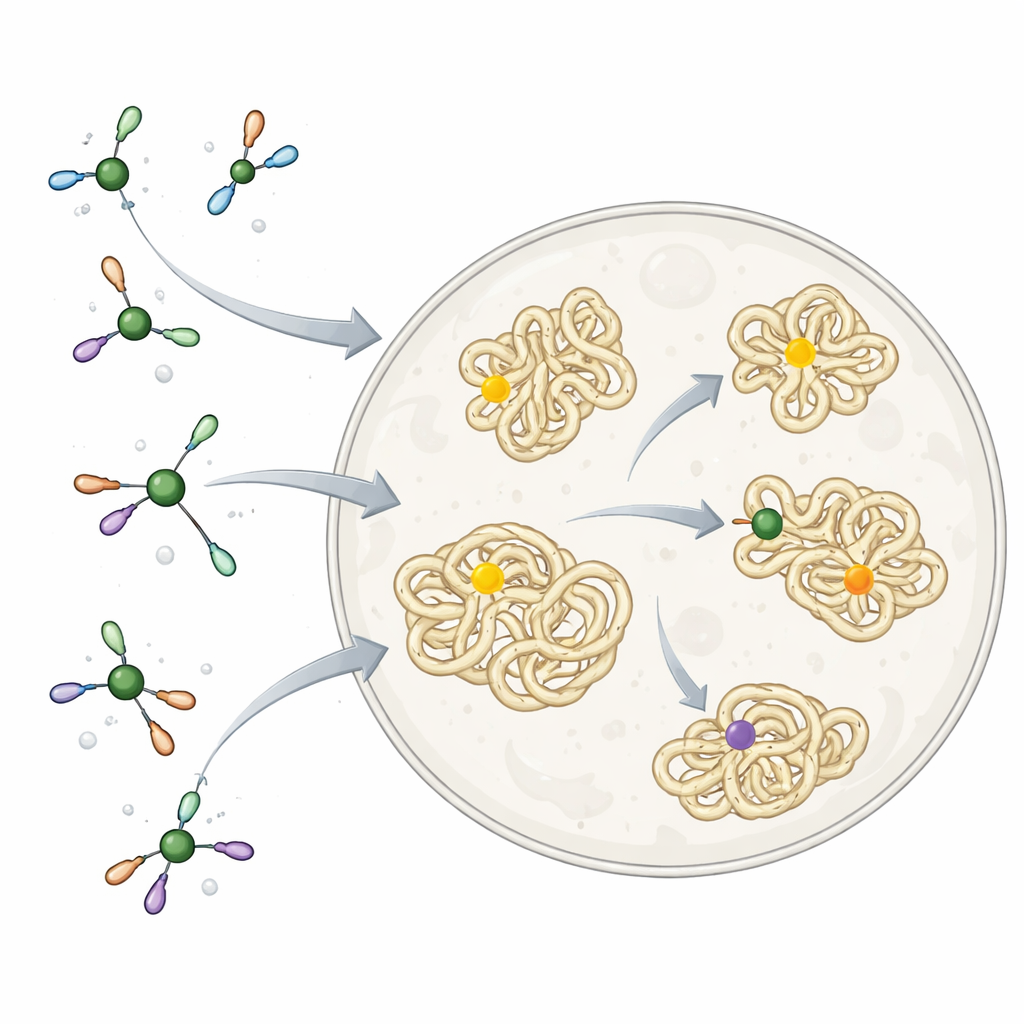
מדוע מתכות הן גם ידידות וגם אויב
ניקל ומתכות אחרות כבר פועלות בשקט בגופנו כחלק מהאנזימים הטבעיים, אך הן יכולות גם להיות רעילות אם נקשרות במקום הלא נכון. הטבע פותר זאת על ידי הקפת המתכות במולקולות קטנות וחלבונים שנבחרו בקפידה, המנווטים אותן ליעדים הנכונים וחוסמים תגובות לא רצויות. כימאים, לעומת זאת, לעתים קרובות משתמשים במגיבים מתכתיים שהם ריאקטיביים מאוד ולא מותאמים כלל לחיים. אלה היו כלים מצוינים לבניית מולקולות מורכבות בכור, אך קשים מדי לשימוש חופשי בתוך תאים, במיוחד כאשר המטרה היא לחבר תג "תג" קטן לחומצת אמינו ספציפית בחלבון מבלי להפריע לשאר התא.
עיצוב מגיב ניקל עדין יותר
החוקרים שאבו השראה מאופן שבו התאים מטפלים בעצמם בניקל. הם בנו מערך של קומפלקסים של ניקל העטופים בליגנד פשוט וביוקומפטיבי בשם TMEDA. מולקולה קטנה זו מתפקדת כמו מהדק רך: הדוק מספיק כדי למנוע מניקל להידבק לרכיבים תאיים לא רצויים, אך רפה דיו כדי לאפשר לו לבצע תגובה מפתח. התגובה מחברת מקטע "אריל" — קבוצת טבעת שטוחה שנפוצה בתרופות — לאטום הגופרית של חומצת האמינו ציסטאין בחלבונים. על חלבונים מטוהרים בתמיסה, הקומפלקסים האלה הצמידו קבוצות אריל במהירות ובסלקטיביות לאתרים יחידים של ציסטאין, ועבדו על רבגוניות של צורות ומיקומים של חלבונים, מה שמראה שהכימיה תואמת באופן רחב למולקולות ביולוגיות אמיתיות.
עריכת חלבונים בתוך תאים חיים
בהמשך, הצוות בדק האם המגיבים הללו יכולים לפעול בתוך תאים חיים מבלי להיות רעילים. הם השוו בין מלחים פשוטים של ניקל, שהם ידועים כפוגעים, לבין קומפלקסי ניקל הקשורים ל‑TMEDA. בתאים של יונקים, מקורות הניקל הפשוטים גרמו למוות תאי משמעותי במינונים יחסית נמוכים, אך הקומפלקסים עם האיזון הליגנדי נשארו נסבלים היטב אפילו בריכוזים מילימולריים. חלון הבטיחות הזה איפשר לחוקרים להשרות תאי חיידקים ותאים של יונקים במגיבי הניקל למשך זמן מספיק כדי שהם ייחדרו ויתקנו חלבונים. על ידי בניית "ידית" אזידית באחת הגרסאות של קבוצת האריל, הם יכלו לבצע תגובת־click לאחר מכן כדי לחבר צבעים זוהרים או תגיות ביטין, ולקבל צביעה ברורה ותלויה מינון של חלבונים בציטופלזמה ובגרעין של תאים חיים.
מיפוי אתרי חלבון ריאקטיביים ברחבי הפרוטאום
עם תגובה בתוך תא שהיא בטוחה ומהירה, החוקרים הפכו אותה לכלי גילוי. הם טיפלו בתאים אנושיים חיים במגיב הניקל המנשא אזיד, ואז השתמשו בתג ביטין הניתן לשחרור בפוטו ומסה ספקטרומטריה מתקדמת כדי לראות בדיוק אילו ציסטאינים שונו. בניסוי יחיד הם זיהו כמעט 11,000 אתרי ציסטאין בכמעט 5,000 חלבונים — בערך פי שניים יותר חלבונים מכל מחקרי מיפוי ציסטאינים בתא חי קודמים יחד. הסימון היה בררני מאוד לציסטאינים והראה הטיה מועטה לסוגי חלבון, מיקומים או אתרי פעילות ידועים מסוימים. באופן מרשים, רבים מהחלבונים הממוקדים נחשבו "לא־ליגנדריים" לפי סטנדרטים נוכחיים של גילוי תרופות, כולל חלבוני איתות בעלי שפע נמוך ומפסקים רגישי‑רדוקס שקשה לחקור בגנטיקה בלבד.
מעקב אחר פתוגנים נסתרים בזמן אמת
הכימיה הזאת הוכיחה גם שהיא רגישה דיו כדי לתפוס חלבונים זרים המיוצרים בזמן זיהום. בתאים אנושיים שנשאבו רצפי וירוס לטנטיים, השיטה גילתה גורמי שעתוק ויראליים שנמצאו ברמות נמוכות מאוד, כולל צורות חיתוך חילופיות. הצוות אז הדביק תאים בשני פתוגנים שונים מאוד: החיידק התוך‑תאי Chlamydia trachomatis והווירוס RNA Sindbis, וירוס קרוב לצ'יקונגוניה. על ידי מתן הדבקה של תאים במגיב הניקל בזמנים שונים, הם יכלו ללכוד אתרי ציסטאין בחלבוני ריבוזומים ורגולטוריים מרכזיים בחיידק כשהוא עבר בין שלבי מחזור החיים, וגם בחלבונים ויראליים לא־מבניים קריטיים שמניעים שכפול RNA. האתרים המסומנים הללו בולטים כעת כנקודות תורפה פוטנציאליות לאסטרטגיות אנטי‑ויראליות או אנטי‑חיידקיות עתידיות.
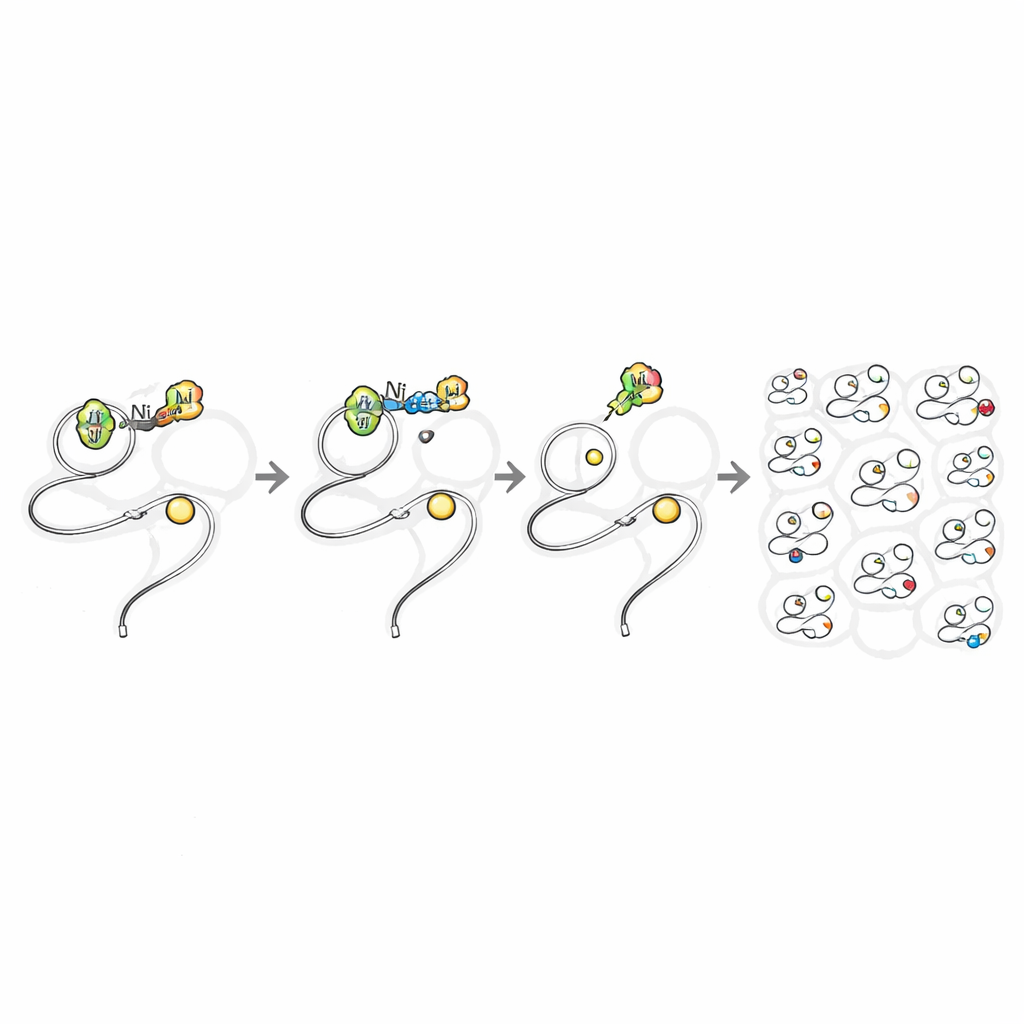
מה משמעות הדבר לכימיה תאית עתידית
על ידי איזון קפדני של מעטפת הליגנדים סביב הניקל, העבודה מראה כי מתכת שלעיתים נחשבת למסוכנת יכולה לבצע תגובת עריכה קוולנטית מדויקת של חלבונים עמוק בתוך תאים חיים עם נזק מינימלי. זה מאפשר לצייר מפת פונקציונלית ומפורטת של אתרי ציסטאין ריאקטיביים ברחבי הפרוטאום, כולל חלבונים שהם נדירים, ארעיים או קשים למטיפול בתרופות. בנוסף, זה מציע דרך לעקוב ולבדוק פתוגנים בתוך תאי המאחסן ברזולוציה של חומצות אמינו יחידות. ברמה רחבה יותר, המחקר מצביע על כך שאפשר לווסת מתכות "אסורות" רבות אחרות בדומה, ולפתוח עידן שבו כלים חזקים של כימיה סינתטית פועלים בבטחה בתוך מערכות חיות.
ציטוט: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
מילות מפתח: מיפוי ציסטאינים, ביוקוניגוגציה על ידי ניקל, תיוג חלבונים בתא חי, כימופרוטאומיקה, מיפוי פרוטאום של פתוגנים