Clear Sky Science · he
התמודדות עם עמידות ל־TKI שממומנת על ידי הנישה הווסקולרית בלוקמיה מיילואידית חריפה באמצעות עיכוב miR-126
למה זה חשוב לחולי סרטן
לוקמיה מיילואידית חריפה (AML) היא אחד מסוגי הסרטן הדמיים האגרסיביים ביותר, ואף עם תרופות ממוקדות מודרניות רבים מהחולים נחזרים. המחקר הזה שואל שאלה שנראית פשוטה אך יש לה השלכות משמעותיות: האם הבעיה אינה רק בתאי הסרטן עצמם, אלא גם ב"השכונה" שבה הם חיים בתוך מח העצם? באמצעות בניית מודל ממוחשב מפורט המושתת על נתוני מעבדה, המחברים בוחנים כיצד כלי דם זעירים יכולים להגן על תאי גזע לוקמיים מפני תרופות — וכיצד חסימת אות RNA קטן אחד עשויה לפרק את ההגנה הזו.
המסתור השקט במח העצם
AML מתפתחת במח העצם, שם תאי הבלסטים הממאירים דוחקים החוצה את יצירת הדם התקינה. בתוך המוני התאים הללו מסתתרים אוכלוסיות קטנות יותר של תאי גזע לוקמיים המסוגלות להתחדש ולהשרוד טיפול, ולנבוט חזרת מחלה. תאי גזע אלה אינם צפים לבד; הם מתחבאים בכיסים מיוחדים סביב עורקים וקפילרות זעירים, הידועים ביחד כנישת הווסקולרית. המחקר מתמקד בחולים שהתאים הלוקמיים שלהם נושאים מוטציות FLT3-ITD, המטופלות במעכבי טירוזין קינאז (TKIs). למרות שתרופות אלה יכולות לצמצם במידה ניכרת את העומס הסרטני, חולים רבים עדיין נחזרים — דבר שמרמז שחלק מהתאים מוסתרים או מוגנים.
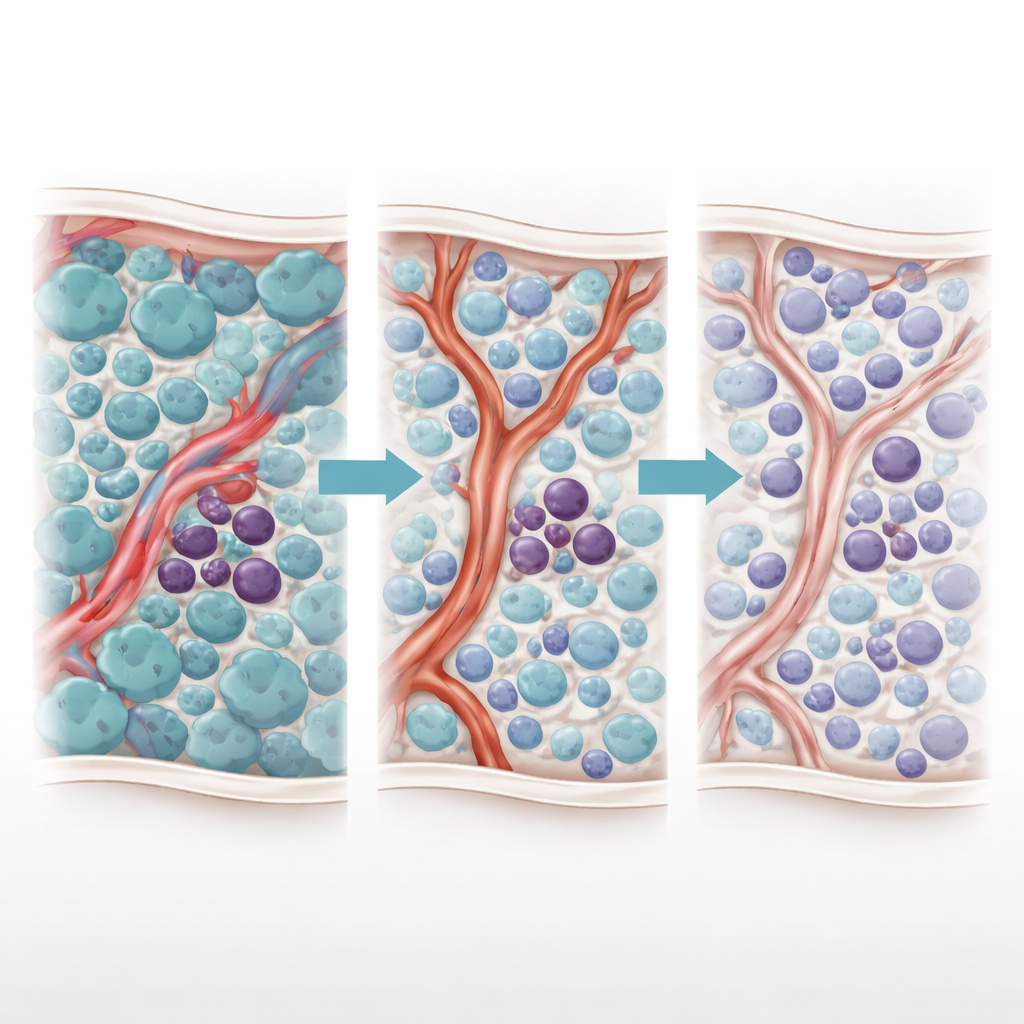
אפקט דו־פני של הטיפול
המחברים חשפו קודם לכן תופעה מסתורית שהם כינו "פנומנון יאנוס" — תגובה דו־פנית לטיפול ב‑TKI. כאשר ה‑TKIs הורגים את תאי הבלסט מתחלקים במהירות, רמות מולקולת דלקתית, TNF-α, יורדות. הנפילה הזו מפתיעה מאפשרת לתאי האנדותל הסמוכים להעלות את הייצור של RNA קטן מווסת בשם miR-126. ה‑miR-126 מועבר מתאים אנדותל לתאי הגזע הלוקמיים, ודוחף אותם למצב שקט, בלתי מחלק, שהופך אותם לעמידים מאוד לתרופות. במילים אחרות, הטיפול שמנקה את מרבית תאי הסרטן מחדש את מח העצם בצורה שמסתירה את המסוכנים ביותר.
בניית מח עצם וירטואלי
כדי לפרוץ את הדינמיקה הזו, הצוות יצר מודל חישובי מבוסס סוכנים של מח העצם ב‑AML. כל שחקן מפתח — תאי בלסט, תאי גזע לוקמיים ותאי אנדותל המצפים את כלי הדם — מיוצג כסוכן עצמאי הפועל לפי חוקים ביולוגיים מודעי־נתונים. מולקולות מפוצלות כדוגמת TNF-α, miR-126, ה‑TKI AC220 ותרופה חוסמת miR-126 בשם miRisten מתפשטות ברקמה המודל. המודל כויל באמצעות נתוני הדמיה בעכברים שממפים תבניות וסקולריות אמיתיות, כולל אזורים עשירים או דלים בכלי דם המייצרים miR-126. בסימולציות, טיפול סטנדרטי ב‑TKI שיחזר באופן אמין את אפקט היינוס: כמות הבלסטים ירדה, TNF-α ירד, miR-126 מכלי הדם עלתה, תאי הגזע נסוגו לנישות המגנות, ולאחר מכן המחלה חזרה.
כיבוי המגן בזמינות מדויקת
מצוידים במערכת הווירטואלית הזו, החוקרים ניסו דרכים לשבור את המעגל המרושע. הוספת miRisten פשוטה במקביל ל‑TKI עזרה אך לעתים רחוקות ריפאה את המחלה במודל. גישה אסטרטגית יותר הייתה עוצמתית יותר: "טיפול מקדים" קצר עם miRisten לבדה להחליש את miR-126 הווסקולרי, ואחר כך מתן TKI לבד או המשך טיפול משולב. במגוון תצורות וסקולריות מדומות, אפילו מספר ימים של טיפול מקדים ב‑miRisten לפני תחילת AC220 הקטינו או חיסלו חזרת מחלה באופן דרמטי תוך צמצום החשיפה הכוללת לתרופות. המודל גם חשף כי כמה קרוב תאי הגזע הלוקמיים יושבים לכלי הדם משפיע בעוצמה על גורלם — תאים המקובצים ממש לצד הכלי זוכים להגנה המרבית אלא אם miR-126 נחסם.
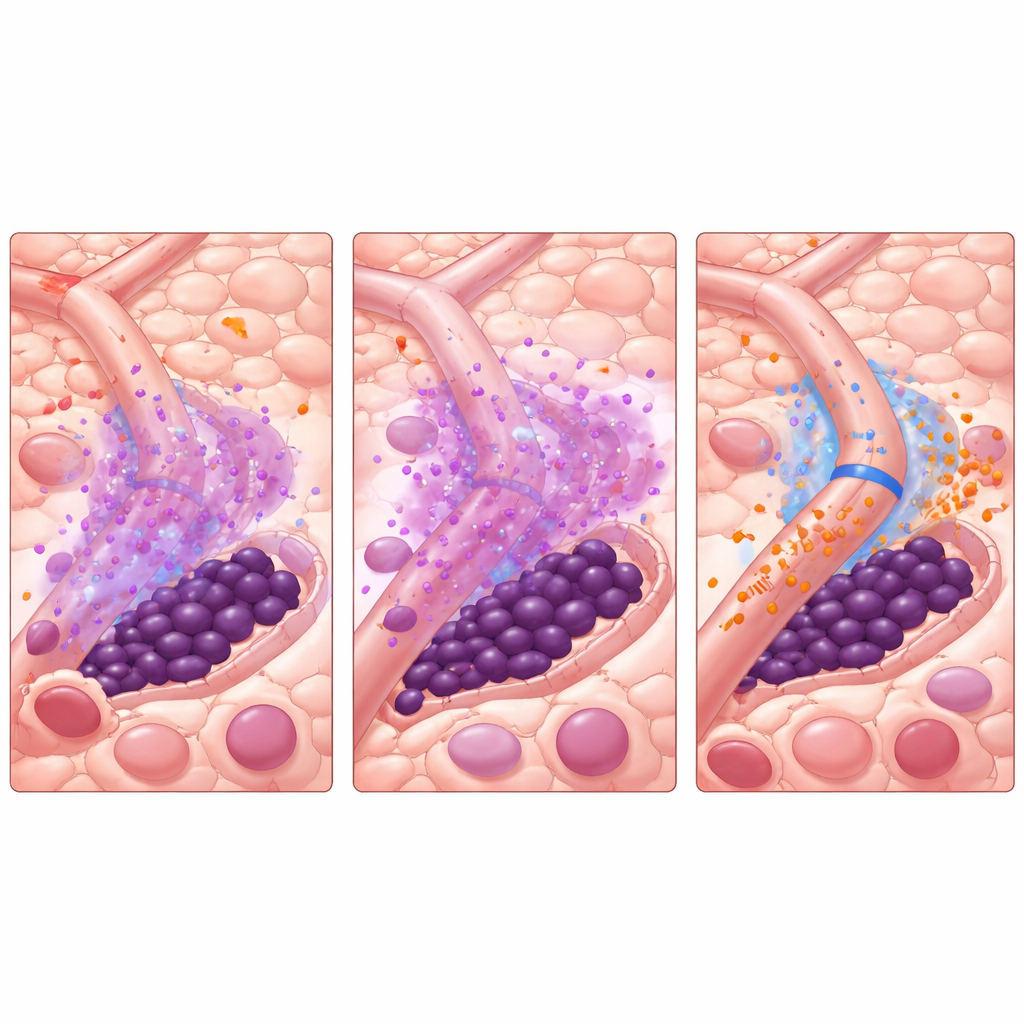
מה המשמעות לטיפול בעתיד
באופן פשוט, המחקר מציע שחלק מתאי הגזע הלוקמיים שורדים לא כי ה‑TKIs חלשים, אלא כי כלי הדם הקטנים במח העצם עוברים באופן זמני למצב "מגן" במהלך הטיפול. על ידי כיבוי קצר של אות יחיד, miR-126, לפני מתן ה‑TKI, ייתכן שאפשר להסיר את המגן הזה, להכריח את תאי הגזע לצאת מהמסתור ולגרום להם להיהרג על ידי תרופות קיימות. אף שעל העבודה הזו מבוססות סימולציות מחשב המעוגנות בנתוני מעבדה — ולא עדיין ניסויים קליניים — היא מציעה אסטרטגיה מוחשית: לתזמן תרופה הממוקדת במיקרו־הסביבה מיד לפני ובמהלך הטיפול הסטנדרטי. אם תאומת, גישה זו עשויה לא רק לשפר את התוצאה בחולים עם AML מוטנטי FLT3, אלא גם להשריש אסטרטגיות דומות במחלות דמיות ומוצקות אחרות שבהן "השכונה" של הגידול מסייעת לו להתחמק מהטיפול.
ציטוט: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
מילות מפתח: לוקמיה מיילואידית חריפה, תאי גזע של לוקמיה, מיקרו־סביבה של מח עצם, עמידות למעכבי טירוזין קינאז, עיכוב miR-126