Clear Sky Science · he
מודלים של למידה עמוקה מזהים שינויים במוח במהלך התקדמות מחלת האלצהיימר
למה חשוב לעקוב אחרי שינוי מוחי לאורך זמן
מחלת האלצהיימר גוזלת לאט את הזיכרון והחשיבה של אנשים, אך הנזק במוח מצטבר שנים לפני שהתסמינים היומיומיים נעשים ברורים. רופאים בדרך כלל מסתמכים על סריקת מוח אחת או תוצאה בודדת של בדיקה כדי לשפוט האם לאדם יש אלצהיימר, אף על פי שהמחלה מתפתחת בהדרגה לאורך זמן. המחקר הזה שואל שאלה פשוטה עם השלכות גדולות: אם נעקוב אחרי סריקות מוח של אנשים לאורך כמה שנים ונאפשר למודל מחשב מתקדם ללמוד מהשינויים הללו, האם נוכל לא רק לזהות את האלצהיימר בצורה מדויקת יותר, אלא גם לראות אילו אזורי מוח נפגעים ראשון ובחומרה?
לעקוב אחרי סיפור המוח, לא רק תמונה אחת
החוקרים השתמשו בסריקות MRI מבניות, שמראות אנטומיה מדויקת של המוח, מיותר מ-280 מבוגרים, כולל אנשים עם אלצהיימר ועמיתים קוגניטיבית תקינים. קריטי לכך שכל אחד מהם עבר שלוש סריקות שנעשו בערך במרווח של שנה, מה שאיפשר לצוות לעקוב כיצד רקמת המוח השתנתה במשך שנתיים. במקום להתייחס לכל סריקה כתמונה נפרדת, הם בנו מודל למידה עמוקה שלוקח בחשבון את כל נקודות הזמן יחד. המודל תוכנן לשים לב לחומר אפור—הרקמה המלאה בגופי תאי העצב—כמו גם לחומר לבן ולנוזל הבהיר המוחי, וללמוד כיצד תבניות ברקמות אלה מתפתחות ככל שהמחלה מתקדמת.
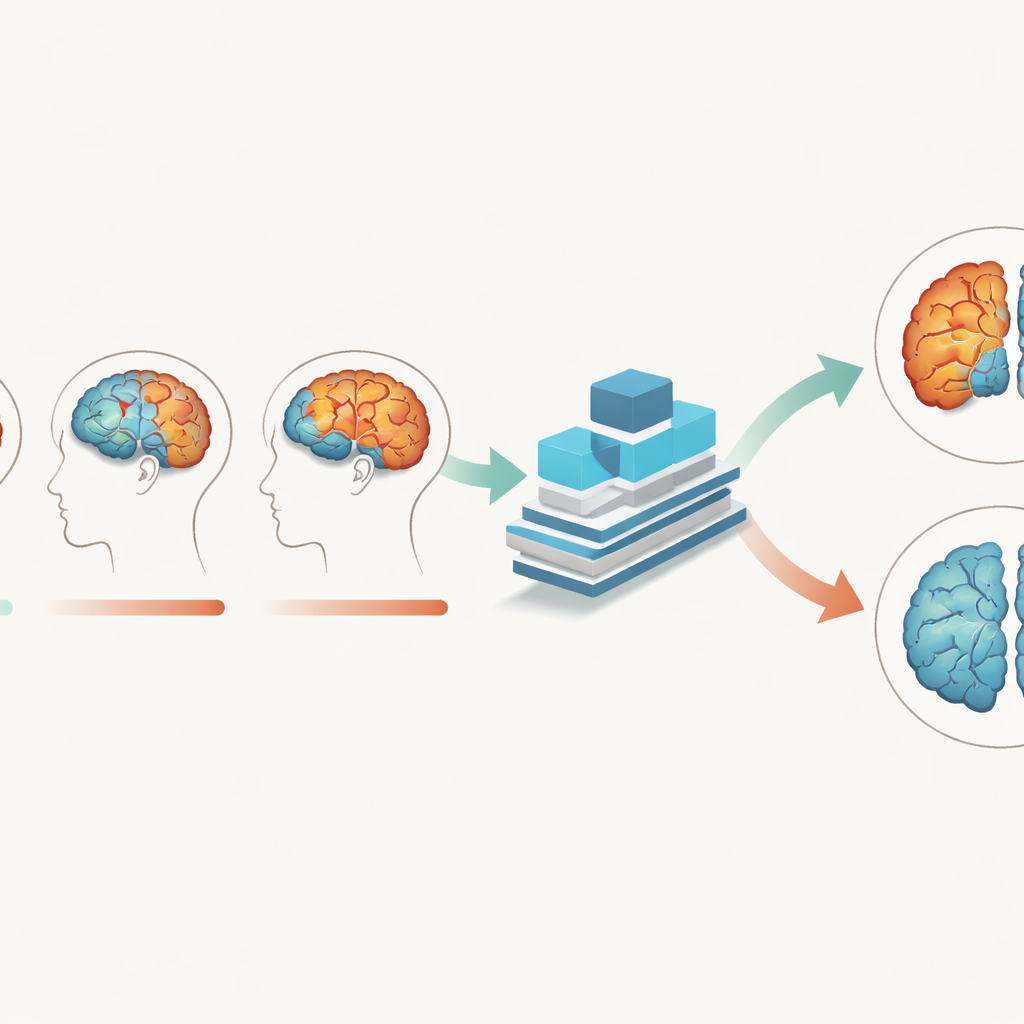
מודל למידה עמוקה המותאם לקצבי שינוי במוח
כדי ללכוד את ההסטים העדינים הללו, הצוות יצר רשת תשומת-לב מיזוג-תת-ענפית (Multi-Branch Fusion Channel Attention Network), רשת עצבית קונבולוציונית תלת-ממדית שמעבדת נפחי MRI במקום תמונות שטוחות. ענפים נפרדים מטפלים ברקמות שונות או בנקודות זמן שונות ואז מאחדים את המידע, בעוד מנגנון "תשומת לב" מסייע למודל להתמקד באזורים התלת-ממדיים הממלאים מידע רב ביותר. מאומן בעיקר על נתוני רקמה אפורה, הרשת למדה להבחין בין מוח של חולי אלצהיימר לבין מוח של הזדקנות נורמלית עם דיוק של כ-93% וספציפיות מושלמת על מערך נתונים אחד, כשהיא עולה על מספר שיטות AI קיימות. היא גם היטהּרה היטב למערך נתונים עצמאי מאוסטרליה, מה שמרמז שאינה סתם שיננה מגרעות של מחקר אחד אלא לוכדת אותות מחלה רחבים יותר.
לראות אילו אזורים במוח משפיעים ביותר
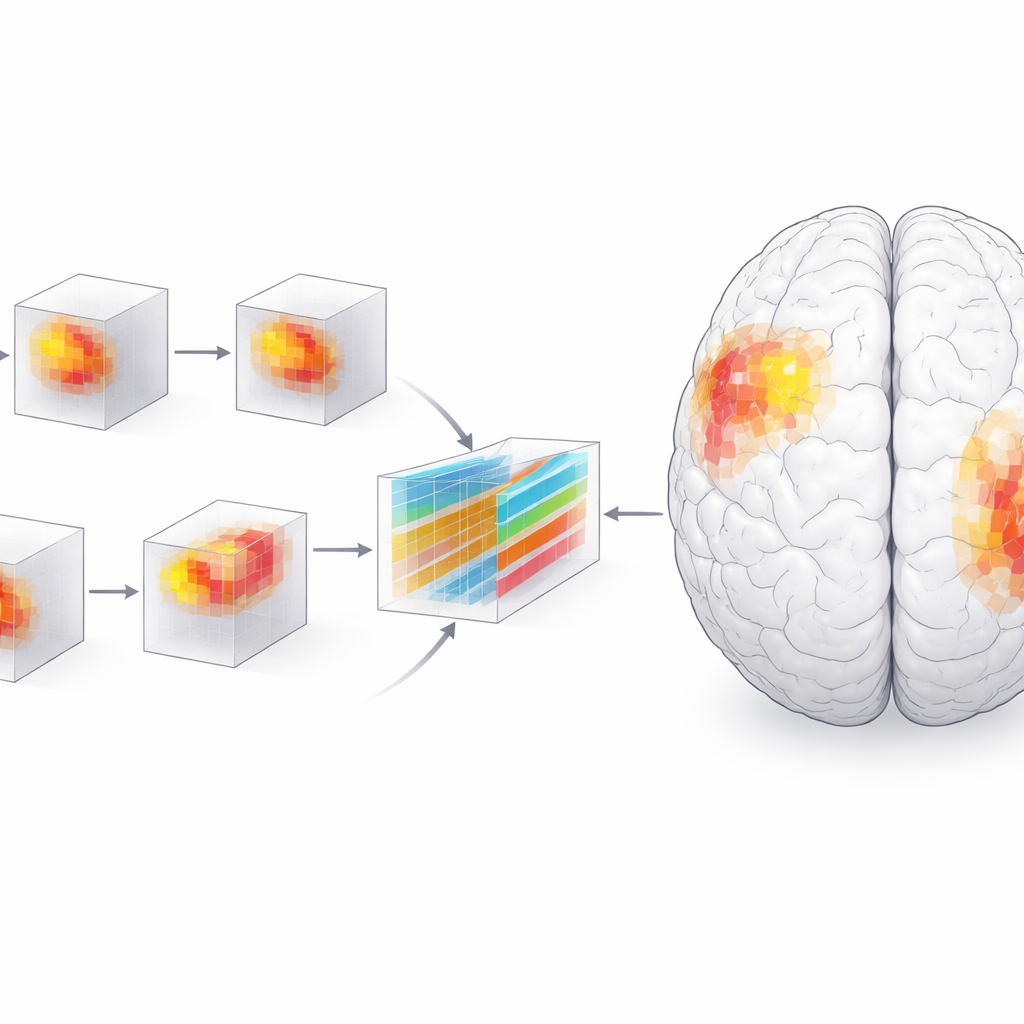
דיוק גבוה מאולי אינו מספיק לרפואה; קלינאים צריכים להבין מה מניע את החלטות המודל. לכן החוקרים השתמשו בטכניקת פרשנות בשם SHAP, שיוצרת ציון חשיבות לכל פיקסל תלת-ממדי קטן—או ווקסל—ב-MRI. קיבוץ הווקסלים לאזורים אנטומיים חשף תמונה דינמית של המחלה. בשלב המוקדם בלטה האמיגדלה, אזור המעורב ברגש וזיכרון, כחשובה במיוחד להבחנה בין חולים לעמיתים בריאים. עם הזמן החלו להשפיע ההיפוקאמפוס, הפאראהיפוקאמפאל גיירוס, ובאופן בולט חלקי האונה הטמפורלית האחורית, בעוד התפקיד היחסי של האמיגדלה נחלש. אחרי שנתיים ההבדלים בין חולים ובקרות היו חדים ומרוכזים יותר, במיוחד בצד השמאלי של המוח.
תבניות שמשקפות תסמינים וציונים קליניים
כדי לבדוק שהמוקד של המודל תואם לביולוגיה, הצוות ביצע ניתוחים מסורתיים של נפח המוח ובדיקות סטטיסטיות. הם מצאו שהחומר האפור באזורים המדגישים הצטמצם מהר יותר בקרב אנשים עם אלצהיימר מאשר במבוגרים שניהלו הזדקנות נורמלית, ושנפח נמוך יותר באזורים אלה התאם לציון גרוע יותר במבחנים קוגניטיביים סטנדרטיים כמו מבחן המצב המנטלי הקצר (MMSE) ודירוג הדמנציה הקליני (CDR). מסלול הנזק—ממבנים טמפורליים פנימיים החוצה לאזורי שפה וקישור אחוריים—שיקף את שלבי הפתולוגיה הקלאסיים של האלצהיימר. עלה גם הטיה לצד שמאל, בהתאמה לדומיננטיות של המוח לשפה ולתפקודים זיכרוניים מסוימים בצד זה. ממורפומטריה מבוססת ווקסלים הראתה ששינויים מוקדמים היו מפוזרים וקטנים, ואז הפכו לגדולים ומרוכזים יותר באזורי הטמפורלי האחורי והמצחי ככל שהמחלה התקדמה.
מה המשמעות עבור מטופלים ורופאים
לשומע שאינו מומחה, המסקנה המרכזית היא שאלצהיימר אינו מתנהג כמו מתג פשוט של כבוי־/דלק במוח; הוא עוקב מסלול מסודר אך מואץ, ומשאיר עקבות מובחנים לאורך הזמן. על ידי כך שמלמדים מודל למידה עמוקה לקרוא לא רק איפה המוח נראה שונה, אלא גם איך ההבדלים הללו מתרחבים לאורך מספר שנים, המחקר הזה מציע דרך לציין את האלצהיימר בדיוק רב יותר ובשלב מוקדם יותר בקורס שלו. הוא גם מזהה קבוצת אזורים מוחיים קטנה—כולל את האמיגדלה, ההיפוקאמפוס, הפאראהיפוקאמפאל גיירוס והקורטקס הטמפורלי האחורי—שגודלם ומבנם המשתנים מקושרים באופן הדוק לירידה קוגניטיבית. בעוד שיש צורך בעבודה נוספת, במיוחד עם שיטות דימות נוספות ומאגרי נתונים גדולים יותר, גישה זו מקרבת אותנו לשימוש בסריקות מוח מרוכבות בזמן וב-AI פרשני ככלים מעשיים לאבחון מוקדם, למעקב ובסופו של דבר להכוונת התערבויות נגד מחלת האלצהיימר.
ציטוט: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
מילות מפתח: מחלת האלצהיימר, MRI של המוח, למידה עמוקה, דימות לאורך זמן, נוירודגנרציה